Диуретики при гипертонии и сердечной недостаточности
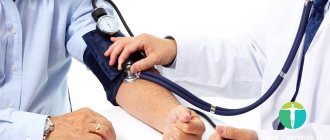
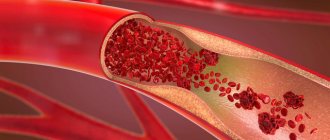
Отеки на лице, нижних, верхних конечностях и туловище возникают в результате нарушения водно-солевого обмена с задержкой натрия, накопления жидкости в тканях и межклеточном пространстве. Основные причины: повышение давления в сосудах (капиллярах, венах и артериях), уменьшение количества белков в плазме крови, снижение функции почек. При кардиоваскулярной патологии отеки свидетельствуют о нагрузке на миокард в результате устойчивого давления. Это симптом гипертонии и СН, что требует незамедлительного лечения.
При подобной патологии диуретики применяют в комбинации с антигипертензивными лекарствами, для улучшения питания сердечной мышцы, возобновления венозного оттока, устранения застоя в легких и уменьшения отдышки.
Используют пять групп мочегонных:
- Петлевые диуретики составляют основную группу. Быстро действуют, улучшают всасываемость натрия и хлора, стимулируя выделение хлора с мочой. За счет этого нормализуется выведение жидкости и уменьшается периферическая отечность.
- Тиазидные препараты действуют иначе: уменьшают обратное всасывание калия и натрия, увеличивая диурез. Бесконтрольный прием опасен гипокалиемией, что требует внимательного расчета дозировки и кратности мочегонного средства. Лекарство противопоказано при почечной недостаточности.
- Калийсберегающие стимулируют выведение солей натрия, что в комплексе улучшает выделение жидкости почками и устраняет отечность тканей. Безопасная группа медикаментов, чаще их назначают для самостоятельного приема для поддержания водно-солевого обмена и профилактики отеков у пациентов с хронической кардиоваскулярной патологией.
- Осмотические диуретики воздействуют на осмолярность плазмы крови, стимулируют почечную фильтрацию. На фоне артериальной гипертензии при сердечной недостаточности их назначают крайне редко, в условиях стационара.
- Мочегонные из группы ингибиторов фермента карбоангидразы повышают всасывание натрия и выведения жидкости почками. Эти препараты влияют на рН мочи, вызывают ацидоз, что требует от врача внимания. В лечении АГ такие диуретики используют не часто.
Показания
В кардиологии для лечения АГ и СН чаще применяют петлевые и тиазидные диуретики. Рекомендованы для устранения отеков разного генеза: почечных, циррозе, задержке жидкости при лишнем весе. Гидрохлортиазид и аналоги показаны при несахарном диабете для уменьшения мочевыделения и разрешены беременным.
«Спиронолактон» и калийсберегающие мочегонные эффективны при застойной кардиальной недостаточности, сочетаются с другими антигипертензивными. Назначают пациентам с синдромом Конна, при вторичном и первичном гиперальдостеронизме. Помогают выводить жидкость в предменструальном периоде, рекомендованы в качестве дополнительного средства при нехватке магния и калия.
Осмотические диуретики прописывают для купирования отека мозговой ткани, при церебральной гипертензии, тяжелой патологии печени с асцитом. У пациентов с эпилепсией или острым приступом глаукомы используют как средство неотложной терапии.
Ингибиторы карбоангидразы чаще применяют в офтальмологии для лечения всех форм глаукомы и неврологии для коррекции судорожных приступов. В кардиологии рекомендованы при неэффективности других мочегонных, артериальном давлении при сердечной недостаточности и отеках, спровоцированных приемом лекарств.
Список рекомендованных препаратов
Выбор лекарственного средства зависит от патологии.
Далее представлен список мочегонных таблеток при гипертонии:
| Группа препаратов | Основные представители | Особенности употребления | |
| 1. | Петлевые | «Фуросемид», «Лазикс», «Торасемид» («Торсид»), «Этакриновая кислота» («Урегит») | «Фуросемид» и аналоги выпускают в таблетках (принимать по 40 мг 1-2 раза в день). Максимальная суточная доза 80-160 мг. При почечной недостаточности до 320 мг. Ампулы 1% внутривенно, по 20-60 мг, в сутки не более 120 мг. «Этакриновая кислота» в таблетках и ампулах по 0,05 г, не больше 0,1 г в день. |
| 2. | Тиазидные | «Гидрохлортиазид», «Индапамид» («Арифон, Равел» | «Гипотиазид» назначают по 0,025-0,05 г в сутки, в тяжелых случаях 0,2 г, 3-7 дней с перерывом 3-4 дня. «Индапамид» по 2,5 мг принимают однократно. |
| 3. | Калийсберегающие | «Спиронолактон», «Верошпирон» | Выпускают в таблетках для перорального приема. Минимальная дозировка – 25мг, при АГ и СН в сутки показан прием 50-100 мг, максимальная – 200 мг. Дозу рассчитывают индивидуально. |
| 4. | Осмотические | «Маннит», «Мочевина» | «Маннитол» вводят в вену по 0,5-1,5 г/кг с 10-20% натрия хлорида или 5% глюкозы. В сутки не больше 140-180 г. |
| 5. | Ингибиторы карбоангидразы | «Диакарб», «Ацетазоламид» («Дихлорфенамид») | Основной представитель – «Диакарб». Применяют в среднем 0,125-0,25 г 1-2 раза в день в течение 2-4 дней, после чего прекращают прием. |
Побочные эффекты и противопоказания
Все мочегонные препараты, что применяются при высоком давлении, на фоне длительного приема вызывают электролитные нарушения в результате потери с мочой калия, магния, натрия и хлора. Выведение жидкости провоцирует изменение рН крови, снижение давления, ухудшение самочувствия с симптомами выраженной слабости, головной боли, судорог. Большие дозы лекарств при сохраненной функции почек приводят к обезвоживанию, гиповолемии. При сгущении крови повышает риск тромбообразования. Возможна индивидуальная чувствительность и развитие аллергии.
Неправильный расчет дозировки и кратности приема петлевых диуретиков провоцирует резкое выведение значительного объема мочи с потерей электролитов. Возникает компенсаторное повышение креатинина и мочевой кислоты, что ухудшает состояние при подагре. У пациентов с диабетом может развиться гиперосмолярная кома. Не показаны для лечения при тяжелой степени нарушения почечной функции, анурии, печеночной энцефалопатии.
При приеме тиазидных средств возможно развитие непереносимости с аллергией и сыпью на коже, диспепсией, сна, психического состояния. Со стороны кардиоваскулярной системы велик риск падения АД на фоне потери жидкости, тахикардии и головной боли. Лекарство противопоказано при почечной недостаточности с клиренсом креатинина <30 миллилитров в минуту, нарушении печеночной функции, декомпенсированном сахарном диабете.
Побочные эффекты калийсберегающих диуретиков связаны с воздействием препарата на обмен веществ и гормональный фон. Возможно повышение мочевины и креатинина с развитием гипохлоремического ацидоза или алкалоза. При длительном приеме гинекомастия у мужчин и сбои менструального цикла у женщин. Аллергические реакции или нарушения кроветворения со снижением числа тромбоцитов. Противопоказан прием лекарств при болезни Аддисона, высоком уровне калия, кальция и натрия в крови, хронической патологии почек, диабете или нефропатии. Не рекомендован при мастопатии, аменореи, раннем климаксе.
Осмотические диуретики не назначают при почечной недостаточности и нарушении кровообращения. Избыточное выведение жидкости провоцирует быстро нарастающую гиповолемию, падение АД с обмороком или развитием галлюцинаций. Неправильно рассчитанные дозы вызывают диспептические явления, острый психоз. Ингибиторы карбоангидразы переносятся хорошо, но при развитии гипокалиемии возникают головокружения, судороги или подергивания в конечностях. На фоне слабости головная боль, дезориентация, нарушение зрения, беспокойство. Препараты не назначают при выраженном ацидозе, болезни Аддисона, глаукоме.
Тиазидные диуретики в лечении артериальной гипертонии
Хлоротиазид – первый тиазидный диуретик, эффективный при приеме внутрь, был создан в 1956 г. В 1957 г. был синтезирован гидрохлоротиазид (ГХТ), который вытеснил хлортиазид из клинической практики благодаря более высокой эффективности. В 1959 г. появился тиазидоподобный диуретик хлорталидон, в 1974 г. – индапамид. Наиболее часто использующимися и, следовательно, наиболее изученными, представителями диуретиков в клинических исследованиях являются хлорталидон, ГХТ и индапамид (в том числе в форме индапамида–ретард). В нашей стране наиболее популярными диуретиками являются ГХТ и индапамид (индапамид–ретард). Однако несмотря на признание клинической ценности этого класса препаратов в последние годы их лидирующие позиции подвергались сомнению, и связано это было прежде всего с обсуждением их метаболических эффектов, с результатами исследования ACCOMPLISH [7] и новым мета–анализом антигипертензивных эффектов ГХТ [8]. Метаболические эффекты диуретиков: мифы и реальность В качестве аргументов против приоритетного применения ТД в качестве препаратов первого выбора используются отрицательные метаболические эффекты на углеводный, липидный и пуриновый обмены, электролитные нарушения. Наиболее значительные дебаты развернулись в последние годы вокруг «диабетогенного» действия ТД. Препарат считается существенным фактором в манифестации сахарного диабета (СД), если, во–первых, количество пациентов с развившимся СД на фоне использования этого препарата больше, чем при естественном течении АГ, и, во–вторых, развитие СД на фоне терапии сопровождается ухудшением клинических исходов. Имеющиеся данные позволяют обсуждать различия между основными классами лекарственных препаратов в отношении развития новых случаев СД. Однако значение существующих доказательств на сегодняшний день следует считать ограниченным, прежде всего ввиду того, что ни в одном из завершившихся крупных контролируемых исследований развитие нового СД не являлось первичной конечной точкой. Анализ 27 рандомизированных контролируемых исследований с включением 158709 пациентов (из них 33395 с СД), сравнивающих влияние «старого» и «нового» режимов антигипертензивной терапии на сердечно–сосудистые события и смертность у пациентов с АГ в зависимости от наличия СД, не выявил различий в снижении риска основных сердечно–сосудистых событий у пациентов с наличием или отсутствием СД на фоне терапии, основанной на иАПФ, АК, АРА II и ТД/БАБ. Более жесткий контроль АД сопровождался значительным снижением основных сердечно–сосудистых событий у пациентов с СД по сравнению с пациентами, не имеющими СД [9]. Следовательно, все современные классы антигипертензивных препаратов, включая ТД, могут быть использованы в лечении АГ. В когортном исследовании ARIC (Atherosclerotic Risk in Community cohort, n=13877) – одном из наиболее методически качественных наблюдений – при анализе подгруппы с АГ (3804 чел.) терапия ТД по сравнению с нелеченными больными не сопровождалась увеличением частоты СД (ОР 0,91, 95% ДИ 0,73–1,13), что существенно не отличалось от данных в отношении иАПФ (ОР 0,98, 95% ДИ 0,72–1,34) или АК (ОР 1,17, 95% ДИ 0,83–1,66) [10]. К достоверному увеличению новых случаев СД приводила лишь терапия ББ (ОР 1,28, 95% ДИ 1,04–1,57; p<0,05). В исследованиях EWPHE, STOP–Hypertension–2, INSIGHT, ALLHAT, LIFE, ASCOT–BPLA в группах, где назначался ТД, действительно отмечалась более высокая частота СД [11–16]. При этом EWPHE, STOP–Hypertension–2, INSIGHT и ALLHAT не выявили преимуществ других препаратов над ТД в отношении исходов [12,13,14,16]. В исследовании LIFE [15] были выявлены различия по первичной конечной точке, в ASCOT–BPLA [11] – по вторичным сердечно–сосудистым исходам, однако следует помнить, что в последних двух исследованиях ТД не были основными препаратами. Представляется важным отметить существенные методические различия при определении новых случаев СД. Например, в исследовании EWPHE оценка новых случаев СД основывалась на сообщениях врачей [12]. Итак, ни в одном из завершившихся исследований новые случаи СД не рассматривались, как первичная конечная точка. Противоречивость результатов в отношении новых случаев СД может быть следствием разного дизайна и продолжительности исследования, размеров выборок, групп сравнения, популяций пациентов, лабораторных методик, лекарственных препаратов и применяемых дозировок. Данные, полученные при сравнении двух режимов терапии, могут в равной мере отражать как положительный эффект одного препарата, так и отрицательный другого. Несмотря на потенциально отрицательное влияние ТД на метаболизм глюкозы, терапия этим классом препаратов приводит к снижению сердечно–сосудистой заболеваемости и смертности у пациентов с АГ. Любые возможные отрицательные метаболические эффекты терапии ТД компенсируются положительным влиянием на другие сердечно–сосудистые конечные точки и общую смертность. Лечение относительно высокими дозами ТД в течение первого года может сопровождаться повышением уровня общего ХС, ХС ЛПНП на 5–7% без существенного влияния на ХС ЛПВП, ни в одном из длительных исследований не выявлено повышения уровня сывороточного ХС на фоне терапии ТД по сравнению с плацебо [17]. Эффективность ТД в отношении частоты инсультов, ИБС, сердечно–сосудистых заболеваний не зависела от исходного уровня ХС в исследовании SHEP [18]. Неблагоприятные эффекты ТД в отношении липидного обмена являются дозозависимыми. На современном этапе ГХТ используется в низких дозах, безопасных с точки зрения влияния на липидный обмен, а индапамид–ретард обладает минимальным эффектом в отношении метаболизма глюкозы и липидов. Влияние длительной терапии ТД на уровни ХС минимально и, возможно, имеет ограниченное клиническое значение. Пациенты могут получать ТД независимо от исходного уровня липидов, особенно учитывая возможность терапии статинами. Риск развития электролитных нарушений (в первую очередь гипокалиемии) определяется исходным содержанием калия в организме, уровнем потребления соли во время лечения, дозами диуретиков. Для современной дозы ГХТ 12,5–25 мг/сут. влияния на уровень сывороточного калия минимальны. Для профилактики гипокалиемии, индуцированной диуретиками, рекомендуется использование минимальных доз диуретиков (ГХТ 12,5–25 мг/сут., индапамид–ретард 1,5 мг/сут.), уменьшение потребления натрия до 2,5 мг/сут., увеличение потребления калия, применение диуретиков в составе комбинированной терапии. Развитие гипокалиемии при назначении низких доз диуретиков является фактором, требующим исключения первичного гиперальдостеронизма [17]. Повышение в сыворотке крови уровня мочевой кислоты, связанное с усилением ее реабсорбции в проксимальных канальцах, является также дозозависимым эффектом терапии ТД [17]. К положительным метаболическим эффектам ТД, которые практически не обсуждаются, относится их способность повышать плотность кости. Лечение ГХТ сопровождается повышением резорбции кальция почечными канальцами, снижением активности общей и костно–специфичной щелочной фосфатазы, благоприятным влиянием на маркеры образования кости (N–телопептид и остеокальцин). В нескольких РКИ оценивалось, улучшает ли ГХТ плотность кости, изучались возможные механизмы, которые могли бы объяснить эти эффекты [19–22]. Так, например, в рандомизированном двойном слепом двухгодичном исследовании сравнивались ГХТ 50 мг/сут. против плацебо у 138 здоровых женщин в постменопаузе [19]. Обнаружены значимые эффекты в группе активной терапии на общую плотность костей голени и предплечья, отсутствие влияния на позвоночник, шейку бедренной кости. ТД оказались способны предотвращать переломы, что особенно важно у пожилых пациентов с остеопорозом (не является отдельным показанием, рассматривается как дополнительный положительный метаболический эффект). По данным когортного исследования с участием 7891 пациента старше 55 лет (средний возраст 68,9 лет), терапия ТД в течение года сопровождалась статистически значимым снижением риска переломов бедра (ОР 0,46, 95% ДИ 0,21–0,96) по сравнению с лицами, не получавшими лечения диуретиками. Однако через 4 мес после прекращения терапии ТД риск переломов соответствовал таковому до лечения [21]. Таким образом, неблагоприятные метаболические эффекты минимально выражены при использовании диуретиков в низких дозах и не приводят к нежелательным клиническим последствиям, а способность ТД влиять на плотность костной ткани и снижать риск развития остеопороза заслуживает внимания в ряде клинических ситуаций. Изменили ли результаты исследования ACCOMPLISH место диуретиков в лечении АГ? Основным результатом исследования ACCOMPLISH (Аvoiding Сardiovascular Events in Сombination therapy in Patients Living with Systolic Hypertension) [7] стало достоверное на 20% снижение относительного риска сердечно–сосудистой заболеваемости и смертности (первичной комбинированной конечной точки) в группе больных АГ высокого риска (n=11506), получавших беназеприл/амлодипин, по сравнению с получавшими беназеприл/гидрохлоротиазид, через 36 мес. наблюдения. На сегодняшний день эт единственное исследование, в котором сравнивались исходы при использовании двух фиксированных комбинаций антигипертензивных препаратов. Предвидя главный вопрос в связи с результатами ACCOMPLISH, должна ли комбинация иАПФ с антагонистом кальция вытеснить комбинацию иАПФ с тиазидным диуретиком, авторы подчеркнули, что «результаты исследования не должны вызывать сомнений в способности диуретиков снижать риск сердечно–сосудистых осложнений у больных АГ» [7]. В качестве объяснения полученных результатов обсуждались особенности группы наблюдения, особенности конечной точки, выбор диуретика, дозы амлодипина и гидрохлоротиазида. Группа наблюдения оказалась популяцией с показаниями для назначения антагониста кальция и относительными противопоказаниями для назначения тиазидного диуретика [3–5]: средний возраст пациентов составил 68 лет, 60% из них имели в анамнезе сахарный диабет, 50% – ожирение, 36% – коронарную реваскуляризацию, 23% – инфаркт миокарда, 11% – анамнез нестабильной стенокардии (не включались пациенты с бессимптомной систолической дисфункцией). Таким образом, популяция ACCOMPLISH была нерепрезентативной, и, следовательно, его результаты не могут быть экстраполированы на всех больных АГ. Кроме того, переносимость терапии комбинацией, включавшей ГХТ, была лучше, чем комбинацией с использованием амлодипина. В состав первичной комбинированной конечной точки не входила госпитализация в связи с сердечной недостаточностью (событие, по способности предотвращать которое антагонисты кальция заведомо уступают другим препаратам, включая тиазидные диуретики) [23,24], но включалась коронарная реваскуляризация (обычно является компонентом вторичной конечной точки). При этом на долю реваскуляризации пришлось более 40% событий, регистрировавшихся в качестве первичной конечной точки. Таким образом, ряд особенностей популяции наблюдения и первичной конечной точки во многом объясняют полученные различия. Другая обсуждавшаяся причина – выбор диуретика с предположением о том, что ГХТ менее эффективен, чем хлорталидон в отношении снижения риска развития сердечно–сосудистых осложнений. Гидрохлоротиазид и хлорталидон различаются по своим фармакокинетическим характеристикам. ГХТ начинает действовать через 2 ч после приема, пик его эффекта наступает через 4–6 ч. При однократном приеме продолжительность действия составляет около 12 ч. При длительном применении продолжительность антигипертензивного эффекта увеличивается и достигает 24 ч. Знание особенностей фармакокинетики ГХТ может уберечь от распространенной ошибки – преждевременной смены тактики терапии. В отличие от ГХТ пик действия хлорталидона наступает через 6 часов. При этом препарат обладает очень большим периодом полувыведения – около 42 часов. Это связано с тем, что хлорталидон накапливается в эритроцитах и медленно высвобождается из них в плазму, обеспечивая продолжительный терапевтический эффект. О том, что фармакокинетические характеристики ГХТ не отразились на контроле АД в исследовании ACCOMPLISH, свидетельствуют результаты подисследования с использованием СМАД, которые подтвердили сопоставимость контроля АД [25]. Мета–анализ, специально посвященный сравнению результатов исследований с использованием хлорталадиона или других ТД, в том числе ГХТ (5 исследований, в 2–х из которых использовался хлорталидон), не выявил существенных различий по влиянию хлорталидона и других ТД на клинические исходы [26]. Таким образом, в настоящее время не существует сильных доказательств в поддержку применения хлорталидона вместо ГХТ. Имеющиеся данные говорят о том, что один из этих двух препаратов следует применять для лечения АГ. Вопрос о преимуществах одного препарата над другим может быть решен только в исследовании с прямым их сравнением. Критику эффективности ГХТ содержал и мета–анализ исследований, в которых сравнивались антигипертензивные эффекты ГХТ с другими препаратами, с заключением, что ГХТ является «слабым препаратом», эффективность которого в современных дозах 12,5–25 мг/сут. «не была доказана ни в одном из рандомизированных контролируемых исследований», и что он «должен быть исключен из числа антигипертензивных препаратов первого выбора» [8]. Необходимо отметить, что в данный мета–анализ включались исследования, в которых ГХТ в суточных дозах 12,5 и 25 мг использовался в качестве монотерапии. Мета–анализу, как методическому подходу, свойственен ряд известных ограничений, и по своей доказательной силе он существенно уступает двойным слепым рандомизированным исследованиям. В двойном слепом рандомизированном исследовании эффективности применения индапамида–ретард, амлодипина или гидрохлоротиазида (Гипотиазида) у пожилых пациентов была показана схожая эффективность режимов терапии [27] (рис. 1). С точки зрения современных рекомендаций по АГ очевидна неактуальность рассмотрения монотерапии диуретиками в качестве стратегии преимущественного выбора. Единым позицией всех современных рекомендаций по АГ является акцент на комбинированную антигипертензивную терапию, и с этой точки зрения очень важным представляется факт, что ГХТ увеличивает эффективность всех без исключения классов антигипертензивных препаратов при использовании в комбинированном режиме. Кроме того, практически все представители классов иАПФ, АРА II и некоторые b–блокаторы имеют форму фиксированных комбинаций, содержащих именно ГХТ в дозе 12,5–25 мг. Более того, именно ГХТ входит в состав первой зарегистрированной фиксированной трехкомпонентной комбинации АРАII, АК и ТД. Все это ставит ГХТ на позиции самого широко применяемого ТД во всем мире. Эффективность ГХТ в качестве стартовой или дополнительной терапии в отношении исходов хорошо изучена в рандомизированных контролируемых исследованиях (табл. 1). Использование препарата в низких дозах сопровождалось улучшением исходов в ряде ранних и современных исследований в области АГ. Так, в плацебо–контролируемом исследовании EWPHE (European Working Party on High blood pressure in the Elderly trial) у пациентов старше 60 лет (средний возраст 72 года) в группе терапии ГХТ 25 мг/сут. и триамтереном 50 мг/сут. отмечалось достоверное уменьшение сердечно–сосудистой смертности, смертности от инфаркта миокарда, число несмертельных цереброваскулярных осложнений [12]. По данным сравнительного исследования MRC Substudy (Medical Research Council trial of treatment hypertension in older adults), в группе больных, получавших диуретики (амилорид 2,5 мг/сут. + ГХТ 25 мг/сут.), достоверно снизился риск развития инсультов, сердечных событий и всех сердечно–сосудистых осложнений по сравнению с группой плацебо. В группе атенолола 50 мг/сут. не выявлено достоверного уменьшения частоты вышеуказанных событий [28]. В исследовании ANBP–2 (Second Australian National Blood Pressure Study) у 6083 пожилых пациентов при равном значительном снижении АД были получены неоднозначные результаты о преимуществах иАПФ перед ГХТ. Ингибиторы АПФ были более эффективны в отношении предотвращения комбинации сердечно–сосудистых событий (ОР 0,89, 95% ДИ 0,79–1,00; p=0,05). При этом в группе иАПФ риск развития смертельного инсульта был почти в два раза выше по сравнению с группой диуретика (ОР 1,91, 95% ДИ 1,04–3,5, p=0,01) [29]. Анализ результатов исследования LIFE, в ходе которого из 9193 больных АГ с ЭКГ–ГЛЖ 70% получали ГХТ дополнительно к основной терапии лозартаном или атенололом в течение 4,8 лет наблюдения [30], был специально адресован вопросу, как прием ГХТ повлиял на исходы. Результаты анализа показали, что дополнительное назначение ГХТ 12,5–25 мг/сут. ассоциировалось с более низкой сердечно–сосудистой заболеваемостью, сердечно–сосудистой и общей смертностью независимо от снижения АД, регресса ГЛЖ и рандомизированной терапии. У больных, получавших диуретик, по сравнению с не получавшими, ОР комбинированной конечной точки составил 0,70 (0,62–0,80), сердечно–сосудистой смерти 0,58 (0,47–0,71), инфаркта миокарда 0,64 (0,51–0,79), инсульта 0,82 (0,68–0,99), смерти от любой причины 0,55 (0,47–0,64). Таким образом, данные рандомизированных контролируемых исследований убедительно демонстрируют способность ГХТ в дозировке 12,5–25 мг/сут. улучшать клинические исходы при АГ и ценность этого препарата в ее лечении. Заключение Тиазидные диуретики по–прежнему остаются краеугольным камнем современной антигипертензивной терапии и являются доступным эффективным классом антигипертензивных препаратов. Это один из классов антигипертензивных препаратов, который в полной мере сохранил свое значение в лечении АГ с момента своего создания. Неблагоприятные метаболические эффекты минимально выражены при использовании тиазидных диуретиков в низких дозах и не приводят к нежелательным клиническим последствиям. Гидрохлоротиазид – один из наиболее изученных диуретиков, входит в большинство фиксированных комбинаций антигипертензивных препаратов и в настоящее время остается одним из наиболее важных препаратов для снижения АД, достоверно уменьшая риск развития сердечно–сосудистых осложнений и снижая смертность от сердечно–сосудистых заболеваний.
Литература 1. Chobanian A.V., Bakris G.L., Black H.R. et al. Seventh report of the Joint National Committee on prevention, detection, evaluation and treatment of high blood pressure. Hypertension. 2003;42:1206–1252. 2. 2003 World Health Organization (WHO)/International Society of Hypertension (ISH) statement on management of hypertension. J Hypertens 2003;21:1983–1992. 3. 2007 Guidelines for the Management of Arterial Hypertension: The Task Force for the Management of Arterial Hypertension of the European Society of Hypertension (ESH) and of the European Society of Cardiology (ESC); Journal of Hypertension. 25(6):1105–1187, June 2007. 4. Диагностика и лечение артериальной гипертензии, Рекомендации Российского медицинского общества по артериальной гипертонии и Всероссийского научного общества кардиологов, приложение 2 к журналу «Кардиоваскулярная терапия и профилактика» 2008; 7(6) 5. Mancia G, Laurent S, Agabiti–Rosei E et al. Reappraisal of European guidelines on hypertension management: a European Society of Hypertension Task Force document. J Hypertens 2009, 27:2121–2158 6. Williams B., Poulter N.R., Brown M.J. et al. British Hypertension Society guidelines for hypertension management 2004 (BHS–IV): summary. BMJ 2004;328:634–64 7. Jamerson K, Weber MA, Bakris GL, et al. Benazepril plus amlodipine or hydrochlorothiazide for hypertension in high–risk patients. N Engl J Med 2008;359:2417–28 8. Messerli FH et al. Hydrochlorothiazide is inappropriate for first–line antihypertensive therapy. ESH Meeting; June 12–16, 2009; Milan, Italy. Abstract LB1.3. 9. Blood Pressure Lowering Treatment Trialists’ Collaboration. Effects of different blood pressure–lowering regimens on major cardiovascular events in individuals with and without diabetes mellitus: results of prospectively designed overviews of randomized trials. Arch Intern Med. 2005;165:1410–9. 10. Gress T.W., Nieto F.J., Shahar E. et al. Hypertension and antihypertensive therapy as risk factors for type 2 diabetes mellitus. N Engl J Med 2000;342:905–912 11. Dahlof B, Sever PS, Poulter NR, et al. Prevention of cardiovascular events with an antihypertensive regimen of amlodipine adding perindopril as required versus atenolol adding bendroflumethiazide as required, in the Anglo–Scandinavian Cardiac Outcomes Trial–Blood Pressure Lowering Arm (ASCOT–BPLA): a multicentre randomised controlled trial. Lancet 2005;366:895–906. 12. Fletcher A., Amery A., Birkenhager W. et al. Risks and benefits in the trial of the European Working Party on High Blood Pressure in the Elderly. J Hipertens 1991;9:225–2230 13. Нansson L., Lindholm L.H., Ekbom T. et al. Randomized trial of old and new antihypertensive drugs in elderly patients: cardiovascular mortality and morbidity the Swedish Trial in Old Patients with Hypertension–2 study. Lancet 1999;354:1751–1756. 14. Mancia G., Broun M., Castaigne A. et al. Outcomes with nifedipine GITS or co–amilozide in hypertensive diabetics and nondiabetics in Intervention as a Goal in Hypertension (INSIGHT). Hypertension 2003;41:431–436. 15. Dahlof B., Devereux R.B., Kjeidsen S.E. et al. Cardiovascular morbidity and mortality in the Losartan Intervention For Endpoint reduction in hypertension study (LIFE): a randomized trial against atenolol. Lancet. 2002;359:995–1003. 16. ALLHAT Officers and Coordinators for the ALLHAT Collaborative Research Group. Major outcomes in high–risk hipertensive patients randomized to angiotensin–converting enzyme inhibitor or calcium channel blockers diuretic: The Antihypertensive and Lipid–Lowering Treatment to Prevent Heart Attack Trial (ALLHAT). JAMA 2002;288:2981–2997. 17. Michael E. Ernst, Pharm.D., and Marvin Moser, M.D. Use of Diuretics in Patients with Hypertension N Engl J Med 2009;361:2153–64. 18. Savage P.H., Pressel S.L., Curb D. et al. Influence of long–term, low–dose, diuretic–based anyhypertensive therapy on glucose, lipid, uric acid, and potassium levels in older men and women with isolated systolic hypertension. Arch Intern Med 1998;158:741–751. 19. Raid I.R., Ames R.W., Orr–Walker B.J. et al. Hydrochlorothiazide reduces loss of cortical bone in normal postmenopausal women: a randomized controlled trial. Am J Med. 2000;109:362–370. 20. LaCroix A.Z., Ott S.M., Ichikawa L. et al. Low–Dose Hydrochlorothiazide and Preservation of Bone Mineral Density in Older Adults: A Randomized, Double–Blind, Placebo–Controlled Trial. Ann Intern Med. 2000;133:516 – 526. 21. Schoofs M., Klift M., Hofman A. et al. Thiazide diuretics and the risk for hip fracture. Ann Intern Med. 2003;139:476–482. 22. Raid I.R., Ames R.W., Orr–Walker B.J. et al. Hydrochlorothiazide reduces loss of cortical bone in normal postmenopausal women: a randomized controlled trial. Am J Med. 2000;109:362–370. 23. Psaty BM, Lumley T, Furberg CD, et al. Health outcomes associated with various antihypertensive therapies used as first–line agents: a network meta–analysis. JAMA 2003;289:2534–44. 24. Costanzo P, Perrone–Filardi P, Petretta M et al. Calcium channel blockers and cardiovascular outcomes: a meta–analysis of 175,634 patients. J Hypertens 2009; 27:1136–1151 25. https://www.medscape.com/viewarticle/702679 26. Barry L. Carter, Michael E. Ernst and Jerome D. Cohen Hydrochlorothiazide Versus Chlorthalidone: Evidence Supporting Their Interchangeability Hypertension 2004; 43;4–9 27. Emeriau JP, Knauf H., Pujadas J.O. et al. A comparison of indapamide SR 1.5 mg with both amlodipine 5 mg and hydrochlorothiazide 25 mg in elderly hypertensive patients: a randomized double–blind controlled study. J Hypertens 2001; 19;343–350 28. Medical research council working party. Medical research counsil trial to treatment of hypertension in older adults: principal results. BMJ 1992;304:405–12. 29. Wing L.M., Reid C.M., Ryan P. et al. Second Australian National Blood Pressure Study Group. A comparison of outcomes with angiotensin–converting–enzyme inhibitors and diuretics for hypertension in elderly. N Engl J Med 2003;348:583–592. 30. Okin PM, Devereux RB; Hille DA et al. Concomitant Hydrochlorothiazide Therapy in Hypertensive Patients is Associated with Reduced Cardiovascular Morbidity and Mortality.
Народные мочегонные средства
Народная медицина предлагает много рецептов натуральных мочегонных средств. Наиболее популярны:
- Отвары из ягод калины и брусники. Для этого сушеные плоды и листья (15 г) залить 200 мл кипятка, настоять 30 минут и процедить. Полученный настой выпивают за 8-12 часов.
- Некоторые натуропаты рекомендуют запаривать березовые почки и молодые побеги. Чайную ложку сухого очищенного сырья проварить на медленном огне в 300 мл воды и отцедить. Полученный чай охлаждают и пьют днем.
- Клюквенный чай помогает от отеков. Для этого понадобится стакан спелых ягод, 250 мл кипятка и 2 ложки сахара. Через 10 минут отвар готов к употреблению.
- Так же диуретически эффектна вода, настоянная на ложке семян и травы укропа.
- Сезонные фрукты и ягоды улучшают диурез. Арбуз, дыня или сельдерей нормализуют выведение жидкости с мочой и помогут избавиться от отеков. Включение в рацион эффективно при похудении.
Доказательная медицина не рекомендует применять народные мочегонные средства при гипертонии с задержкой жидкости. Врачи-кардиологи и терапевты советуют не лечиться самостоятельно, по отзывам других пациентов и внимательно читать инструкцию. Отеки при артериальной гипертензии и кардиальной патологии свидетельствуют об ухудшении насосной функции сердца, что требует приема лекарственных препаратов для предотвращения застоя венозной крови, одышки, отека легких.
Клиническая фармакология тиазидных и тиазидоподобных диуретиков
Эталоны ответов
К комплексному экзамену
По дисциплине «Основы клинической фармакологии»
1. Классификация диуретиков. Клинико-фармакологическая характеристика петлевых и калийсберегающих диуретиков. Показания и противопоказания к применению. Отдельные представители. Особенности применения петлевых и калийсберегающих диуретиков. Побочные эффекты и меры их профилактики. Взаимодействие петлевых и калийсберегающих диуретиков с лекарственными средствами других групп.
Эталон ответа
Диуретики — препараты, влияющие на диурез, имеют различные механизмы действия и влияют на процессы в различных участках нефрона.
Проксимальные канальцы нефрона.В этом участке нефрона происходит активная реабсорбция натрия, сопровождающаяся изотоническим потоком воды в интерстициальное пространство. На реабсорбцию ионов в этом отделе влияют осмотические диуретики и ингибиторы карбоангидразы.
1. Осмотические диуретики(маннитол) — группа препаратов, фильтрующихся в клубочках нефрона, но плохо реабсорбирующихся в дальнейшем. В проксимальных канальцах нефрона они повышают осмотическое давление фильтрата и выделяются почками в неизмененном виде с изоосмотическим количеством воды.
2. Ингибиторы карбоангидразы.Препараты этой группы (диакарб) уменьшают реабсорбцию бикарбонатов в проксимальных канальцах путем угнетения процессов гидратации двуокиси углерода.
Образующиеся в результате этого процесса ионы водорода поступают в просвет канальца в обмен на ионы натрия. Повышение концентрации натрия в просвете канальца приводит к увеличению секреции калия. Потеря организмом бикарбоната может приводить к возникновению метаболического ацидоза, но при этом диуретическая активность ингибиторов карбоангидразы также снижается.
Восходящий отдел петли Генле.Этот отдел нефрона непроницаем для воды, но в нем происходит реабсорбция ионов хлора и натрия. Ионы хлора активно переходят в интерстициальное пространство, увлекая за собой ионы натрия и калия. Реабсорбция воды происходит пассивно по градиенту осмотического давления через нисходящий участок петли нефрона. Здесь точка приложения действия петлевых диуретиков.
Петлевые диуретики(фуросемид) селективно блокируют транспорт Na+, К+, что приводит к увеличению диуреза. Одновременно повышается экскреция ионов магния и кальция.
Дистальный каналец.В разводящем сегменте петли нефрона происходит активный совместный транспорт ионов натрия и хлора в интерстициальное пространство, в результате чего осмотическое давление фильтрата снижается. Здесь происходит реабсобция кальция, который в клетках соединяется со специфическим протеином, а затем возвращается в кровь в обмен на ионы натрия. Здесь точка приложения действия тиазидовых диуретиков.
Тиазидные диуретики (бензтиазид, хлоротиазид)угнетают транспорт ионов натрия и хлора, в результате чего выведение из организма этих ионов и воды повышается. Увеличение содержания ионов натрия в просвете канальца стимулирует процесс обмена ионов натрия на калий и Н+, что может привести к гипокалиемии и алкалозу.
Собирательные трубочкипредставляют собой альдостеронзависимый участок нефрона, в котором происходят процессы, контролирующие гомеостаз калия. Альдостерон регулирует обмен ионов натрия на Н+ и ионы калия. Здесь точка приложения действия калийсберегающих диуретиков.
Калийсберегающие диуретикипонижают реабсорбцию ионов натрия, конкурируя с альдостероном за цитоплазматические рецепторы (спиронолактон)или блокируя натриевые каналы (амилорид).Препараты этой группы могут вызывать гиперкалиемию.
Классификация диуретиков.Диуретики классифицируют по их действию:
• диуретики, вызывающие преимущественно водный диурез (ингибиторы карбоангидразы, осмотические диуретики), действуют преимущественно на проксимальные канальцы нефрона;
• петлевые диуретики с наиболее выраженным диуретическим действием, подавляющие реабсорбцию натрия и воды в восходящем отделе петли Генле. Увеличивают экскрецию натрия на 15—25%;
• тиазидные диуретики, действующие преимущественно в области дистальных канальцев нефрона. Увеличивают экскрецию натрия на 5—10% ;
• калийсберегающие диуретики, действующие преимущественно в области собирательных трубочек. Увеличивают экскрецию натрия не более чем на 5%.
Принципы рациональной терапии и выбор диуретического препарата.Принципиальные моменты в лечении мочегонными средствами:
• назначение слабейшего из эффективных у данного больного диуретиков;
• назначение мочегонных средств в минимальных дозах, позволяющих добиться эффективного диуреза (активный диурез предполагает прибавку 800 — 1000 мл/сут, поддерживающая терапия не более 200 мл/сут);
• применение комбинаций диуретиков с разным механизмом действия при недостаточной эффективности.
Выбор диуретического средства зависит от характера и тяжести заболевания.
Ø В неотложных ситуациях, например при отеке легких, сильные и быстродействующие петлевые диуретики вводят внутривенно.
Ø При выраженном отечном синдроме (например, у пациентов с декомпенсацией хронической сердечной недостаточности) терапию также начинают с внутривенного введения петлевых диуретиков, а в дальнейшем переводят больного на прием фуросемида внутрь.
Ø При недостаточной эффективности монотерапии используют комбинации диуретиков с разным механизмом действия: фуросемид + гидрохлортиазид, фуросемид + спиронолактон.
Ø Комбинацию фуросемида с калийсберегающими диуретиками используют также для предупреждения нарушения баланса калия.
Ø Для длительной терапии (например, при артериальной гипертензии) применяют тиазидные и калийсберегающие диуретики.
Ø Осмотические диуретики показаны для увеличения водного диуреза и предупреждения анурии, для снижения внутричерепного и внутриглазного давления.
Ø Ингибиторы карбоангидразы используют при глаукоме (уменьшает продукцию внутриглазной жидкости), при эпилепсии, при острой высотной болезни, для повышения выведения с мочой фосфатов при тяжелой гиперфосфатемии.
Контроль эффективности и безопасности диуретической терапии.Эффективность терапии оценивается по ослаблению симптомов (одышки при отеке легких, отеков при хронической сердечной недостаточности и т.д.), а также по увеличению диуреза. Наиболее надежный способ контроля эффективности долговременной диуретической терапии — взвешивание больного.
Для контроля безопасности проводимого лечения необходимо регулярно оценивать водно-электролитный баланс и АД.
Клиническая фармакология тиазидных и тиазидоподобных диуретиков
К тиазидным диуретикам относятся гидрохлортиазид, бендрофлуметиазид, бензтиазид, хлоротиазид, циклотиазид, гидрофлуметиазид, метиклотиазид, политиазид, трихлорметиазид, к тиазидоподобным — хлорталидон, клопамид, ксипамид, индапамид, метолазон.
Фармакокинетика.Тиазиды и тиазидоподобные диуретики хорошо всасываются в желудочно-кишечном тракте при приеме внутрь. Хлоротиазид плохо растворим в липидах, хлорталидон медленно всасывается и действует долго.
Связывание с белками высокое. Препараты подвергаются в почках активной канальцевой секреции и поэтому являются конкурентами для секреции мочевой кислоты, которая выводится из организма с помощью этого же механизма. Диуретики выводятся почти полностью почками, индапамид выводится главным образом с желчью.
Показания.Артериальная гипертензия, задержка жидкости, отеки, связанные с сердечной недостаточностью, циррозом печени, отеки при лечении глюкокортикостероидами и эстрогенами, некоторые нарушения функции почек, предупреждение образования кальциевых почечных конкрементов, лечение центрального и нефрогенного несахарного диабета.
Противопоказания.Анурия или тяжелое поражение почек, сахарный диабет, подагра или гиперурикемия, нарушение функции печени, гиперкальциемия или гиперлипидемия, гипонатриемия. Повышенная чувствительность к тиазидным диуретикам или другим сульфаниламидным препаратам.
Гидрохлоротиазид(гипотиазид)
Фармакокинетика.Хорошо всасывается в желудочно-кишечном тракте. В крови на 60% связывается с белками, проникает через плацентарный барьер и в грудное молоко, выводится почками. Начало действия через 30—60 мин, максимум достигается через 4 ч, продолжается 6—12 ч. Т1/2 быстрой фазы равен 1,5 ч, медленной — 13 ч. Продолжительность гипотензивного эффекта 12—18 ч. Гидрохлоротиазид экскретируется более чем на 95% в неизмененном виде, главным образом с мочой (60—80%).
НЛР.Большинство НЛР дозозависимы. Возможно развитие гипокалиемии, слабости, парестезии, гипонатриемии (редко) и метаболического алкалоза, глю-козурии и гипергликемии, гиперурикемии, гиперлипидемии. Диспепсические явления, аллергические реакции, гемолитическая анемия, холестатическая желтуха, отек легкого, узелковый некротический васкулит.
Взаимодействие с другими Л С.При одновременном применении с амио-дароном, дигоксином, хинидином наблюдается повышение риска аритмий, связанных с гипокалиемией. Нестероидные противовоспалительные средства, особенно индометацин, могут противодействовать натрийурезу и повышению активности ренина плазмы, вызываемому тиазидными диуретиками, могут снижать антигипертензивный эффект и объем мочи, возможно, путем подавления синтеза простагландинов или задержки натрия и жидкости. Наблюдается перекрестная повышенная чувствительность с сульфаниламидными препаратами, фуросемидом и ингибиторами карбоангидразы. При одновременном применении с препаратами кальция возможна гиперкальциемия.
Клопамид(бринальдикс)
Фармакокинетика.Препарат хорошо всасывается в желудочно-кишечном тракте, латентный период 1 ч, максимальная концентрация в крови определяется через 1,5 ч, длительность действия 12 ч. 60% препарата выводится с мочой в неизмененном виде.
Взаимодействие с другими ЛС.При одновременном применении снижает эффективность инсулина и других сахаросодержащих средств.
Индапамид(арифон)
Фармакодинамика.Не только оказывает слабое диуретическое действие, но и расширяет системные и почечные артерии. Обладает гипотензивным действием.
Снижение АД объясняется снижением концентрации натрия и уменьшением общего периферического сопротивления из-за снижения чувствительности сосудистой стенки к норадреналину и ангиотензину II, повышения синтеза про-стагландинов (Е,). При длительном применении у больных с умеренной артериальной гипертензией и нарушением функции почек индапамид ускоряет клу-бочковую фильтрацию. Индапамид используется главным образом как гипотензивное ЛС.
Индапамид дает пролонгированный гипотензивный эффект без значительного влияния на диурез. Латентный период 2 нед. Максимальное устойчивое действие препарата развивается через 4 нед.
Фармакокинетнка.Препарат хорошо всасывается в желудочно-кишечном тракте, максимальная концентрация в крови определяется через 2 ч. В крови на 75% связывается с белками, может обратимо связываться с эритроцитами. Т1/2 около 14 ч. 70% экскретируется через почки, остальное — через кишечник.
НЛРпри применении индапамида отмечаются у 5-10% больных. Возможны тошнота, диарея, кожная сыпь, слабость.
Эталоны ответов
К комплексному экзамену
По дисциплине «Основы клинической фармакологии»
1. Классификация диуретиков. Клинико-фармакологическая характеристика петлевых и калийсберегающих диуретиков. Показания и противопоказания к применению. Отдельные представители. Особенности применения петлевых и калийсберегающих диуретиков. Побочные эффекты и меры их профилактики. Взаимодействие петлевых и калийсберегающих диуретиков с лекарственными средствами других групп.
Эталон ответа
Диуретики — препараты, влияющие на диурез, имеют различные механизмы действия и влияют на процессы в различных участках нефрона.
Проксимальные канальцы нефрона.В этом участке нефрона происходит активная реабсорбция натрия, сопровождающаяся изотоническим потоком воды в интерстициальное пространство. На реабсорбцию ионов в этом отделе влияют осмотические диуретики и ингибиторы карбоангидразы.
1. Осмотические диуретики(маннитол) — группа препаратов, фильтрующихся в клубочках нефрона, но плохо реабсорбирующихся в дальнейшем. В проксимальных канальцах нефрона они повышают осмотическое давление фильтрата и выделяются почками в неизмененном виде с изоосмотическим количеством воды.
2. Ингибиторы карбоангидразы.Препараты этой группы (диакарб) уменьшают реабсорбцию бикарбонатов в проксимальных канальцах путем угнетения процессов гидратации двуокиси углерода.
Образующиеся в результате этого процесса ионы водорода поступают в просвет канальца в обмен на ионы натрия. Повышение концентрации натрия в просвете канальца приводит к увеличению секреции калия. Потеря организмом бикарбоната может приводить к возникновению метаболического ацидоза, но при этом диуретическая активность ингибиторов карбоангидразы также снижается.
Восходящий отдел петли Генле.Этот отдел нефрона непроницаем для воды, но в нем происходит реабсорбция ионов хлора и натрия. Ионы хлора активно переходят в интерстициальное пространство, увлекая за собой ионы натрия и калия. Реабсорбция воды происходит пассивно по градиенту осмотического давления через нисходящий участок петли нефрона. Здесь точка приложения действия петлевых диуретиков.
Петлевые диуретики(фуросемид) селективно блокируют транспорт Na+, К+, что приводит к увеличению диуреза. Одновременно повышается экскреция ионов магния и кальция.
Дистальный каналец.В разводящем сегменте петли нефрона происходит активный совместный транспорт ионов натрия и хлора в интерстициальное пространство, в результате чего осмотическое давление фильтрата снижается. Здесь происходит реабсобция кальция, который в клетках соединяется со специфическим протеином, а затем возвращается в кровь в обмен на ионы натрия. Здесь точка приложения действия тиазидовых диуретиков.
Тиазидные диуретики (бензтиазид, хлоротиазид)угнетают транспорт ионов натрия и хлора, в результате чего выведение из организма этих ионов и воды повышается. Увеличение содержания ионов натрия в просвете канальца стимулирует процесс обмена ионов натрия на калий и Н+, что может привести к гипокалиемии и алкалозу.
Собирательные трубочкипредставляют собой альдостеронзависимый участок нефрона, в котором происходят процессы, контролирующие гомеостаз калия. Альдостерон регулирует обмен ионов натрия на Н+ и ионы калия. Здесь точка приложения действия калийсберегающих диуретиков.
Калийсберегающие диуретикипонижают реабсорбцию ионов натрия, конкурируя с альдостероном за цитоплазматические рецепторы (спиронолактон)или блокируя натриевые каналы (амилорид).Препараты этой группы могут вызывать гиперкалиемию.
Классификация диуретиков.Диуретики классифицируют по их действию:
• диуретики, вызывающие преимущественно водный диурез (ингибиторы карбоангидразы, осмотические диуретики), действуют преимущественно на проксимальные канальцы нефрона;
• петлевые диуретики с наиболее выраженным диуретическим действием, подавляющие реабсорбцию натрия и воды в восходящем отделе петли Генле. Увеличивают экскрецию натрия на 15—25%;
• тиазидные диуретики, действующие преимущественно в области дистальных канальцев нефрона. Увеличивают экскрецию натрия на 5—10% ;
• калийсберегающие диуретики, действующие преимущественно в области собирательных трубочек. Увеличивают экскрецию натрия не более чем на 5%.
Принципы рациональной терапии и выбор диуретического препарата.Принципиальные моменты в лечении мочегонными средствами:
• назначение слабейшего из эффективных у данного больного диуретиков;
• назначение мочегонных средств в минимальных дозах, позволяющих добиться эффективного диуреза (активный диурез предполагает прибавку 800 — 1000 мл/сут, поддерживающая терапия не более 200 мл/сут);
• применение комбинаций диуретиков с разным механизмом действия при недостаточной эффективности.
Выбор диуретического средства зависит от характера и тяжести заболевания.
Ø В неотложных ситуациях, например при отеке легких, сильные и быстродействующие петлевые диуретики вводят внутривенно.
Ø При выраженном отечном синдроме (например, у пациентов с декомпенсацией хронической сердечной недостаточности) терапию также начинают с внутривенного введения петлевых диуретиков, а в дальнейшем переводят больного на прием фуросемида внутрь.
Ø При недостаточной эффективности монотерапии используют комбинации диуретиков с разным механизмом действия: фуросемид + гидрохлортиазид, фуросемид + спиронолактон.
Ø Комбинацию фуросемида с калийсберегающими диуретиками используют также для предупреждения нарушения баланса калия.
Ø Для длительной терапии (например, при артериальной гипертензии) применяют тиазидные и калийсберегающие диуретики.
Ø Осмотические диуретики показаны для увеличения водного диуреза и предупреждения анурии, для снижения внутричерепного и внутриглазного давления.
Ø Ингибиторы карбоангидразы используют при глаукоме (уменьшает продукцию внутриглазной жидкости), при эпилепсии, при острой высотной болезни, для повышения выведения с мочой фосфатов при тяжелой гиперфосфатемии.
Контроль эффективности и безопасности диуретической терапии.Эффективность терапии оценивается по ослаблению симптомов (одышки при отеке легких, отеков при хронической сердечной недостаточности и т.д.), а также по увеличению диуреза. Наиболее надежный способ контроля эффективности долговременной диуретической терапии — взвешивание больного.
Для контроля безопасности проводимого лечения необходимо регулярно оценивать водно-электролитный баланс и АД.
Клиническая фармакология тиазидных и тиазидоподобных диуретиков
К тиазидным диуретикам относятся гидрохлортиазид, бендрофлуметиазид, бензтиазид, хлоротиазид, циклотиазид, гидрофлуметиазид, метиклотиазид, политиазид, трихлорметиазид, к тиазидоподобным — хлорталидон, клопамид, ксипамид, индапамид, метолазон.
Фармакокинетика.Тиазиды и тиазидоподобные диуретики хорошо всасываются в желудочно-кишечном тракте при приеме внутрь. Хлоротиазид плохо растворим в липидах, хлорталидон медленно всасывается и действует долго.
Связывание с белками высокое. Препараты подвергаются в почках активной канальцевой секреции и поэтому являются конкурентами для секреции мочевой кислоты, которая выводится из организма с помощью этого же механизма. Диуретики выводятся почти полностью почками, индапамид выводится главным образом с желчью.
Показания.Артериальная гипертензия, задержка жидкости, отеки, связанные с сердечной недостаточностью, циррозом печени, отеки при лечении глюкокортикостероидами и эстрогенами, некоторые нарушения функции почек, предупреждение образования кальциевых почечных конкрементов, лечение центрального и нефрогенного несахарного диабета.
Противопоказания.Анурия или тяжелое поражение почек, сахарный диабет, подагра или гиперурикемия, нарушение функции печени, гиперкальциемия или гиперлипидемия, гипонатриемия. Повышенная чувствительность к тиазидным диуретикам или другим сульфаниламидным препаратам.
Гидрохлоротиазид(гипотиазид)
Фармакокинетика.Хорошо всасывается в желудочно-кишечном тракте. В крови на 60% связывается с белками, проникает через плацентарный барьер и в грудное молоко, выводится почками. Начало действия через 30—60 мин, максимум достигается через 4 ч, продолжается 6—12 ч. Т1/2 быстрой фазы равен 1,5 ч, медленной — 13 ч. Продолжительность гипотензивного эффекта 12—18 ч. Гидрохлоротиазид экскретируется более чем на 95% в неизмененном виде, главным образом с мочой (60—80%).
НЛР.Большинство НЛР дозозависимы. Возможно развитие гипокалиемии, слабости, парестезии, гипонатриемии (редко) и метаболического алкалоза, глю-козурии и гипергликемии, гиперурикемии, гиперлипидемии. Диспепсические явления, аллергические реакции, гемолитическая анемия, холестатическая желтуха, отек легкого, узелковый некротический васкулит.
Взаимодействие с другими Л С.При одновременном применении с амио-дароном, дигоксином, хинидином наблюдается повышение риска аритмий, связанных с гипокалиемией. Нестероидные противовоспалительные средства, особенно индометацин, могут противодействовать натрийурезу и повышению активности ренина плазмы, вызываемому тиазидными диуретиками, могут снижать антигипертензивный эффект и объем мочи, возможно, путем подавления синтеза простагландинов или задержки натрия и жидкости. Наблюдается перекрестная повышенная чувствительность с сульфаниламидными препаратами, фуросемидом и ингибиторами карбоангидразы. При одновременном применении с препаратами кальция возможна гиперкальциемия.
Клопамид(бринальдикс)
Фармакокинетика.Препарат хорошо всасывается в желудочно-кишечном тракте, латентный период 1 ч, максимальная концентрация в крови определяется через 1,5 ч, длительность действия 12 ч. 60% препарата выводится с мочой в неизмененном виде.
Взаимодействие с другими ЛС.При одновременном применении снижает эффективность инсулина и других сахаросодержащих средств.
Индапамид(арифон)
Фармакодинамика.Не только оказывает слабое диуретическое действие, но и расширяет системные и почечные артерии. Обладает гипотензивным действием.
Снижение АД объясняется снижением концентрации натрия и уменьшением общего периферического сопротивления из-за снижения чувствительности сосудистой стенки к норадреналину и ангиотензину II, повышения синтеза про-стагландинов (Е,). При длительном применении у больных с умеренной артериальной гипертензией и нарушением функции почек индапамид ускоряет клу-бочковую фильтрацию. Индапамид используется главным образом как гипотензивное ЛС.
Индапамид дает пролонгированный гипотензивный эффект без значительного влияния на диурез. Латентный период 2 нед. Максимальное устойчивое действие препарата развивается через 4 нед.
Фармакокинетнка.Препарат хорошо всасывается в желудочно-кишечном тракте, максимальная концентрация в крови определяется через 2 ч. В крови на 75% связывается с белками, может обратимо связываться с эритроцитами. Т1/2 около 14 ч. 70% экскретируется через почки, остальное — через кишечник.
НЛРпри применении индапамида отмечаются у 5-10% больных. Возможны тошнота, диарея, кожная сыпь, слабость.
Артериальная гипертензия при сердечной недостаточности – что еще пить?
Диуретики при гипертонии и сердечной недостаточности от отеков при высоком давлении позволяют устранить симптомы, но не причину заболевания. Основную группу составляют:
- ингибиторы АПФ;
- бета-адреноблокаторы;
- блокаторы Са каналов;
- блокаторы рецепторов к ангиотензину-II;
- прямые ингибиторы ренина;
- вазодилататоры;
- лекарства, влияющие на адренергические рецепторы.
Учитывая риск развития хронической сердечной недостаточности (ХСН), инфаркта и инсульта на фоне гипертензии и ишемической болезни сердца, от начала терапии зависит продолжительность и качество современной жизни пациента-гипертоника. Комплексное лечение диуретиками гипертонической болезни включает прием одного или нескольких медикаментов для снижения АД и мочегонных для коррекции отеков. При аритмии в схему добавляют «Дигоксин», при гипертонии «Лизиноприл» или аналоги. Терапию проводят под контролем врача в лечебном учреждении для предотвращения негативных последствий.
Применение диуретиков при артериальной гипертензии: преимущества торасемида
В крупных международных исследованиях показана антигипертензивная эффективность диуретиков и их роль в предупреждении сердечно-сосудистых осложнений при долгосрочной терапии у пациентов с артериальной гипертензией. Дана характеристика механизмов действия различных диуретиков – петлевых, тиазидных/тиазидоподобных и калийсберегающих. Особое внимание уделено петлевым диуретикам. С 2006 г. в России появился петлевой диуретик торасемид (Диувер), который может назначаться для длительной терапии артериальной гипертензии. При использовании в субдиуретических дозах он обладает высокой антигипертензивной эффективностью и отсутствием значимого риска развития гипокалиемии, аритмий, влияния на уровни глюкозы, мочевой кислоты и липидный профиль.
Рис. 1. Экскреция электролитов с мочой в зависимости от дозы торасемида
Рис. 2. Гипотензивный эффект торасемида и гидрохлоротиазида в сочетании с триамтереном в течение суток после приема
Рис. 3. Влияние торасемида на уровень электролитов в сравнении с эффектом комбинации гидрохлоротиазида с триамтереном [19]
Рис. 4. Влияние торасемида в дозе 5 и 10 мг/сут на углеводный и липидный обмен при длительном (48 недель) применении
Рис. 5. Динамика выделения электролитов (натрия, хлора, калия и магния) при добавлении торасемида к гидрохлоротиазиду [21]
Рис. 6. Влияние торасемида на уровень альдостерона плазмы [24]
Рис. 7. Влияние торасемида на активность ренин-ангиотензивной системы [34]
Рис. 8. Плазменная концентрация торасемида разных форм высвобождения в течение суток (как должно быть)
Рис. 9. Профили средней концентрации в плазме крови торасемида разных форм высвобождения (как на самом деле)
Артериальная гипертензия (АГ) – один из основных факторов риска развития сердечно-сосудистых осложнений – встречается у 40% взрослого населения России, а среди лиц пожилого и старческого возраста ее распространенность превышает 50–60%. Согласно результатам многочисленных исследований, длительная терапия АГ позволяет значительно снизить риск сердечно-сосудистых осложнений. В связи с этим чрезвычайно актуальной представляется проблема выбора врачом эффективного препарата исходя из индивидуальных особенностей больного АГ.
В зарубежных и отечественных рекомендациях по лечению АГ в основной список антигипертензивных препаратов включены ингибиторы ангиотензинпревращающего фермента (иАПФ), антагонисты рецепторов ангиотензина II, антагонисты кальция, бета-адреноблокаторы и диуретики. К дополнительным относятся альфа-адреноблокаторы, агонисты имидазолиновых рецепторов и прямые ингибиторы ренина [1].
В зависимости от «места действия» в нефроне диуретики делят на петлевые (действующие преимущественно на восходящий отдел петли Генле), тиазидные и тиазидоподобные (действуют на начальную часть дистального канальца) и калийсберегающие (действуют на конечную часть дистального канальца). Следует отметить, что доказательная база по тиазидным диуретикам была получена главным образом на хлорталидоне, в то время как данных по гидрохлоротиазиду гораздо меньше.
Тиазидные диуретики
В течение ряда лет тиазидные диуретики оставались препаратами выбора у пожилых больных с изолированной систолической АГ. В последние годы рекомендации по терапии АГ были пересмотрены, о чем свидетельствуют изменившиеся подходы к лечению резистентной и неконтролируемой АГ, предполагающие обязательное применение диуретиков [1, 2]. Их способность снижать уровень систолического артериального давления (АД) и, что особенно важно, риск развития сердечно-сосудистых осложнений продемонстрирована в ряде крупномасштабных плацебоконтролируемых исследований, таких как SHEP (Systolic Hypertension in the Elderly Program – Систолическая гипертензия у пожилых) [3], STOP-Hypertension I–II [4], MRC (Medical Research Council trial of treatment of hypertension in older adults – Исследование лечения артериальной гипертензии у пожилых Совета по исследованиям в области медицины (Великобритания)) [5, 6], ALLHAT (Antihypertensive and Lipid Lowering treatment to prevent Heart Attack Trial – Исследование профилактики сердечных приступов с помощью антигипертензивной и гиполипидемической терапии) [7]. Так, в ходе исследования SHEP на фоне антигипертензивной терапии у пожилых пациентов с изолированной систолической АГ было показано снижение частоты развития инсультов на 36%, ишемической болезни сердца – на 27%, застойной сердечной недостаточности – на 49%, всех сердечно-сосудистых осложнений – на 32% [8].
В результате исследования ALLHAT доказана более высокая эффективность диуретиков (хлорталидон) в отношении снижения АД у больных с АГ и высоким риском сердечно-сосудистых осложнений по сравнению с блокаторами кальциевых каналов (БКК) (амлодипин) и иАПФ (лизиноприл). По первичной конечной точке (смерть от ишемической болезни сердца и нефатальные инфаркты миокарда) различий между тремя группами препаратов не выявлено, однако хлорталидон оказался эффективнее лизиноприла в плане снижения риска развития инсульта и эффективнее лизиноприла и амлодипина в отношении частоты развития хронической сердечной недостаточности (ХСН) [7].
При недостаточном эффекте диуретика не следует увеличивать дозу препарата, поскольку в этом случае его антигипертензивное действие не усиливается, но возрастает частота побочных эффектов. Так, не рекомендуется назначать гидрохлоротиазид в дозе более 12,5–25 мг, хлорталидон – более 12,5–25 мг и индапамид – более 1,25–2,5 мг – у пациента может развиться гипокалиемия с увеличением риска развития желудочковой экстрасистолии. С последней в свою очередь связывают повышение частоты внезапной смерти среди больных с АГ и наличием ЭКГ-признаков гипертрофии левого желудочка.
В целом при назначении диуретиков обязателен контроль уровня электролитов, глюкозы, липидов, мочевой кислоты у пациентов, так как эти препараты, особенно в высоких дозах, могут вызвать нарушения электролитного баланса в виде гипокалиемии и гипомагниемии, нарушения углеводного, липидного и пуринового обмена. Необходимо также помнить, что подагра является абсолютным, а гиперурикемия – относительным противопоказанием к назначению диуретиков.
Тиазидоподобные диуретики
Среди тиазидоподобных диуретиков особое место занимает индапамид, который иногда называют диуретиком без диуретического эффекта. Действительно, индапамид в дозе до 2,5 мг (Индапамид ретард – до 1,5 мг) не изменяет суточный объем мочи, действуя главным образом как периферический вазодилататор. В отличие от гидрохлоротиазида он оказывает небольшое влияние на уровень калия, глюкозы, общего холестерина и триглицеридов. Однако в новой инструкции к индапамиду указано, что пациентам с сахарным диабетом применять его следует с осторожностью. Это связано с проаритмогенным эффектом индапамида, который выражается в развитии опасных для жизни ари за счет удлинения интервала Q – T и объясняется его способностью тормозить активность калиевых каналов в мембранах кардиомиоцитов [9]. Поскольку функция мембранных калиевых каналов прежде всего нарушается у больных сахарным диабетом [10], применение индапамида может способствовать развитию у них желудочковых аритмий.
Потенциально аритмогенное действие индапамида может проявляться при его совместном применении с препаратами из других клинико-фармакологических групп, которые также могут удлинять интервал Q – T. Поэтому при лечении индапамидом необходимо следить не только за содержанием калия в крови, но и за изменениями интервала Q – T, что усложняет терапию и повышает ее стоимость.
Петлевые диуретики
Петлевые диуретики действуют на восходящий отдел петли Генле, где реабсорбируется 20–30% всего профильтрованного натрия, поэтому именно они оказывают более быстрое и мощное действие и применяются в экстренных ситуациях, например при отеке легких. При АГ до недавнего времени петлевые диуретики использовались лишь в особых ситуациях: при гипертонических кризах, тяжелой хронической почечной недостаточности (ХПН).
Однако после появления в России в 2006 г. препарата Диувер область применения торасемида расширилась: субдиуретические дозы Диувера (2,5–5 мг) стали назначать больным с АГ довольно часто.
Торасемид очень хорошо всасывается при пероральном приеме (максимальная концентрация в плазме достигается в течение 1–2 часов). Биодоступность препарата составляет 80–90%, что существенно выше, чем у фуросемида. Биодоступность торасемида не изменяется в зависимости от состояния пациента, в то время как у фуросемида отмечена ее значительная вариабельность. Особо стоит отметить, что биодоступность торасемида не зависит от приема пищи, а также у торасемида более продолжительный период полувыведения (3–4 часа) по сравнению с фуросемидом (1 час) [11].
При назначении торасемида в дозе 2,5–100 мг/сут объем выделенной жидкости, а также экскреция натрия и хлоридов возрастают линейно, в зависимости от дозы. Однако уникальность действия торасемида в том, что при увеличении его дозы экскреция калия практически не изменяется (рис. 1) [12]. В дозе 10 мг/сут торасемид вызывает такую же экскрецию натрия, как фуросемид в дозе 40 мг/сут, в значительно меньшей степени влияя на экскрецию калия [13]. Важно отметить, что торасемид в дозе 2,5–5 мг/сут не дает пикового диуретического эффекта, поэтому для него не характерно развитие так называемого эффекта рикошета (задержка натрия вслед за повышенной его экскрецией), обычно отмечаемого при использовании фуросемида.
При приеме 2,5–5 мг Диувера АД снижается постепенно, без клинически значимого увеличения диуреза. Это достигается за счет трех основных антигипертензивных механизмов: вазодилатации, в том числе вследствие блокады кальциевых каналов, снижения объема циркулирующей крови и натрийуреза. Максимальный антигипертензивный эффект достигается через 12 недель приема препарата и сохраняется длительно; число пациентов, ответивших на терапию, среди лиц с АГ I и II степени составляет от 60 до 90% [14].
Согласно данным 12-недельного двойного слепого исследования, у 147 больных с АГ по антигипертензивному действию торасемид в дозе 2,5–5 мг/сут достоверно превосходил плацебо [14]. Диастолическое АД нормализовалось у 46–50% больных, получавших торасемид, и у 28% больных из группы плацебо.
В исследовании P. Baumgart и соавт. [15] больным с АГ торасемид назначали в течение 48 недель, причем у одной половины пациентов лечение торасемидом начиналось с дозы 2,5 мг/сут, у другой – с 5 мг/сут. При недостаточной эффективности допускалось удвоение дозы. Существенных различий в эффективности торасемида в дозе 2,5 и 5 мг не отмечалось, и на этом основании был сделан вывод, что 2,5 мг/сут – оптимальная доза торасемида для лечения АГ. По данным суточного мониторирования АД, применение торасемида один раз в сутки обеспечивало сохранение сниженного уровня АД в течение 24 часов при поддержании нормального циркадного профиля АД (рис. 2) [16]. Антигипертензивный эффект при применении торасемида развивается постепенно, без резкого снижения АД. Это особенно важно для пожилых пациентов, у которых тиазидные и тиазидоподобные диуретики иногда вызывают ортостатическую гипотензию.
N. Spannbrucker и соавт. в рандомизированном двойном слепом многоцентровом исследовании [17] сравнили антигипертензивную эффективность торасемида (2,5 мг/сут) и индапамида (2,5 мг/сут) у больных с АГ и диастолическим АД 100–110 мм рт. ст. При недостаточном снижении АД через 4 недели допускалось удвоение дозы сравниваемых препаратов. К концу исследования у большинства пациентов в обеих группах отмечена нормализация АД. Серьезных побочных эффектов ни у больных, получавших торасемид, ни у пациентов, получавших индапамид, не отмечено, но в группе индапамида уровень калия в крови оказался на 0,4 ммоль/л ниже по сравнению с группой торасемида. Следует отметить также, что при увеличении дозы индапамида до 5 мг/сут регистрировалось статистически достоверное повышение в крови уровней мочевой кислоты и глюкозы, то есть в отличие от торасемида индапамид при увеличении дозы терял свою метаболическую нейтральность.
A. Reyes и соавт. [18] сравнили эффективность применения у пациентов с тяжелой АГ четырех мочегонных средств: индапамида, гидрохлоротиазида, циклотиазида и торасемида. Каждый из указанных препаратов был единственным антигипертензивным средством у больных в течение 8–12 недель. Торасемид и индапамид способстовали большему снижению уровня АД, чем гидрохлоротиазид и циклотиазид. При этом отмечено, что торасемид, в отличие от тиазидных диуретиков, не оказывал негативного влияния на уровень глюкозы в крови натощак.
Таким образом, торасемид в дозе 2,5–5 мг/сут по антигипертензивной активности не уступает гидрохлоротиазиду, хлорталидону и индапамиду.
Влияние торасемида на уровень электролитов было сопоставимо с эффектом комбинации гидрохлоротиазида с калийсберегающим диуретиком триамтереном (рис. 3) [19]. В этом же исследовании было изучено влияние разных доз торасемида на углеводный и липидный обмен при длительном (48 недель) применении; достоверных сдвигов уровня глюкозы, холестерина липопротеидов низкой и высокой плотности при использовании ни 5, ни 10 мг торасемида не обнаружено (рис. 4).
Поскольку при АГ почки являются одним из органов-мишеней, у больных нередко отмечается снижение скорости клубочковой фильтрации (СКФ), в том числе выраженное (
При ХПН, даже в случае снижения скорости клубочковой фильтрации
Как отмечено в результатах исследования TORIC (Tоrasemide In Congestive Heart Failure – Торасемид при застойной сердечной недостаточности) [20], при использовании торасемида в 10 раз реже требовалось применять препараты калия, чем при использовании других диуретиков.
Торасемид можно с успехом комбинировать с иАПФ, блокаторами ангиотензиновых рецепторов, БКК, бета-адреноблокаторами, то есть с любым из основных антигипертензивных препаратов. Более того, в исследовании H. Knauf [21] приведены интересные данные, свидетельствующие о возможности сочетания торасемида и гидрохлоротиазида: при усилении натрийуретического действия указанной комбинации отмечено уменьшение потерь калия и магния с мочой (рис. 5).
Следует подчеркнуть хорошую переносимость торасемида. При сравнении переносимости торасемида и гидрохлоротиазида в комбинации с триамтереном у больных с АГ через 4 недели терапии частота побочных эффектов в группе гидрохлоротиазида оказалась почти в 2,5 раза вышe.
Антиальдостероновое действие торасемида
Принципиальным отличием торасемида от других петлевых диуретиков является его антиальдостероновое действие [22]. При этом значительно снижается риск потери калия с характерным для многих других диуретиков развитием гипокалиемии, способной повысить риск развития тяжелых нарушений ритма и ухудшить прогноз [23]. По данным K. Harada и соавт., через 3 месяца после назначения торасемида у пациентов отмечено достоверное снижение уровня альдостерона в плазме (рис. 6) [24].
Уменьшение гипертрофии миокарда левого желудочка на фоне приема торасемида происходит, во-первых, за счет снижения АД, а во-вторых, за счет уменьшения выраженности фиброза миокарда. Антифибротический эффект торасемида [25] является уникальным свойством, которым не обладают ни индапамид, ни гидрохлоротиазид.
С антиальдостероновым эффектом скорее всего связана способность торасемида в значительной степени уменьшать выраженность гипертрофии и улучшать геометрию левого желудочка [26]. Как известно, коррекция гипертрофии левого желудочка у больных с АГ позволяет улучшить долгосрочный прогноз у этой категории лиц.
В настоящее время установлено, что АГ гораздо чаще, чем считалось ранее, сопутствует идиопатический гиперальдостеронизм, даже в отсутствие аденомы надпочечников (синдрома Конна), который в свою очередь способствует повышению уровня АД.
Согласно материалам крупного исследования PAPY (Primary Aldosteronism Prevalence in Italy Study – Распространенность первичного гиперальдостеронизма в Италии) [27], распространенность у больных с АГ идиопатического гиперальдостеронизма составила 6,4% при частоте первичного альдостеронизма в популяции 4,8%. По данным B. Strauch и соавт. [28], распространенность гиперальдостеронизма достигала 25% у пациентов с АД выше 160/100 мм рт. ст. Таким образом, очевидно, что высокое АД способствует развитию гиперальдостеронизма [29].
По данным E. Born-Frontsberg и соавт. [30], при гиперальдостеронизме у больных с АГ чаще обнаруживается и бывает более выраженным поражение органов-мишеней, чаще выявляются сердечно-сосудистые заболевания. Неконтролируемая АГ нередко бывает связана с гиперпродукцией альдостерона, в этом случае включение спиронолактона в схемы комбинированной антигипертензивной терапии позволяет добиться достоверного снижения АД. Не случайно спиронолактон был одним из дополнительных антигипертензивных препаратов в исследовании ASCOT-BPLA (Anglo-Scandinavian Cardiac Outcomes Trial – Blood Pressure Lowering Arm, Англо-скандинавское исследование кардиальных исходов – Группа антигипертензивной терапии) [31]. В ряде случаев (у больных с ХПН и гиперкалиемией, у мужчин с гинекомастией в ответ на применение спиронолактона) альтернативным препаратом может быть торасемид.
Интересно, что комбинация торасемида с эналаприлом по сравнению с комбинацией гидрохлоротиазида с эналаприлом в большей степени улучшала диастолическую функцию левого желудочка, что, по мнению авторов [13], может быть связано с антиальдостероновым действием торасемида. Кроме того, есть основания полагать, что благодаря своему антиальдостероновому действию торасемид ингибирует синтез и, напротив, стимулирует деградацию в миокарде коллагена I типа, как известно способствующего повышению жесткости миокарда. В итоге торасемид уменьшает фиброз миокарда почти на 22% [25], что ведет к снижению частоты аритмий [32].
Показано, что альдостерон за счет блокады эндотелиальной NO-синтазы и соответственно уменьшения образования оксида азота нарушает функцию эндотелия [33]. Поэтому при назначении торасемида, оказывающего антиальдостероновое действие, можно рассчитывать на улучшение функции эндотелия.
Важно отметить, что торасемид, применяемый для снижения АД в дозе 2,5–5 мг/сут, не повышает активности ренин-ангиотензивной системы, что является его несомненным преимуществом по сравнению с другими диуретиками, такими как индапамид и гидрохлоротиазид. Увеличение концентрации ренина плазмы и альдостерона отмечено при увеличении дозы торасемида до 10 мг/сут (рис. 7) [34]. Это говорит о том, что торасемид блокирует рецепторы к альдостерону в органах-мишенях, что позволяет прерывать цепь патологических реакций, запускаемых альдостероном. Блокада рецепторов альдостерона значимо выделяет торасемид среди других диуретиков и обеспечивает его эффективность, уникальные антифибротические свойства, высочайшую метаболическую нейтральность и безопасность.
Полагают, что антигипертензивное действие торасемида во многом связано с ингибированием вазоконстрикторного действия тромбоксана А2 и увеличением высвобождения простациклина в сосудистой стенке, что выгодно отличает торасемид от фуросемида [35]. Кроме того, в этом процессе особую роль играет уменьшение содержания внутриклеточного кальция, как правило повышенного при АГ [36].
И.М. Кутырина и соавт. [37] отметили, что с ростом индекса массы тела значительно увеличивается уровень альдостерона в плазме крови. Так, при индексе массы тела от 30 до 39,9 кг/м2 уровень альдостерона был в 2,5 раза выше, чем при индексе массы тела от 25 до 29,9 кг/м2.
Таким образом, механизмы антигипертензивного действия торасемида многообразны:
- блокада продукции альдостерона;
- уменьшение активности ренин-ангиотензивной системы;
- ингибирование образования тромбоксана А2;
- натрийуретическое действие (уменьшение объема циркулирующей крови);
- уменьшение концентрации внутриклеточного кальция (вазодилатация);
- повышение высвобождения простациклина сосудистой стенкой (дополнительное сосудорасширяющее действие).
При использовании торасемида не происходит рост плазменной концентрации самого агрессивного проаритмогенного медиатора – норадреналина, что выгодно отличает его от других диуретиков [38].
Антагонисты альдостерона (спиронолактон) показаны при гиперальдостеронизме и при сочетании АГ с ХСН. Как правило, избыточная секреция альдостерона сопровождается гипокалиемией, что является основным фактором при скрининге больных на первичный гиперальдостеронизм.
Торасемид разных форм высвобождения
Для практикующего врача интерес представляет сравнение действия торасемида разных форм высвобождения – обычной (немедленное высвобождение) и пролонгированной (постепенное высвобождение). По данным Института маркетинговых исследований ГфК-Русь за 2013 г., в России 9 из 10 кардиологов рекомендуют Диувер (фармацевтическая ) – торасемид с немедленным высвобождением, который выпускается в таблетках по 5 и 10 мг. В соответствии с Национальным руководством по клинической фармакологии [39] препараты с пролонгированными формами высвобождения действующего вещества должны обладать следующими свойствами:
- создавать постоянную плазменную концентрацию действующего вещества (> 75% максимальной концентрации) в течение длительного времени (так называемое плато);
- «плато» должно находиться в пределах «терапевтического коридора» (в диапазоне между минимальной терапевтической и минимальной токсической дозами);
- «плато» должно быть более продолжительным, чем время действия препарата с обычным высвобождением (рис. 8).
Как показано на рис. 9 [40], у обеих форм торасемида концентрация активного вещества в крови уже через 6 часов одинакова, что фактически говорит об отсутствии пролонгации высвобождения действующего вещества. Об этом свидетельствует и отсутствие «плато» – необходимого атрибута препаратов пролонгированного действия, площадь под фармакокинетической кривой у обоих препаратов одинакова.
Объем мочи, количество натрия, хлора и калия, выделенных за сутки с мочой, не различались у пациентов, принимавших препараты торасемида с разными формами высвобождения [40, 41]. По некоторым данным, в первый час после приема препарата с немедленным высвобождением объем выделенной мочи больше, чем после приема препарата пролонгированного действия. В работе M.J. Barbanoj и соавт. [40] отмечено, что разница в объеме мочи в первый час после приема препаратов составила 123,27 мл (578,27 мл против 455 мл). Учитывая, что импульсы в мозг от мочевого пузыря формируются при его наполнении более 150 мл, логично предположить, что этот объем не будет существенно влиять на количество позывов к мочеиспусканию. Данное предположение подтверждено в проведенном сравнительном исследовании. Так, при регулярном применении торасемида количество неотложных позывов к мочеиспусканию у препаратов с разными формами высвобождения было сопоставимо. После применения пролонгированной формы отмечались эпизоды неотложного позыва к мочеиспусканию в среднем через 1,37 и 3,03 часа, а после применения обычного торасемида – через 1,12 и 3,03 часа. При этом средние субъективные оценки интенсивности позывов по визуальной аналоговой шкале были практически идентичны: 81,25 и 74,06 у пациентов, принимавших препарат пролонгированного действия, и 83,87 и 77,2 – у принимавших торасемид обычной формы высвобождения. Исходя из сказанного, ни интенсивность позывов к мочеиспусканию, ни частота мочеиспусканий не различались в группах торасемида с разными формами высвобождения.
S. Gropper и соавт. [42, 43] установили, что при назначении торасемида пролонгированного высвобождения в дозе 5 мг у больных отмечается больше неотложных мочеиспусканий, чем после приема обычного торасемида в той же дозе. Поскольку доза 5 мг рекомендована для лечения АГ, то предпочтительным является применение обычного торасемида. На фоне приеме 10 мг торасемида немедленного высвобождения количество мочеиспусканий у больных больше, чем после приема 10 мг торасемида пролонгированного действия. Учитывая, что торасемид в дозе 10 мг чаще используется при лечении отеков у пациентов с ХСН, управляемый и прогнозируемый диурез обусловливает целесообразность применения обычной формы данного препарата.
Торасемид обычной формы и пролонгированного действия по-разному влияют на фиброз миокарда. Снижение фиброза миокарда подтверждено в исследовании B. Lоpez [25] для торасемида быстрого высвобождения, но не для его пролонгированной формы (исследование TORAFIC) [44]. Так, судя по концентрации карбокситерминального пропептида коллагена I типа в сыворотке крови, в исследовании TORAFIC долгосрочное лечение лекарственной формой торасемида с контролируемым высвобождением не оказало достоверного влияния на фиброз миокарда. Тем самым доказанная способность торасемида (Диувера) снижать количество желудочковых экстрасистол не может быть экстраполирована на торасемид с контролируемым высвобождением.
Неспособность торасемида с пролонгированным высвобождением уменьшать фиброз миокарда, возможно, связана с более низкой пиковой концентрацией действующего вещества по сравнению торасемидом немедленного высвобождения. Данной концентрации может оказаться недостаточно для запуска каскада механизмов по снижению синтеза и увеличению распада коллагена.
Основные показания к применению Диувера: отечный синдром различного генеза, в том числе при ХСН, заболеваниях печени, легких и почек, а также АГ. Очевидно, что Диувер с учетом его метаболической нейтральности, антиальдостероновой активности, отсутствию влияния на электролитный баланс, положительному воздействию на состояние органов-мишеней, включая способность уменьшать фиброз миокарда, а также очень хорошей переносимости следует более широко применять для лечения больных с АГ.
Выводы
На основании изложенного можно сделать следующие выводы.
1. Торасемид рекомендован для комбинирования со всеми классами антигипертензивных препаратов.
2. Торасемид дает такой же антигипертензивный эффект, как индапамид и гидрохлоротиазид, но при этом превосходит их по безопасности, то есть не оказывает существенного влияния на уровень электролитов, глюкозы, липидов и мочевой кислоты в крови и т.д.
3. Торасемид можно использовать даже у больных со сниженной функцией почек, когда индапамид и гидрохлоротиазид неэффективны.
4. Торасемид обладает тройным антигипертензивным механизмом действия: вазодилатация, снижение объема циркулирующей крови и натрийурез.
5. Торасемид обладает важнейшим дополнительным свойством – антиальдостероновым эффектом.
6. При приеме торасемида больные в 10 раз реже нуждаются в коррекции электролитных нарушений по сравнению с другими диуретиками.
7. В отличие от индапамида торасемид не влияет на интервал Q – T, что позволяет безопасно использовать его у всех категорий пациентов; это особенно важно, если у больных нет возможности регулярно проверять интервал Q – T.
8. Торасемид не активирует симпатическую нервную систему, что выгодно отличает его от других диуретиков.
9. Торасемид снижает фиброз миокарда и улучшает его геометрию, что может не только замедлять прогрессирование заболевания, но и снижать риск нарушений ритма, а также улучшать прогноз пациентов.
10. Торасемид с немедленным высвобождением (в частности Диувер) способствует снижению фиброза миокарда в отличие от торасемида пролонгированного действия.