Причины развития патологии. Симптоматика Возможные осложнения при лимфангиоме Диагностика патологии и способы лечения
Лимфангиома
или лимфатическая мальформация — научное определение патологии, является доброкачественной опухолью, образовавшейся в сплетениях лимфатических сосудов соединительной ткани. В настоящее время истинные причины возникновения новообразования не установлены. Среди медиков бытует мнение, что
лимфангиома
является настоящей доброкачественной опухолью, развивающейся в организме благодаря создавшимся условиям. С другой стороны, существует мнение, что патология является врожденным порок развития лимфатической системы. Новообразование представляет собой кисты различной величины. Наиболее распространенным проявлением развития опухоли, являются узлы диаметром 0,2-0,3 см. Однако в медицинской практике имеются случаи наличия крупных образований в результате мальформации лимфатической системы, обнаруживающиеся при визуальном осмотре. Доброкачественная опухоль чаще всего развивается в детском возрасте. В ряде случаев патология является врожденной формой заболевания.
В соответствии с данными МОЗ, лимфангиома
встречается достаточно часто. Каждый десятый случай из общей картины развития опухолей у детей, связан с доброкачественным новообразованием в лимфатической системе. Существует четкое разделение на первичные опухоли и вторичные новообразования. Вторичная форма новообразования опухоли наблюдается в результате перенесенных ребенком инфекционных заболеваний и возникших в связи с этим осложнений.
Причины развития патологии. Симптоматика
Ранее уже говорилось, что в настоящее время не имеется четких представлений о причинах развития доброкачественного новообразования лимфатической системы. В результате обследования пациентов было установлено, что лимфангиома
чаще всего становится результатом развития врожденного порока лимфатической системы. В ряде случаев патология формируется во время внутриутробного периода и начинает интенсивно развиваться сразу после рождения ребенка. Нередко доброкачественная опухоль лимфатической системы развивается на фоне других отклонений организма. На врожденный характер патологии в соответствии с последними научными разработками и догадками ученых медиков, могут оказывать влияние плохая экологическая обстановка для будущей матери, включая воздействие гамма излучения. Другими косвенными факторами, оказывающими влияние на формирование патологии, могут быть плохая наследственность и осложнения, в результате перенесенных будущей матерью тяжелых системных и инфекционных заболеваний.
Симптоматика патологии имеет ярко выраженный характер. С развитием опухоли в раннем возрасте у ребенка наблюдается появление уплотнений в области шеи, в ротовой полости, несколько реже во внутренних органах и в брюшине. Встречаются случаи развития узелков и в других частях тела пациента. Локализация новообразования происходит в подкожной жировой клетчатке. В зависимости от симптоматики различают следующие виды патологии:
- капиллярная лимфангиома
; - кавернозная лимфангиома
; - кистозная лимфангиома
.
К капиллярным или простым патологиям относятся новообразования, местом локализации которых чаще всего становятся ротовая полость, язык, внутренняя поверхность щек ребенка. С клинической точки зрения, новообразования в данном случае выглядят как припухлости размером 203 см, мягкие на ощупь и с неизменной окраской. Болевые ощущения при ощупывании новообразований отсутствуют. При детальном анализе можно обнаружить структуру уплотнений, состоящих из сети капилляров, большого количества лимфоидных клеток и соединительной ткани.
Второй вид патологии, кавернозная лимфангиома
проявляется в виде пузырьков на поверхности кожи, размер которых составляет 2-5 см. Пузырьки, как правило, возникают в мягких подкожных тканях в областях наибольшего сплетения лимфатической системы, шее, области грудной клетки, на боковой поверхности туловища, на руках и ногах. Гораздо чаще в медицинской практике встречается третий вид патологии, кистозные лимфангиомы. Новообразования развиваются в месте сплетения лимфатических узлов. Крупные по размеру, сферические образования могут возникать в подчелюстной области, области подмышек или в районе расположения ушных раковин. В отличие от предыдущих двух видов патологии, кистозная
лимфангиома
отличается стремительным ростом, который обусловлен быстрым заполнением полостей кисты жидкостью. В результате прорыва кисты не редко возникают абсцессы и инфицирование организма.
Отличительная особенность первых двух типов заболевания заключается в возможности самостоятельной остановке роста опухоли. Нередко наблюдается регресс в развитии опухоли, заканчивающийся рубцеванием. Обнаруженная лимфангиома
в детском возрасте имеет достаточно медленное развитие, процесс которого ускоряется в период полового созревания организма. Причины, объясняющиеся подобную динамику, до конца не изучены. Существует мнение медиков, что активизация роста опухоли с началом период полового созревания, связано с воздействием формирующееся секреторной системы организма на состояние лимфатической системой.
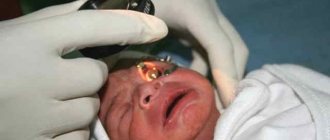
Ограниченная лимфангиома у больного онкологического профиля
Ограниченная (капиллярная) лимфангиома (lymphangioma circumscriptum) — это врожденная или приобретенная аномалия поверхностных лимфатических сосудов, представляющая собой сгруппированные папулы, на вершине которых расположены везикулы, которые содержат прозрачную лимфатическую жидкость, но могут стать геморрагическими, внешне напоминающими «икру лягушки» [1].
Wegener в 1877 г. впервые разделил лимфангиомы на простые, кавернозные и пузырные [2]. Капиллярная лимфангиома относится к категории простых, термин «сutaneous lymphangioma circumscriptum» (CLC) предложен M. Morris в 1889 г. [3]. Спустя почти век Peachey и Lever в 1970 г. на основании гистопатологических признаков и клинической картины описали классическую и локализованную формы дерматоза [4].
CLC составляет 4,0% от всех опухолей кожи и до 25,0% от всех доброкачественных сосудистых новообразований у детей. Дебют заболевания обычно наблюдается в детстве, причем до 90,0% случаев возникает в период до 2 лет [5]. Однако описана манифестация CLC и у взрослых. Ретроспективное исследование, проведенное в госпитале университета Ага Хана (Карачи, Пакистан — Aga Khan University, Karachi, Pakistan), показало, что за период с 2002 г. по 2012 г. средний возраст пациентов с CLC составил 27 лет [6]. Гендерных различий не описано, однако среди детей раннего возраста болеют чаще девочки [7]. Заболеваемость в США составляет 1,2–2,8 на 1000 новорожденных [8]. Данные по заболеваемости в России в литературе не встречаются. Роль наследственности не установлена [9].
Патогенетически CLC является типичной гамартомой. Патогенез дерматоза описан Whimster в 1976 г. Автор отметил, что в ходе онтогенеза аномальные лимфатические цистерны растут отдельно от нормально функционирующих в толще гиподермы и связаны лишь с поверхностным лимфатическим руслом. Сокращения гладкой мускулатуры сбрасывают лимфу из цистерн в поверхностные лимфатические сосуды, которые вследствие высокого давления расширяются и выпячиваются в эпидермис [10]. Примечательно, что видимый клинический кожный процесс не соответствует количеству аномальных цистерн, создавая эффект «айсберга» [11]. Важно отметить, что отсутствие кожной лимфедемы свидетельствует о наличии дренажа лимфы через нормально функционирующие сосуды [5].
Гистологически определяются скопления пузырных лимфатических пространств, занимающие всю толщу дермы. Характерны акантоз и папилломатоз, морфологические различия поверхностных и глубоких лимфатических сосудов. Так, эндотелиоциты верхнего русла имеют большую электронную плотность, уплощены (до 0,1–0,3 мкм), их ядра содержат плотно упакованный хроматин, а базальная мембрана имеет разное количество слоев на различных участках. В свою очередь эндотелиоциты глубокого русла менее плоские (до 0,6–2,5 мкм), базальная мембрана непрерывна на всем протяжении, определяются пиноцитозные вакуоли, формирующиеся путем инвагинации клеточной мембраны. Сравнение морфологии позволяет предположить, что сосуды поверхностного лимфатического русла подверглись патологическим изменениям в результате потери транспортной функции, в то время как сосуды глубокого русла морфологически не изменены [12].
Кожные проявления CLC представлены сгруппированными полупрозрачными везикулами с серозно-геморрагическим содержимым, напоминающими «лягушачью икру» [13]. Однако наравне с везикулами могут наблюдаться буллезные элементы. Травматизация элементов приводит к кровотечению и лимфорее. Иногда высыпания могут претерпевать изменения по типу гиперкератоза или веррукозных разрастаний. Так, L. C. Horn в 2005 г. описал случай гигантской CLC у 22-летней женщины, внешне напоминающей гигантскую кондилому Бушке–Левенштайна [14, 15]. Чаще всего высыпания локализованы на проксимальных участках конечностей, туловище, подмышечной области, а также на слизистой рта, особенно на языке. Также описаны высыпания на половом члене, вульве, мошонке [16, 17]. Дерматоскопическая картина представлена напоминающими гипопион лакунами от светло-коричневого до фиолетового цвета, окруженными светлыми септами. Некоторые авторы сравнивают такие находки с «гроздьями винограда». Напоминающие гипопион лакуны отражают оседание крови в тканевой жидкости [18].
Классическая форма CLC поражает преимущественно верхние конечности, верхнюю часть спины, подмышечную область, грудь. Для данной формы не характерна веррукозная и гиперкератотическая трансформация, размеры ее превышают 1 см2, характерна манифестация в раннем возрасте. Локализованная форма в свою очередь обычно менее 1 см2, возникает в любом возрасте и на любом участке тела. Описаны две формы у одного пациента в виде overlap-синдрома [4]. Возможны ассоциации CLC с синдромами Cobb, Proteus, Maffucci [19–21]. Д. В. Елькини и др. описывают вторичные лимфангиомы, развивающиеся в зоне постмастэктомической лимфедемы, возникшие в результате хирургического и/или лучевого вмешательства, что наблюдалось и в нашем случае [22].
Дифференциальный диагноз проводится с контагиозным моллюском, гемангиомой, ангиокератомой. Кроме того, важным является исключение кожных метастазов злокачественных новообразований (carcinoma teleangiectoides), визуальные проявления которых почти идентичны CLC. Однако в случае неоплазий основными морфологическими элементами являются узелки — часто безболезненные, круглые или овальные, плотные, подвижные, эластические на ощупь, от физиологической окраски до коричневого, черно-синего и даже красного цветов, расположенные, как правило, рядом с первичной опухолью [23].
Целью лечения CLC является устранение болевых ощущений, дренаж дилатированных лимфатических и кровеносных сосудов, а также лечение вторичной инфекции в случае ее присоединения [24]. Важно объяснить пациенту, что существующие методики лечения CLC не исключают развитие рецидива дерматоза. Наибольшей эффективностью обладает хирургическое лечение, результативность которого по данным литературы достигает 75,0%, в случае повторного иссечения увеличивается на 12,0% [9]. Разрез при CLC требуется глубокий, доходящей иногда до мышечной фасции, что обусловлено необходимостью иссечь глубоко залегающие аномальные лимфатические цистерны. Для определения максимально точных границ разреза высокой эффективностью обладают методы визуализации, в частности магнитно-резонансная томография (МРТ). Авторы отмечают, что, определяя адекватный объем хирургического вмешательства, использование МРТ снижает шанс рецидива дерматоза [10]. Положительные результаты описаны при применении карбонового лазера мощностью 5 Вт в непрерывном режиме. Электрокаутеризация, как и криотерапия, применяется в случае поверхностного расположения CLC. Используется склеротерапия с помощью натрия тетрадецилсульфата 0,25–0,5% и полидоканола 0,5%, однако препараты не одобрены Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов США (Food and Drug Administration, FDA) для лечения CLC. Лучевая терапия не применяется, так как существует риск малигнизации. Так, в литературе описаны случаи трансформации лимфангиомы в опухоль Дабски (эндоваскулярная папиллярная ангиоэндотелиома) и лимфангиосаркому [25, 26].
При инфицировании опухоли в качестве антибактериальной терапии используют цефалексин 500 мг 2–4 раза в день в течение 10 дней или же доксициклин 100 мг 2 раза в день в течение 10 дней при обнаружении метициллинрезистентного золотистого стафилококка (англ. Methicillin-resistant Staphylococcus aureus, MRSA) в отделяемом элементов [27].
Приводим наблюдение клинического случая.
Клинический случай
Женщина, 54 года, обратилась в кожно-венерологический диспансер с жалобами на пузырьковые высыпания на коже передней поверхности грудной клетки, правом плече, без субъективных ощущений. Из анамнеза известно, что считает себя больной в течение двух лет, когда впервые стали появляться пузырьки в области подмышечной впадины справа. Периодически отмечала появление аналогичных элементов на коже груди, плече. При травматизации пузырьков наблюдалось выделение желтоватой жидкости. Самостоятельно смазывала раствором борной кислоты, спиртом, хлоргексидином — без эффекта. В анамнезе радикальная левосторонняя мастэктомия по поводу рака левой молочной железы Т1сN0M0 в 1999 г., лимфостаз справа. Правосторонняя мастэктомия в 2015 г. по поводу рака правой молочной железы Т1N0M0.
Status specialis: высыпания асимметричные, расположены на передней поверхности грудной клетки в маммарных областях, медиальной поверхности левого плеча. Представлены милиарными и лентикулярными папулами коричневого и фиолетового цветов, на вершине которых расположены мелкие (до 0,2 см в диаметре) везикулы с серозным содержимым, возвышающимися над окружающей кожей по типу «лягушачьей икры». Дерматоскопически определяются лакуны, заполненные содержимым оранжевого и фиолетового цветов, разделенные белыми перегородками.
На основании клинического обследования, дерматоскопической картины установлен диагноз ограниченной лимфангиомы кожи груди, правого плеча. Рекомендовано профилактировать травматизацию элементов, использовать растворы антисептиков, анилиновых красителей, антибактериальные пластыри.
Описанный случай представлен в связи с редкостью данного дерматоза.
Литература
- William J., Timothy B., Dirk E. Andrews’ Diseases of the Skin // Clinical Dermatology. 2005, p. 585.
- Bauer B. S., Kernahan D. A., Hugo N. E. Lymphangioma circumscriptum – a clinicopathological review // Annals of Plastic Surgery. 1981. Vol. 7. P. 318–326.
- Morris M. Lymphangioma circumscriptum // International Atlas of Rare Skin Diseases. London: Lewis. 1889. P. 1–4.
- Peachey R. D., Lim C. C., Whimster I. W. Lymphangioma of skin. A review of 65 cases // British Journal of Dermatology. 1970. Vol. 83. P. 519–527.
- Fernandez G. Lymphangioma // eMedicine Dermatology. 2007. URL https:// www.emedicine.com/DERM/topic866.htm (Accessed 26 Nov 2019).
- Fatima S., Uddin N., Idrees R. Lymphangioma Circumscriptum: Clinicopathological Spectrum of 29 Cases // Journal of College of Physicians and Surgeons Pakistan. 2015. Vol. 25. № 9. P. 658–61.
- Schwartz R. A. Arterial vascular malformations including hemangomias and lymphangiomas // eMedicine Pediatrics. 2009. URL https://emedicine.com/ped/topic2926.html (Accessed 26 Nov 2019).
- Filston H. C. Hemangiomas, cystic hygromas, and teratomas of the head and neck // Seminars in Pediatric Surgery. 1994. Vol. 3. P. 147–159.
- Flanagan B. P., Helwig E. B. Cutaneous lymphangioma // Archives of Dermatology. 1977. Vol. 113. P. 24–30.
- Whimster I. W. The pathology of lymphangioma circumscriptum // British Journal of Dermatology. 1976. Vol. 94. P. 473–486.
- Martínez-Menchón T., Mahiques-Santos L., Febrer-Bosch I. Lymphangioma Circumscriptum: An Example of Whimster’s Hypothesis // Pediatric Dermatology. 2004. Vol. 21. № 6. P. 652–654.
- Asano S., Endo H., Sagami S. An ultrastructural study of localized lymphangioma circumscriptum // Archives of Dermatological Research. 1978. Vol. 262. P. 301–309.
- Mordehai J., Kurzbart E., Shinhar D. Lymphangioma circumscriptum // Pediatric Surgery International. 1998. Vol. 13. P. 208–210.
- Erkilic S., Kocer N. E., Mutaf M. Giant lymphangioma circumscriptum mimicking wart in a 13-year-old girl // The Journal of Dermatology. 2006. Vol. 33. P. 501–503.
- Horn L. C., Kuhndel K., Pawlowitsch T. Acquired lymphangioma circumscriptum of the vulva mimicking genital warts // European Journal of Obstetrics & Gynecology and Reproductive Biolog. 2005. Vol. 123. P. 118–120.
- Yagmurlu A. et al. A children’s disease of rarity: «scrotal lymphangioma circumscriptum» // International Urology and Nephrology. 2004. Vol. 36. P. 229–233.
- Yildiz F., Atahan I. L., Ozyar E. Radiotherapy in congenital vulvar lymphangioma circumscriptum // The International Journal of Gynecological Cancer. 2008. Vol. 18. P. 556–559.
- Mabel D. A. Gomides, Laís D. Costa. Cutaneous lymphangioma circumscriptum: The relevance of clinical, dermoscopic, radiological, and histological assessments // Clinical Case Reports. 2022. Vol. 7. № 4. P. 612–615.
- Child F. J., Werring D. J., Vivier A. W. Proteus syndrome: diagnosis in adulthood // British Journal of Dermatology. 1998. Vol. 139. P. 132–136.
- Shim J. H., Lee D. W., Cho B. K. A case of Cobb syndrome associated with lymphangioma circumscriptum // Dermatology. 1996. Vol. 193. P. 45–47.
- Елькин В. Д., Митрюковский Л. С., Седова Т. Г. Избранная дерматология. Редкие дерматозы и дерматологические синдромы. Ил. справ. по диагностике и лечению дерматозов. Изд. второе, испр. и доп. Пермь: ИПК Звезда, 2004. 943 с.
- Van Vonno N. A case of carcinoma telangiectaticum // The British Journal of Dermatology and Syphilis. 1933. Vol. 45. P. 423–424.
- Bond J., Basheer M. H., Gordon D. Lymphangioma circumscriptum: pitfalls and problems in definitive management // Dermatologic Surgery. 2008. Vol. 34. P. 271–275.
- Emanuel P. O., Lin R., Silver L. Dabska tumor arising in lymphangioma circumscriptum // Journal of Cutaneous Pathology. 2008. Vol. 35. P. 65–69.
- King D. T., Duffy D. M., Hirose F. M. Lymphangiosarcoma arising from lymphangioma circumscriptum // Archives of Dermatology. 1979. Vol. 115. P. 969–972.
- Bryan A., Galen F. Lymphangioma Circumscriptum (Lymphangiectasia, Dermal Lymphangioma) // Dermatology Advisor. 2017. URL https://www.dermatologyadvisor.com/home/decision-support-in-medicine/dermatology/lymphangioma-circumscriptum-lymphangiectasia-dermal-lymphangioma/ (Accessed 27 Nov 2019).
М. А. Уфимцева1, доктор медицинских наук Ю. М. Бочкарев, кандидат медицинских наук А. А. Комаров А. С. Шубина
ФГБОУ ВО УГМУ Минздрава России, Екатеринбург
1 Контактная информация
DOI: 10.26295/OS.2020.35.92.006
Ограниченная лимфангиома у больного онкологического профиля/ М. А. Уфимцева, Ю. М. Бочкарев, А. А. Комаров, А. С. Шубина Для цитирования: Лечащий врач № 5/2020; Номера страниц в выпуске: 33-35 Теги: кожа, лимфатические сосуды, злокачественные новообразования
Возможные осложнения при лимфангиоме
Несмотря на доброкачественную природу, лимфангиома
представляет серьезную опасность для организма. Основная опасность обусловлена угрозой организму в процессе деторождения, как для матери, так и для будущего ребенка. Патология представляет опасность не только для новорожденных, но и для детей подросткового возраста, нанося серьезный вред состоянию здоровья. Новообразования, возникшие в плоде, создают трудности для роженицы во время прохождения плода родовыми путями. Нередко происходит сдавливание соседних органов, смещение тканей, вызывая у новорожденного врожденную гипоксию и ишемическую болезнь сердца, других органов.
Проявившаяся после рождения у новорожденного лимфангиома
, дает все основания подозревать на наличие у ребенка серьезных нарушений функциональности жизненно-важных органов. Со временем может наступить полная утрата функциональности отдельных органов. Исходя из того, что порок в процессе рождения затрагивает органы в области головы и шеи, у новорожденного могут возникнуть проблемы с дыхательным процессом, затруднить процесс глотания.
Самое распространенное осложнение, возникающее в результате развивающейся патологии, является лимфатическая мальформация, образовавшаяся в результате любого воспалительного процесса. Осложнения могут возникнуть в результате возникшего отита, ОРВИ, заболеваний дыхательных органов, лимфаденита. К разряду тяжелых осложнений, вероятность которых вырастает в результате развития доброкачественной опухоли в лимфатической системе, является истечение лимфы в область грудной клетки и брюшины, создающее угрозу для жизни пациента.
Причины
Причины образования лимфангиом у детей в настоящее время научно не доказаны. Предполагают, что основным этиологическим фактором врожденной патологии является внутриутробный порок развития кровеносных и лимфатических сосудов. Неправильное развитие сосудистой ткани, скопление жидкости в лимфатических сосудах приводит к их расширению и превращению в полости. Подтверждают теорию о нарушении эмбриогенеза следующие факты: врожденный характер опухоли, ее сочетание с другими внутриутробными пороками и аномалиями плода.
Другие ученые считают, что лимфангиома – истинная опухоль. Это мнение обусловлено пролиферацией опухолевых клеток и наличием в неоплазии факторов роста. Этот путь образования опухолей наиболее характерен для взрослых пациентов.
Причины вторичных лимфангиом:
- Инфекционные болезни,
- Оперативные вмешательства,
- Лучевая терапия,
- Другие опухоли.
Преимущества лечения с ServiceMed
- Отличные возможности для ранней диагностики
- Приоритет щадящих хирургических техник лечения
- Активное применение инновационных фармацевтических препаратов
- Обоснованная цена операции по удалению лимфангиомы почки в Израиле
ServiceMed – это уникальная возможность избавиться от опасного заболевания почек!
План лечения и цены получите бесплатно, заполнив форму Специалисты по направлению
- БиографияОнлайн- консультация
Др. Нейман Виктория Онкология. Лучевая терапия. Рак груди. Рак мочевой системы. Рак кожи (меланома) - БиографияОнлайн- консультация
Проф. Адерка Дан Онкология. Терапия. Гастроэнтерология
- БиографияОнлайн- консультация
Проф. Бренер Барух Онкология. Терапия. Гастроэнтерология
Диагностика лимфангиомы в Израиле
Для пациентов, приезжающих на лечение в Израиль, длительность его имеет очень большое значение, ведь каждый день пребывания в чужой стране стоит денег. Специалисты Топ Ихилов знают об этом, поэтому процесс диагностики здесь четко скоординирован и не занимает более трех дней.
- День 1
- День 2
- День 3
1 день: консультация ведущего хирурга
Ваш личный помощник назначит для вас консультацию врача заранее, поэтому вам не нужно будет тратить время на поиск нужного специалиста и ожидание в очередях. На первом посещение врача вы пройдете физический осмотр. Кроме этого, доктор задаст вам необходимые вопросы и изучит медицинские документы. Затем он составит план последующих диагностических мероприятий.
2 день: диагностические процедуры
Диагностика лимфангиомы в Израиле может включать в себя следующие тесты:
- Ультразвуковое обследование. Это информативный и недорогой метод диагностики лимфангиомы.
- Ангиографическое исследование. Позволяет точно определить, какие кровеносные сосуды вовлечены в патологический процесс.
- Биопсия. Взятие небольшого участка опухоли для гистологического анализа. Помогает отличить лимфангиому от других схожих по клиническим проявлениям новообразований.
- Компьютерная и магнитно-резонансная томография. Эти исследования обычно проводятся в рамках предоперационного планирования. Высокая различительная способность МРТ помогает четко разграничить патологические и здоровые ткани и избежать неполной или излишней резекции.
- Общий и генетический анализы крови.
3 день: врачебный консилиум
После того, как результаты диагностических исследований будут готовы, ваш лечащий врач соберет консилиум специалистов. В нем будут принимать участие врачи различного профиля. Такой подход позволяет всесторонне оценить каждый конкретный случай болезни и выбрать оптимальную тактику лечения. Еще одним плюсом коллегиальной постановки диагноза является минимальный риск врачебной ошибки. Пациент сразу же получает второе мнение и может быть уверенным в правильности выбранной линии терапии.
Как лечат лимфангиому почки?
Самый результативный способ устранения патологии, это хирургическая операция по удалению лимфангиомы почки, в израильских центрах ее производят радикально. Применяют эту технику в следующих случаях:
- Опухоль стремительно растет
- Имеет опасное расположение
- Существенно ухудшает самочувствие пациента
В процессе хирургического вмешательства лимфангиома иссекается в границах здоровых тканей. Если удалить ее полностью не удается, то не иссеченные ткани коагулируются, это снижает риск возникновения рецидива. Надо сказать, что отзывы о лечении лимфангиомы почки в Израиле с помощью данных техник самые положительные.
Кроме хирургии активно используются и другие методы, среди которых и медикаментозное лечение. В последнее время популярность набирает препарат Пицибанил, которые способен не только существенно уменьшить размер лимфангиомы, но и полностью заблокировать ее рост. Кроме этого традиционно применяется иммуно- и гормонотерапия, которые также показывают хорошие результаты. При этом стоимость лечения лимфангиомы почки в израильских клиниках с применением вышеперечисленных процедур по сей день остается максимально доступной для многих пациентов.