Что такое атеросклероз брахиоцефальных артерий?
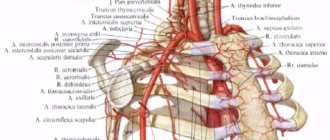
Атеросклероз брахиоцефальных артерий – это образование бляшек или атером в интиме брахицефального ствола. Он представляет собой ответвление аорты и является одним из крупных магистральных сосудов с разветвлениями на три артерии: правую позвоночную, правую подключичную и правую сонную.
Опасность образования атеросклеротических бляшек в полости брахиоцефальных артерий заключается в том, что повышается риск развития инсультов, в результате нарушения кровообращения головного мозга. Это связано с тем, что именно брахиоцефальная артерия в совокупности с общей сонной и веткой левой подключичной артерии отвечают за его кровоснабжение, образуя так называемый Виллизиев круг. При затруднении хода крови хотя бы по одной из артерий приводит к нарушению работы всей системы и негативно отражается на функционировании головного мозга. Если для определенных структур, например, костной ткани, нарушение кровоснабжения является относительно терпимой ситуацией, то мозг человека подобного патологического процесса может не перенести.
Согласно статистическим данным именно атеросклероз крупных сосудов, питающих головной мозг, в 90% случаев является причиной ишемического его поражения. К тому же, по данным ВОЗ, практически у каждого человека, перешагнувшего рубеж в 55 лет, обнаруживаются признаки атеросклеротического поражения брахиоцефальных артерий, по результатам проведения эхограммы. Манифестирует патологический процесс, как правило, после 40 лет.
Стенозирующий атеросклероз МАГ — что это такое?
Стенозированный атеросклероз является патологией кровеносных сосудов. На внутренних стенках этих сосудов образуются жировые отложения – холестериновые бляшки.
Что немаловажно, болезнь не является внезапной. Ее развитие происходит в течение длительного периода времени, с медленным образованием бляшек.
Идет процесс с формированием кальцинатов и постепенным разрастанием соединительных тканей. Механизм возникновения и распространения болезни в организме сводится к накоплению жиров низкой плотности в крови. С течением времени они налипают на малейшие неровности внутри сосудов и образуются бляшки, которые по мере прогрессирования болезни приводят к закупорке артерий. В результате уменьшается просвет для тока крови до такой степени, что кровоснабжение полностью нарушается вплоть до ишемии органов и тканей.
Симптомы атеросклероза брахиоцефальных артерий
Опасность атеросклероза брахиоцефальных артерий заключается в том, что в 50% случаев болезнь себя никак не проявляет и инсульт развивается неожиданно для человека.
Среди симптомов, которые можно заметить:
- Периодически возникающие головокружения и головные боли невыясненной этиологии. Причем кружиться голова начинает в то время, как человек делает попытку совершить резкие движения или при падении артериального давления.
- Неустойчивое эмоциональное состояние: повышенная психологическая возбудимость или развитие депрессии.
- Нарушения со стороны мыслительных процессов: снижение внимания, памяти.
- Возникновение предобморочных состояний или обмороков.
- Периодически возникающий шум в ушах.
- Снижение зрения, возникновение точек и вспышек перед глазами.
- Снижение трудоспособности на фоне повышенной утомляемости.
- Постоянно холодные конечности, независимо от температуры окружающей среды и их кратковременное онемение.
Если человек не имеет в анамнезе заболеваний, приводящих к развитию подобных симптомов, то необходимо обратиться к врачу и осуществить диагностику брахиоцефальных артерий.
Атеросклероз церебральных и периферических артерий: вопросы терапии
Атеросклероз – это хроническое заболевание сосудов эластического и мышечно–эластического типа, то есть крупных артерий. Основными патогенетическими событиями атеросклероза являются липидная инфильтрация внутренней мембраны сосудов и разрастание соединительной ткани в сосудистой стенке. На первых стадиях патологического процесса липидная инфильтрация имеет вид так называемой жировой полоски, которая не возвышается над поверхностью сосудистой стенки. Однако, в дальнейшем разрастание соединительной ткани приводят к формированию атеросклеротической бляшки, которая уменьшает просвет сосуда. Закрытие просвета сосуда на 70% и более считается гемодинамически значимым стенозом, при котором риск ишемических осложнений очень высок. При наличии крупной атеросклеротической бляшки весьма значителен риск нарушения целостности сосудистой стенки с последующим развитием тромбоза. Атеросклероз является почти универсальным патологическим процессом, который развивается у подавляющего большинства людей. При этом, по данным патологоанатомических методов исследования, первые признаки атеросклероза нередко определяются уже в 15–20–летнем возрасте. Основные факторы риска атеросклероза указаны в таблице 1 [2,4]. Клиническая картина атеросклероза церебральных артерий Из магистральных артерий головы наиболее часто атеросклероз поражает сонные артерии. В частности, типичным местом локализации атеросклеротической бляшки является бифуркация общей сонной артерии на внутреннюю и наружную сонные артерии. Физикальным признаком стенозирующего процесса данной локализации является систолический шум, который выслушивается при аускультации сонных артерий. Следует, однако, оговориться, что при полной закупорке артерии систолический шум отсутствует. Более надежными методами диагностики атеросклероза являются ультразвуковое дуплексное сканирование магистральных артерий головы, магнитно–резонансная или рентгеновская ангиография [2,4]. Гемодинамически значимый атеросклеротический стеноз является одной из основных причин цереброваскулярных расстройств, таких как транзиторные ишемические атаки, ишемический инсульт и дисциркуляторная энцефалопатия (табл. 2) [2,4,23]. Транзиторная ишемическая атака (ТИА) – это преходящее нарушение мозгового кровообращения, в основе которого лежит локальная ишемия мозга, приводящая к формированию кратковременного неврологического дефицита. По определению, симптомы ТИА проходят в течение 24 часов (самостоятельно или на фоне терапии); в противном случае речь идет об ишемическом инсульте. Риск ТИА увеличивается при сочетании гемодинамически значимого атеросклероза и системных гемодинамических расстройств (падение артериального давления, сердечного выброса), которые приводят к декомпенсации церебрального кровотока. Кроме того, ТИА могут развиваться в результате микроэмболии фрагментами атеросклеротической бляшки или тромботическими массами при нарушении целостности сосудистой стенки в области стеноза [2,4,23]. Вариант ишемического инсульта, связанный с атеросклерозом магистральных артерий головы, получил название атеротромботического инсульта. Как видно из данного термина, в его основе лежат два патологических процесса: атеросклероз, который, при нарушении целостности сосудистой стенки, осложняется тромбозом. Развитие тромбоза ведет к полной окклюзии магистральной артерии или к артерио–артериальной эмболии. Атеротромботическому инсульту нередко предшествуют ТИА в том же бассейне. Полная окклюзия крупной артерии часто развивается постепенно, в течение нескольких часов (так называемый прогрессирующий инсульт) и приводит к формированию крупных корковых инфарктов со значительной неврологической симптоматикой [2,4,23]. Наряду с острыми нарушениями атеросклероз является одной из основных причин хронической сосудистой мозговой недостаточности, которая в отечественной неврологической практике обозначатся термином дисциркуляторная энцефалопатия (ДЭ). В качестве синонима ДЭ иногда употребляются выражения «хроническая ишемия мозга», «ишемическая болезнь мозга», «ангиоэнцефалопатия» и некоторые другие. С нашей точки зрения, термин «дисциркуляторная энцефалопатия» наиболее точен, так как отражает локализацию поражения (энцефалопатия) и его природу (дисциркуляция, острая или хроническая) [4,23]. В течении ДЭ выделяют три основных стадии (табл. 3). На третьей стадии этого заболевания в большинстве случаев отмечается синдром сосудистой деменции, а в неврологическом статусе определяется сочетание псевдобульбарного, пирамидного, экстрапирамидного и атактического синдромов (нередко в сочетании с тазовыми расстройствами) [5,27,28]. Периферическая артериальная недостаточность Цереброваскулярные расстройства являются лишь одним из проявлений системного атеросклероза и, как правило, сочетаются с поражением других органов мишеней. В частности, нарушения мозгового кровообращения нередко сочетаются с периферической артериальной недостаточностью, основным проявлением которой является вазогенная перемежающая хромота. Популяционные исследования свидетельствуют, что встречаемость сосудистой перемежающей хромоты в возрастном промежутке от 55 до 74 лет составляет 4,5%. Еще у 8% лиц той же возрастной группы встречаются асимптомные атеросклеротические стенозы брюшной аорты и сосудов нижних конечностей [37]. Атеросклероз нижних конечностей в 70% случаев сочетается с ишемической болезнью сердца и в 25% случаев – с сосудистой мозговой недостаточностью [7,19]. Основные принципы терапии атеросклероза Основными методами лечения атеросклероза церебральных и периферических артерий являются сосудистая хирургия, антитромбоцитарная, гиполипидемических терапия и воздействие на микроциркуляторное сосудистое русло. Для профилактики инсульта и других цереброваскулярных расстройств при наличии гемодинамически значимого стеноза магистральных артерий головы выполняется каротидная эндартерэктомия или стентирование сонных артерий. В настоящее время профилактический эффект оперативного вмешательства считается доказанным у пациентов с ТИА, малым инсультом или инсультом с минимальным неврологическим дефицитом в анамнезе. Более сложен вопрос о целесообразности хирургического лечения асимптомного (до развития ТИА или инсульта) стеноза церебральных артерий. В этих случаях убедительных данных, подтверждающих профилактический эффект оперативного вмешательства, пока не получено [2,4]. При атеросклерозе сосудов нижних конечностей показанием к хирургическому лечению является 2Б и более поздние стадии патологического процесса по классификации А.B. Покровского (табл. 4) [7, 20]. Наличие атеросклеротического стеноза крупных артерий является безусловным показанием к назначению антитромбоцитарных средств. К препаратам с доказанной антитромбоцитарной активностью относятся ацетилсалициловая кислота в дозах 50–100 мг в сутки и клопидогрел в дозе 75 мг в сутки. По статистике, антитромбоцитарная терапия снижает риск развития инфарктов миокарда, ишемических инсультов и периферических тромбозов на 20–25%. Однако известна широкая вариабельность индивидуального ответа на антитромбоцитарную терапию. В частности, у некоторых пациентов (особенно женщин) на фоне назначения ацетилсалициловой кислоты наблюдается парадоксальное увеличение агрегации форменных элементов крови. Поэтому после назначения антитромбоцитарной терапии для контроля эффективности необходимо лабораторное исследование состояния гемостаза [2,4]. При наличии гемодинамически значимого стеноза церебральных или периферических сосудов может обсуждаться необходимость применения гиполипидемических препаратов для профилактики дальнейшего нарастания атеросклероза. В настоящее время наиболее широко применяются гиполипидемические препараты из группы статинов. Данные препараты, безусловно, показаны при наличии некорригируемой диетой гиперхолестеринемии. В ряде случаев практикуется назначение статинов даже при нормальном уровне атерогенного холестерина при наличии высокого риска развития ишемических осложнений (в частности, у больных сахарным диабетом, ишемической болезнью сердца и др.) [32]. При наличии церебрального или периферического атеросклероза необходимо корригировать другие имеющиеся сосудистые факторы риска, такие как артериальная гипертензия, курение, злоупотребление алкоголем, сахарный диабет, ожирение, гиподинамия и др. Следует, однако, соблюдать осторожность при проведении антигипертензивной терапии пациентам с выраженным стенозом магистральных артерий головы. В этих случаях излишне быстрое и выраженное снижение артериального давления не уменьшает, а напротив, увеличивает риск ишемического инсульта [2,4]. Коррекция микроциркуляторных нарушений Важной стратегией лечения атеросклероза является медикаментозная оптимизация кровообращения в микроциркуляторном русле. Воздействие на микроциркуляцию оправдано как при церебральной, так и при периферической артериальной недостаточности. С этой целью используют так называемые вазоактивные («сосудистые») препараты. К ним относятся ингибиторы фосфодиэстеразы (теофиллин, пентоксифиллин, винпоцетин), блокаторы кальциевых каналов (циннаризин, флунаризин, нимодипин) и a–адреноблокаторы (ницерголин). Одним из наиболее перспективных сосудистых препаратов для лечения церебральной и периферической артериальной недостаточности является Танакан, который оказывает разнонаправленное положительное воздействие на микроциркуляцию и нейрональный метаболизм [9,35,39]. Танакан представляет собой стандартизованный и титрованный экстракт из натурального сырья. Препарат действует на все участки сосудистого русла (артериолы, капилляры, венулы). В эксперименте доказано, что на фоне применения препарата в большей степени расширяются спазмированные или склерозированные микрососуды, то есть не развивается «эффект обкрадывания» [35]. Свидетельства положительного воздействия Танакана на микроциркуляцию были получены как в экспериментальных, так и в клинических работах с помощью капилляроскопии и радионуклидных методов исследования [1,6,11,12,14,15,24,39,41]. Клинический опыт применения Танакана насчитывает более 20 лет и базируется на надежной доказательной базе. В западноевропейских странах эффективность Танакана при хронической сосудистой мозговой недостаточности подробно исследовалась в 80–90–х годах XX века. Было показано, что на фоне применения Танакана наблюдается улучшение памяти и других когнитивных функций у пациентов с сосудистой деменцией и менее выраженными когнитивными нарушениями. Положительный эффект терапии был зафиксирован с помощью клинических, нейропсихологических и электрофизиологических методов исследования [9,30,36,38,40]. Следует особенно подчеркнуть, что, по данным ретроспективного исследования EPIDOS, пожилые лица, длительное время применяющие Танакан, характеризуются достоверно меньшим риском развития деменции, чем те, кто принимают другие сосудистые препараты или не лечатся вовсе [31]. В России к настоящему времени также накоплен достаточный опыт применения Танакана как при нарушениях церебрального, так и периферического кровообращения. В 1998 г. Н.Н. Яхно и соавт. применяли данный препарат у больных с ранними формами хронических нарушений мозгового кровотока [26]. Было показано положительное влияние проводимой терапии на память, концентрацию и устойчивость внимания, ассоциативные процессы, психомоторные функции. По данным электрофизиологических методов исследования после лечения было зафиксировано достоверное уменьшение относительной мощности медленноволновой активности. Эффект терапии был достаточно стойким, о чем свидетельствовало катамнестическое наблюдение за частью пациентов [22]. Эффективность Танакана при церебральной сосудистой недостаточности изучалась в России и странах СНГ еще не менее чем в 10 клинических исследованиях [1,3,6,11,14,15,17,21,35]. В общей сложности в них приняли участие более 500 пациентов. Из них 100 – имели в анамнезе оперативные вмешательства на магистральных артериях головы (исследование Л.А. Дзяк и соавт. [6]), 90 пациентов подвергались в прошлом проникающей радиации (исследование Г.М. Румянцевой и соавт. [21], В.Л. Малыгина и соавт. [15]). 30 пациентов, помимо ДЭ, страдали облитерирующим атеросклерозом нижних конечностей (исследование В.В. Шпрах и соавт., [24]). Эффективность Танакана оценивалась по формализованным клиническим шкалам и опросникам, с помощью которых давалась количественная оценка субъективных и объективных неврологических симптомов, когнитивных, эмоционально–аффективных и поведенческих нарушений. Кроме того, в 5 исследованиях использовались нейропсихологические методы [1,6,15,21,24], в 3 – ультразвуковая допплерография [6,14,24], и в 2 исследованиях – капилляроскопия сосудов бульбарной конъюнктивы [6,10]. Танакан назначался в дозах 120–160 мг/сут. в течение 45–90 дней. Во всех работах было показано благоприятное воздействие Танакана на клиническое состояние больных, показатели психометрических шкал и нейропсихологических тестов. В ряде работ было отмечено улучшение мозговой гемодинамики по данным УЗДГ, оптимизация биоэлектрической активности головного мозга, нормализация капилляроскопической картины. Наибольший эффект отмечалася при нетяжелых неврологических расстройствах, что указывает на целесообразность наиболее раннего назначения Танакана при ДЭ [14,17]. Положительный эффект Танакана в отношении когнитивных функций недавно был вновь продемонстрирован в крупномасштабном многоцентровом исследовании у пациентов с синдромом умеренных когнитивных нарушений в пожилом возрасте (координатор исследования – акад. РАМН, проф. Н.Н. Яхно). Было показано, что применение данного препарата в течение 6 месяцев способствует достоверному регрессу выраженности нарушений памяти, внимания, диспрактических и интеллектуальных нарушений. При этом выраженность положительного эффекта на 6–м месяце лечения была достоверно большей по сравнению с 3–м месяцем, что свидетельствует о целесообразности более продолжительных курсов, чем обычно принято в неврологической практике [28]. Следует отметить, что будучи препаратом натурального происхождения Танакан характеризуется благоприятным профилем безопасности и переносимости, что позволяет применять его в течение длительного времени, не опасаясь причинения какого–либо вреда здоровью. Сегодня имеется также серьезный опыт применения Танакана при периферической артериальной недостаточности. U. Bauer исследовал эффективность Танакана при облитерирующем атеросклерозе нижних конечностей в двойном слепом плацебо–контролируемом исследовании. Пациенты получали препарат в дозе 120 мг/сут. в течение шести месяцев. После курса лечения было зафиксировано достоверное увеличение дистанции ходьбы до появления боли по сравнению с плацебо [33]. Аналогичные результаты были получены в работе E.D. Berndt и M. Kramar. При этом было показано превосходство Танакана над буфломедилом [34]. Эффективность Танакана при облитерирующем атеросклерозе нижних конечностей исследовалось также В.М. Кошкиным и соавт. Препарат назначался в дозе 160 мг/сут. в течение трех месяцев. Было показано, что лечение Танаканом способствует увеличению дистанции безболевой ходьбы, уменьшению частоты судорог в икроножных мышцах. Кроме того, было отмечено уменьшение выраженности головокружения и повышение потенции [10]. Те же эффекты Танакана были показаны в работе А.В. Покровского и А.В. Чупина, которые применяли препарат в дозе 80 мг/сут. в течение 90 дней у 30 пациентов с облитерирующим атеросклерозом нижних конечностей [18]. О положительном эффекте Танакана при данной патологии сообщает также Ю.В. Лукьянов [13]. В ряде работ на фоне терапии Танаканом отмечено увеличение регионарного систолического давления и систолической частоты по данным допплерографии, что свидетельствует об увеличении кровоснабжения нижних конечностей [16,24,25]. О.А. Лобут и соавт. применяли Танакан в дозе 120 мг/сут. в течение 3 месяцев у пациентов с ишемическим поражением верхних конечностей. Было показано, что курс терапии способствует уменьшению выраженности субъективных симптомов, таких как онемение пальцев рук, похолодание кистей, сухость кожи, гипергидроз. Отмечалась также положительная динамика по данным ультразвуковой допплерографии [12]. Таким образом, результаты проведенных исследований и многолетняя клиническая практика подтверждают несомненную целесообразность применения длительных повторных курсов Танакана при ведении пациентов с церебральной и периферической артериальной недостаточностью.
Литература 1. Астапенко А.В., И.П.Антонов, В.Б.Шалькевич, Г.И.Овсянкина. Применение танакана в неврологической практике. //Жур.Медицинские новости. –Минск. –1999. –№ 1–2. –С.32–33. 2. Варлоу Ч.П., М.С.Деннис, Ж.ван Гейн и др. Инсульт. Практическое руководство для ведения больных //Пер. с англ. –СПб. –1998. –С.629 3. Гаврилова С.И., И.В.Колыхалов, И.М.Милопольская, М.А.Морозова, Н.Д.Селезнева. Танакан в лечении начальных проявлений церебрально–сосудистой недостаточности. //Клиническая геронтология. –1995. –№ 4. –С.22–23. 4. Дамулин И.В., Парфенов В.А., Скоромец А.А., Яхно Н.Н. Нарушение кровообращения в головном и спинном мозге. //В кн.: «Болезни нервной системы. Руководство для врачей». Под ред. Н.Н..Яхно, И.В.Дамулина. –М.: изд–во «Медицина». –2001. –Т.1. –С.239–302. 5. Дамулин И.В. Болезнь Альцгеймера и сосудистая деменция. //Под ред. Н.Н.Яхно. –М. –2002. –С.85. 6. Дзяк Л.А., В.А.Голик, И.В.Рожкова. Опыт использования танакана в лечении церебральных ишемий, обусловленных патологией магистральных артерий головы в послеоперационном периоде. Материалы научно–практического симпзиума «Танакан».–Киев. –1997. –Тезисы докладов. –С.5–6. 7. Затевахин И.И., Золкин В.Н., Степанов Н.В., Цициашвили М.Ш. Облитерирующие заболевания аорты и нижних конечностей. //Русский медицинский журнал. –2001. –№ 3–4. –С.126–131. 8. Захаров В.В., И.В.Дамулин, Н.Н.Яхно. Медикаментозная терапия деменций. Клиническая фармакология и терапия. –1994. –Т.3. –№ 4. –С.69–75. 9. Захаров В.В. Применение танакана в нейрогериатрической практике. //Неврологический журнал. –1997. –Т.5. –С.42–49. 10. Кошкин В.М. Консервативная терапия хронических облитерирующих заболеваний артерий конечностей.//Русский медцинский журнал. –1997. –Т.6. –№ 13. –С.820. 11. Лазебник Л.Б., С.Б.Маличенко, Ю.В.Конев. Танакан в лечении начальных проявлений сосудисой деменции в инволюционном периоде. //Научно–практическая конференция «Пожилой больной. Качество жизни». –М. –1996. –Тезисы докладов. –С.119. 12. Лобут О.А., Н.П.Макарова. Клиническое применение препарата танакан у пациентов с хронической ишемией верхних конечностй. //В сб.: Танакан: оыт применения в медицинской практике в странах СНГ. –М. –2001. –С.77. 13. Лукьянов Ю.В. Оценка эффективности лечения больных с облитерирующим атеросклерозом нижних конечностей. //Материала юбилейной конференции к столетию С–Пб гос. Мед. Университета. –С–Пб. –1997. –Тезисы докладов. –С.192. 14. Малахов В.А., Е.В.Кочуева. Сравнительная эффективность винпоцетина и танакана (Egb 761) при монотерапии больных с начальными формами сосудистых заболеваний головного мозга. //Фармакологiчний вiсник. –Киев. –грудень 1997. –С50–52. 15. Малыгин В.Л., В.А.Жеребцова, Е.А.Атлас. //Танакан в терапии церебральных сосудистых расстройств у лиц, подвергшихся действию малых доз радиации. //6–й Российский национальный конгресс «Человек и лекарство». –М. –1999. –Тезисы докладов. –С.99. 16. Наумов С.С. Результаты применения танакана у больных хронической артериальной недостаточностью сосудов нижних конечностей в условиях поликлиники. // В сб.: Танакан: оыт применения в медицинской практике в странах СНГ. –М. –2001. –С.73–74. 17. Пирогова Л.Г., Г.С.Ниеткалиева. Применение препарата танакан в лечении больных с дисциркуляторной энцефалопатией II–III стадии, перенесших малые инсульты и лакунарные инфаркты. //Информационный бюллетень «Новое в медицине и фармации». –Алматы. –1998. –№ 2. –С.4. 18. Покровский А.В., А.В.Чупин, О.Г.Грязнов. Клиническое испытание препарата танакан у пацентов с атеросклеротическим поражением артерий нижних конечностей. //Международный симпозиум «Консевативная терапия в ангилогии. Опыт применения препаратов танакан и Гингко форт». –М. –1997. –Тезисы докладов. –С.37. 19. Покровский А.В., Кошкин В.М., Кириченко А.А. и др. Вазапростан (простагландин Е1) в лечении тяжелых стадий артериальной недостаточности нижних конечностей. //Пособие для врачей. –М. –1999. –16С. 20. Покровский А.В., Абрамова Н.Н., Анбатьелло С.Г. Клиническая ангиология. Руководство для врачей. //Под ред. А.В.Покровского. –Москва. –2004. –Т.1. –808С. 21. Румянцева Г.М., И.М.Милопольская, А.В.Грушков, О.В.Чинкина, Т.М.Левина, Т.Н.Соколова. Эффективность лечения препаратом танакан больных с психоорганическим синдромом пограничного уровня, получивших в прошлом различные дозы ионизирующего облучения. //Российский психиатрический журнал. –1999. –№ 1. –С.31–36. 22. Тимербаева С.Л., З.А.Суслина, Э.А.Бодарева, П.А.Федин, О.С.Корепина, Б.Е.Первозванский. //Танакан в лечении начальных проявлений недостаточности кровоснабжения мозга: эффективность, переносмость и отдаленные результаты.//Ж. Неврологии и Психиатрии им. С.С.Корсакова. –1999. –С.54–61. 23. Шмидт Е.В. Классификация сосудистых поражений головного и спинного мозга. //Ж невропатологии и психиатрии. –1985. –№ 9. –С.1281–1288. 24. Шпрах В.В., В.В.Чернявский, М.Б.Татаринова, А.Л.Тарабин, И.В.Шаламова. Особенности клиники, диагностики и лечения цереброваскулярных заболеваний у лиц с облитерирующим атеросклерозом магистральных и периферийных артерий. //Сборник научно–практических статей «Проблемы клинической ангиологии и сосудистой хирургии». –Вып.1. –Иркутск. –1998. –100–107. 25. Янушко В.А. Применение танакана при облитерирующих заболеваниях сосудов нижних конечностей. //Здравоохранение. –Минск. –1999. –№ 6. –С.54–56. 26. Яхно Н.Н., И.В.Дамулин, В.В.Захаров, М.Н.Елкин, Л.Г.Ерохина, Л.В.Стаховская, Н.С.Чекнева, З.А.Суслина, С.Л.Тимербаева, П.А.Федин, Э.А.Бодарева, А.А.Скоромец, В.А.Сорокоумов, В.Т.Ивашкин, Ю.В.Гигорьев, Б.Е.Первозванский. Применение танакана при начальных стадиях сосудистой мозговой недостаточности: результаты открытого мультицентрового исследования. //Неврологический журнал. –1998. –Т.3. –С.18–22. 27. Яхно Н. Н., Левин О. С., Дамулин И. В. Сопоставление клинических и МРТ–данных при дисциркуляторной энцефалопатии. Сообщение 1: двигательные нарушения // Неврол. журн. – 2001. – N 2. – C. 10–16. 28. Яхно Н. Н., Левин О. С., Дамулин И. В. Сопоставление клинических и МРТ–данных при дисциркуляторной энцефалопатии. Сообщение 2: когнитивные нарушения // Неврол. журн. – 2001. – N 3. – C. 10–19. 29. Яхно Н.Н., Захаров В.В., Локшина А.Б. и соавт. Танакан (EGB 761) в терапии умеренных когнитивных нарушений. //Ж. невропатологии и психиатрии. –2007 г. (в печати). 30. Arrigo A. Die Behandlung der chronischen zerebrovaskularen Insuffizienz mit Ginkgo biloba extrakt.//Therapiwoche. –1986. –V.36. –P.5208–5218. 31. Andrieux S., Amouyal K., Renish W. и соавт. The consumption of vasodilators and Ginkgo biloba (Egb 761) in a population of 7598 women over the age of 75 years. // Research and practice in Alzheimer’s disease. –2001. –V.5. –P.57–68. 32. Baiqent C., Keech A., Kearney P.M. et al. Efficacy and safety of cholesterol lowering treatment: prospective meta–analysis of data from 90056 participants in 14 randomized trials of statins. //Lancet. –2005. –V.366. –N.9493. –P.1967–1978. 33. Bauer U. Etude clinicue d L’EGb 761 dans l’artertedes members inferieurs. Essai a duble insu face au placebosur 6 mois. //Arzneim Forsh Drug Res. –1984. –V.34. –N.6. –P.716–720. 34. Berndt E.D., M.Kramar. Traiement medicamente ux des members inferieurs au stade 2b. //Therapiewoche. –1984. –V.187. –N.37. –P.2815–2819. 35. Clostre F. De l’organisme aux membranes cellulaires : lex differents niveuax d’actions pharmacologiques de l’extrait de Ginkgo biloba. //Presse Med; –1986. –V.15. P.1529–1538. 36. Dieli G., V.LaMantia, M.Saetta, E.Constanzo. Studio clinico in doppio cieco del Tanakan nell’insufficienza cerebrale cronica. //Lav Neuropsihiatr. –1981. –V.68. –P.3–15. 37. Fowkes F.G., Housley E., Cawood E.H. et al. Edinburgh artery study: prevalence оf asymptomatic and symptomatic peripheral arterial disease in the general population. //Int J Epidimiol.– 1991. –V.20. –P.384–392. 38. Israel L., E.Dell’Accio, G.Martin, R.Hugonot. Extrait de Ginkgo biloba et expercises d’entrainement de la memoire. Evaluation comparative chez des personnes agees ambulatoires. //Psychol Med. –1987. –V.19. –P.1431–1439. 39. Kleijnen J., P.Knipschild. Ginkgo biloba. //Lancet.–1992. –V.340 : Nov 7.–P.1136–1139. 40. Pidoux B., C.Bastein, S.Niddam. Clinical and quantative EEG double–blind study of GBE. //J Cerebral Blood Flow Metabolism. –1983. –V.3. –P.5556–5557. 41. Spinnewyn B. Ginkgo biloba extract (EGb 761) protects against delayed neuronal death in gerbil. //In : Y.Christen, J.Costentin, M.Lacour (eds): Effects of Ginkgo biloba extract (EGb 761) on central nervous system. Advances in Ginkgo biloba Extract esearch. –Elsevier, Paris. –1992.–P.113–118.
Причины заболевания
Среди причин, приводящих к развитию болезни, можно выделить:
- Вредные привычки, в частности, курение, которое приводит к нарушению обмена веществ, снижению эластичности сосудов, повышению давления.
- Гипертензия первичного или вторичного типа.
- Повышение уровня холестерина в крови, что связано не только с нерациональным питанием, но и с заболеваниями внутренних органов, малоподвижным образом жизни и пр.
- Прием гормональных контрацептивов.
- Некоторые болезни иммунной системы, сахарных диабет, любые метаболические нарушения в организме.
- Повышение массы тела.
Все эти причины являются факторами-провокаторами, способными вызвать заболевание.
Последствия и осложнения
Несвоевременное выявление болезни и отсутствие должного ее лечения может привести к необратимым и очень тяжелым последствиям. К примеру, поражение сонных артерий может спровоцировать инсульт, а сильная закупорка магистральных артерий головы может привести к массивным кровоизлияниям. Существует ряд осложнений, провоцируемых стремительным прогрессированием болезни:
Острые. Развитие болезни может привести к серьезным нарушениям мозгового и сердечного кровообращения (аневризма аорты, гангрена, ишемия сердечной мышцы и т.д.).- Хронические. Недостаточное кровообращение в пораженных болезнью частях тела приводит со временем к функциональным и затем органическим (к сожалению, необратимым) изменениям. Так, если атеросклероз БЦА был обнаружен несвоевременно или вовремя не было назначено лечение, у больного со временем начнется неврологическое нарушение в мозге. На этой почве часто развивается слабоумие.
Диагностика
Прежде чем приступать к лечению атеросклероза брахиоцефальных артерий, необходимо определить степень закрытия просвета, а также скорость циркуляции крови как до проблемного участка, так и после него. Основной метод диагностики, используемый для реализации поставленных целей, является триплексное сканирование артерий. То есть обычное ультразвуковое исследование в данном случае дополняется цветным доплеровским излучением. Сканирование даёт возможность оценить состояние артерий шейного отдела, несущих кровь к мозгу.
При необходимости диагностика атеросклероза брахиоцефальных артерий может быть расширена такими методами исследования, как: дуплексное сканирование, магнитно-резонансная ангиография.
Диагностика патологии не затруднена благодаря современному оборудованию, позволяющему просмотреть каждый сосуд и выявить болезнь на первоначальном этапе её развития.
Диагностика заболевания
Для диагностирования болезни применяется целый ряд медицинских приборов и процедур:
- Первоначально врач собирает анамнез болезни, узнает у больного о его образе жизни и привычках, затем приступает к визуальному осмотру.
- После получения первичных данных больной должен сдать ряд анализов (общий, биохимический и иммунологический анализы крови, анализ мочи – для выявления возможного воспалительного очага).
- Специалист делает ЭКГ и УЗИ сердца, МРТ.
Важно! УЗИ-признаки считаются наиболее точным подтверждением неприятного диагноза. Допплерографическая картина основывается на сигналах ультразвукового аппарата, которые получают во время осуществления процедуры путем отражения от элементов крови. - При получении сомнительного результата врач дополнительно назначает ангиографию для определения уровня тока крови в сосудах.
- Эхокардиография дает возможность определить наличие поражения сосудов сердца, а стресс-эхокардиография позволяет не только выявить наличие значимого атеросклероза, но и определить его локализацию.
- При необходимости врач советуется с другими специалистами в зависимости от области, пораженной стенозирующим атеросклерозом.
Лечение атеросклероза брахиоцефальных артерий
После того, как болезнь была диагностирована, врач принимает решение о том, какое лечение подходит для каждого конкретного пациента.
Медикаментозное лечение
Медицинские средства (лекарства, витамины, медикаменты) упоминаются в ознакомительных целях. Мы не рекомендуем их использовать без назначений врача. Рекомендуем к прочтению: «Почему нельзя принимать медицинские препараты без назначения врача?».
Когда нет необходимости в проведении операции, то пациента ставят на учет к невропатологу и осуществляется медикаментозная регуляция состояния. Обязательными к приему являются антикоагулянты: аспирин или клопидогель, которые являются средствами, разжижающими кровь, что в свою очередь, снижает риск развития тромбоза. Принимать эти медикаменты пациенту необходимо будет пожизненно, как и регулярно сдавать кровь для определения уровня холестерина.
Кроме того, врач может рекомендовать средства, улучшающие ток крови, снимающие спазмы и расширяющие сосуды, среди них: кавинтон, курантил, актовегин.
Статины и фибраты назначаются только врачом, после тщательной диагностики и под непосредственным контролем лечащего доктора, так как статины имеют множество противопоказаний и побочных эффектов. Из современных средств для снижения холестерина применяются эзетрол, эволокумаб и алирокумаб. В дополнение к ним часто назначается приём омега-3.
Больному необходимо будет пересмотреть собственный рацион, исключив из него жирную и жареную пищу. Особенно рекомендуется средиземноморская диета, которая снижает риск развития осложнений на 50%.
Подробнее:
Препараты для лечения атеросклероза
Кроме того, есть растительные препараты от атеросклероза, которые доказали свою эффективность, подробнее о них описано тут.
Стенозирующий атеросклероз магистральных артерий нижних конечностей
Патологии характерны все симптомы предыдущей формы без окклюзии, которые были описаны выше, а также некоторые дополнительные характерные признаки стенозирующего атеросклероза:
хромота (сначала при ходьбе на длительные дистанции, а со временем и на короткие);- покраснение и похолодание стоп;
- отеки стоп;
- боль в икроножных мышцах, ягодицах, бедрах и пояснице усиливается (возникает даже ночью и в состоянии покоя);
- трофические язвы;
- гангрена.
Изменения при обследовании
Отличительной особенностью данного состояния является то, что сужение просвета сосудов будет больше, чем на 50%, а состояние стенки значительно хуже. Это видно на ангиографии, ультразвуковой допплерографии (кровоток замедлен сильнее, чем при нестенозирующем, или вообще прекращен), компьютерной томографии. При объективном обследовании отсутствие пульсации на основных артериях, отеки, язвы, гангрена.
Принципы лечения
Для оказание медикаментозной помощи пациента используются все вышеописанные консервативные методы, которые применимы для нестенозирующего атеросклероза.
Часто врачи прибегают к лечению больного хирургическими методами:
Баллонная дилатация.- Ангиопластика.
- Стентирование пораженных артерий (широко применяется при коронаросклерозе)
- Протезирование поврежденного участка сосуда. Используется синтетический материал.
- Шунтирование — создание искусственного канала, в обход участку артерии, который не функционирует.
- Тромбэндартерэктомия – удаление бляшки внутри сосуда.
- Ампутация (отсечение дистальной части конечности) в случае гангрены.