Быстрый переход Лечение аутоиммунной гемолитической анемии
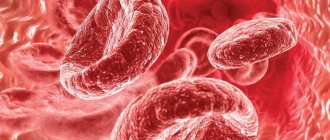
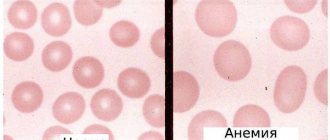
Аутоиммунная гемолитическая анемия (АИГА) — группа редких приобретенных гематологических болезней и синдромов, характеризующихся гемолизом (разрушением) эритроцитов, вследствие образования аутоантител к антигенам этих компонентов крови.
АИГА может возникнуть в любом возрасте, чаще ей подвержены женщины (60%). Патология развивается постепенно или внезапно.
Выделяют два основных типа АИГА: тепловую (аутоантитела наиболее активны/атакуют эритроциты при температуре 37-40 °C) и холодовую — с холодовыми гемолизинами (аутоантитела наиболее активны при температуре менее 30 °C, эритроциты разрушаются даже при локальном воздействии холода, например, когда человек пьет холодную воду или моет руки в холодной воде).
Распространенность АИГА составляет 1 случай на 70-80 тысяч человек в год.
Причины
Причины возникновения заболевания изучены недостаточно. На сегодняшний день известно, что примерно 50% случаев т-АИГА являются идиопатическими (развиваются спонтанно). Тогда как х-АИГА ассоциированы с другими заболеваниями или возникают с ними одновременно: аутоиммунными, онкологическими, инфекционными (системная красная волчанка, лимфолейкоз, неходжкинская лимфома, вирус Эпштейна — Барр, цитомегаловирус, микоплазменная пневмония, гепатит, ВИЧ). Играть роль в развитии АИГА может и прием определенных лекарств, например, препаратов пенициллинового ряда (лекарственно индуцированная АИГА).
Лечение макроцитарной анемии
Лечение макроцитарной анемии применяют такое, которое воздействует на причину патологии. Иногда простое устранение токсина или медикамента может вылечить макроцитарную анемию.
Если у больных выявлена недостаточность фолатов, то назначают ФК по 1 мг в день до нормализации показателей. При дефиците цианокобаламина назначают внутримышечно назначают кобаламин. Обычно скоро возникает ретикулоцитоз (в течение недели от старта лечения витаминами). Полное устранение анемии достигается через 6 недель.
Анемия при недостаточности фолатов идентична анемии при недостаточности цианокобаламина, хотя только при последней могут возникнуть подострые демиелинизирующие неврологические заболевания. Поэтому у больных с дефицитом цианокобаламина терапевтические дозы фолатов могут изменить к лучшему гематологическую ситуацию, тогда как неврологические проявления прогрессировать с инвалидизирующими последствиями. Поэтому при мегалобластной анемии стараются не спутать названные состояния на ранних стадиях.
Заместительная терапия тиреоидными гормонами обычно корректирует макроцитарную анемию, связанную с гипотироидизмом.
Все наши врачи-терапевты высшей квалификационной категории, кандидаты и доктора медицинских наук регулярно проходят курсы усовершенствования, осваивают дополнительные методики. Специалист назначит все необходимые лабораторные и инструментальные обследования. В кратчайшие сроки поставит диагноз – в распоряжении врачей клиники ИНТЛмед современная лаборатория и отделение функциональной диагностики. Звоните, чтобы записаться на прием.
Симптомы
У некоторых людей заболевание может протекать бессимптомно, особенно если АИГА развивается постепенно (разрушение эритроцитов не настолько масштабно). В основном же симптомы АИГА схожи с клиническими проявлениями других типов анемии (слабость, повышенная утомляемость, бледность кожных покровов).
Симптомы при более тяжелом течении заболевания (быстром разрушении эритроцитов) включают желтушность кожных покровов и видимых слизистых оболочек, слабость, повышенную утомляемость с тахикардией и одышкой при физической нагрузке, ощущение дискомфорта в животе, чувство переполнения, холодные конечности и периферический цианоз (при холодовой АИГА). При физикальном осмотре выявляется спленомегалия (патологическое увеличение размеров селезенки) различной степени.
Если АИГА развивается на фоне другой патологии, преобладать могут симптомы основного заболевания, например: увеличение и болезненность лимфатических узлов, лихорадка, сильные боли в спине и ногах, головные боли, рвота, диарея, изменение цвета мочи на темно-коричневый.
Микросфероцитарная гемолитическая анемия (болезнь Минковского — Шоффара)
Микросфероцитарная гемолитическая анемия (болезнь Минковского — Шоффара)
Микросфероцитарная гемолитическая анемия (болезнь Минковского — Шоффара) — наследственное заболевание, обусловленное дефектом белков мембраны эритроцитов, приобретающих сферическую форму с последующим их разрушением макрофагами селезенки.
Эпидемиология Болезнь широко распространена в Европе, в меньшей степени — на Африканском континенте, в Японии и других странах, нередко встречается в нашей стране. Она проявляется в любом возрасте, чаще в детском и подростковом, встречается у близких родственников больного. Существует бессимптомное носительство гена микросфероцитоза.
Этиология и патогенез Микросфероцитарная гемолитическая анемия наследуется по аутосомно-доминантному типу, встречается в основном гетерозиготная форма заболевания. Патогенез связан с дефектом белков мембраны эритроцитов, что сопровождается повышенной ее проницаемостью с поступлением избыточного количества ионов натрия в клетки. Это способствует накоплению в клетке воды, вследствие чего эритроциты деформируются, приобретают сферическую форму. При определенном уровне изменений в структуре мембраны эритроцитов микросфероциты подвергаются внутриклеточному разрушению макрофагами селезенки, что связано со своеобразным кровообращением в ней.
Классификация Выделяют формы наследственной микросфероцитарной гемолитической анемии в подростковом периоде и у взрослых. У детей заболевание диагностируется, когда обследуют семьи пробандов. Редко встречается вариант микросфероцитарной анемии, протекающей с апластическими (арегенераторными) кризами.
Болезнь олбрайта. Симптомы, причины и лечение
Примерная формулировка диагноза: Наследственная микросфероцитарная гемолитическая анемия с увеличением селезенки, пигментными камнями в желчном пузыре, периодическим потемнением мочи, выраженным микросфероцитозом эритроцитов, ретикулоцитозом, лейко- и тромбоцитопенией, умеренной эритробластической реакцией костного мозга, увеличением свободной фракции билирубина сыворотки крови.
Клиника Больные отмечают общую слабость, быструю утомляемость, головокружение, шум в голове, одышку и сердцебиение при физических нагрузках, желтушность кожи и склер, боли в левом (при наличии спленомегалии) и в правом подреберье (при образовании пигментных камней в желчном пузыре и в желчевыводящих путях, редко — при увеличении печени), периодическое потемнение мочи, трофические язвы на голенях, склонность к развитию тромбозов, кожные изменения типа пигментации, экзем, гемангиом и др. Если заболевание с детства протекает с выраженной клинической симптоматологией, наблюдаются деформации скелета, особенно костей черепа.
Анемия нормохромная в большинстве случаев умеренная (гемоглобин 90—100 г/л, при частых и глубоких гемолитических кризах она более выражена (гемоглобин 40—50 г/л), иногда заболевание в течение длительного периода протекает без анемии на фоне небольшого ретикулоцитоза и умеренно выраженной эритробластической реакции костного мозга.
Важным признаком является микросфероцитоз эритроцитов. Средний диаметр их бывает меньше 6,3 мкм, средний объем нормальный, средняя толщина заметно увеличена (больше 2,1 мкм). Сфероцитарный индекс (отношение между диаметром и толщиной эритроцита) всегда снижен в среднем до 2,7 (вместо 3,4—3,9 в норме). В период гемолитических кризов значительно увеличивается свободная фракция билирубина сыворотки крови. Продолжительность жизни эритроцитов, меченных Cr, уменьшена почти в 2 раза по сравнению с нормой. Секвестрация их происходит преимущественно в селезенке.
Диспепсия функциональная. Симптомы, причины и лечение
Метод кислотных эритрограмм выявляет присущие этой болезни характерные изменения — резкое удлинение времени гемолиза, смещение его максимума вправо. Отмывание эритроцитов от плазмы резко ускоряет гемолиз.
При гемолитических кризах наблюдается иногда небольшой лейкоцитоз со сдвигом формулы влево, при явлениях гиперспленизма возможны умеренная лейкопения и тромбоцитопения. Количество ретикулоцитов обычно в пределах 5—10%, гемолитический криз сопровождается увеличением содержания их в несколько раз. В костном мозге резко увеличен эритробластический росток или даже преобладают эритро- и нормобласты. Иногда после гемолитического криза при снижении уровня фолиевой кислоты и витамина В12 обнаруживаются мегалобласты.
Выявляющийся параллелизм между сфероцитозом эритроцитов и понижением их осмотической резистентности, а также повышением аутогемолиза, корригируемый глюкозой, не строго специфичен для наследственной микросфероцитарной гемолитической анемии.
Верификация диагноза При верификации диагноза следует учитывать ее характерные клинико-гематологические признаки. Вместе с тем микросфероцитоз часто встречается при аутоиммунных гемолитических анемиях, иногда — при наследственных дизэритропоэтических анемиях. Что же касается деформации скелета, особенно черепа, то эти изменения наблюдаются и при других формах наследственных гемолитических анемий. Понижение осмотической резистентности эритроцитов и повышение аутогемолиза, корригируемое глюкозой, могут встречаться при аутоиммунных гемолитических анемиях и наследственных гемолитических анемиях, обусловленных недостатком ферментов эритроцитов.
Тампонада сердца. Симптомы, причины и лечение Тампонада сердца
Лечение При наследственном микросфероцитозе, протекающем с частыми и выраженными гемолитическими кризами, наиболее эффективна спленэктомия, приводящая к клиническому выздоровлению; хотя микроцитоз и сфероцитоз остаются, но степень гемолиза значительно уменьшается. При компенсированном течении болезни, особенно у детей раннего и младшего возраста, целесообразно воздерживаться от удаления селезенки.
При наличии тяжело протекающей желчнокаменной болезни наряду со спленэктомией решается вопрос о показаниях к холецистэктомии или к вскрытию и дренированию общего желчного протока. Из гемотерапевтических средств используют трансфузии отмытых или размороженных эритроцитов, при возникновении тромбозов назначаются антикоагулянты.
Прогноз благоприятный, однако возможны летальные исходы (инфекции, тромбозы, реже — тяжелые гемолитические кризы).
Лечение аутоиммунной гемолитической анемии
Первой линией терапии тепловой аутоиммунной гемолитической анемии являются глюкокортикостероиды. Высокодозная монотерапия преднизолоном может назначаться в течение 3-6 недель с постепенным снижением дозы или отменой в дальнейшем. Однако из-за сильно выраженных побочных эффектов такого лечения все чаще используют краткосрочную пульс-терапию метилпреднизолоном или дексаметазоном. Примерно треть пациентов достигают ремиссии, остальным же необходима поддерживающая терапия ГКС.
При неэффективности стероидной терапии рассматривается возможность проведения спленэктомии (хирургическое удаление селезенки), биологической терапии (ритуксимаб) или иммуносупрессивной терапии (циклоспорин, азатиоприн и др.).
Прогноз зависит от первопричины заболевания, своевременно начатого и правильно подобранного лечения. Благоприятный прогноз (достижение ремиссии, длительная ремиссия) полностью связан с положительным терапевтическим ответом у пациента и отсутствием осложнений.
Пациентам с холодовой аутоиммунной гемолитической анемией рекомендуется избегать триггеров (холода, в том числе инфузий холодных растворов), а также пройти лечение основного заболевания (например, лимфомы), если с ним связано развитие х-АИГА. Терапия первой линии при х-АИГА — ритуксимаб. ГКС не является терапией выбора из-за низкого терапевтического ответа у пациентов. Также неэффективна и спленэктомия. В тяжелых случаях рекомендован плазмоферез.
Анемия. Кровь и бескровие
Оксигенация, аноксия, гипоксия
Органы внешнего дыхания, – дыхательная мускулатура, воздухоносные пути и легкие со своей газообменной паренхимой, – в норме обеспечивают бесперебойное поступление в организм кислородсодержащей газовой смеси (которую мы привыкли называть воздухом) и обратный выброс в атмосферу отработанной ее порции, для дыхания уже не пригодной. Это, так сказать, механическая часть процесса оксигенации, – насыщения крови и, затем, тканей кислородом.
С конечными, самыми тонкими ответвлениями бронхиального древа, – бронхиолами, – сопряжены т.н. легочные ацинусы, каждый из которых представляет собой гроздь альвеолярных ходов и мешочков. В свою очередь, стенка каждого мешочка образована множеством единичных микроскопических пузырьков-альвеол, через мембраны которых, собственно, и осуществляется диффузия кислорода в кровь, одновременно с ее очищением от углекислого газа.
Кислород для нас, аэробов – основа существования, топливо; углекислота – выхлопной газ. Можно возразить: а как же, мол, пища и вода, а как же продукты их переработки?…
Одним воздухом, и то правда, сыт не будешь. Но до пищи и воды дело попросту не дойдет, если вы попробуете пообедать в вакууме. В печке может быть сколько угодно дров, но без огня вы не согреетесь. Огня же без кислорода, как известно, не бывает; горение – это не что иное, как окислительно-восстановительная реакция с интенсивным выделением тепла. Только что вы прошли краткий курс катаболизма аэробных живых организмов.
Рассмотрение конкретных окислительно-восстановительных каскадов (начиная со знаменитого цикла Кребса, или цикла трикарбоновых кислот), обеспечивающих жизнедеятельность организма энергией, здесь вполне можно опустить: слишком сложно, долго, да и не важно в данном контексте. Важно то, что кислород для человека, – как электричество для компьютера. Это энергоноситель, в отсутствие которого останавливается и отключается буквально всё, а в нашем случае еще и всё погибает, поскольку сохраняться на диске мы пока не научились.
Встроенного аккумулятора человеческому организму хватает очень ненадолго. При абсолютной аноксии, т.е. полном отсутствии притока кислорода к тканям (например, в безвоздушном пространстве, при странгуляционной асфиксии или обтурации верхних дыхательных путей инородным телом) мучительная смерть наступает через несколько минут, и еще через несколько минут начинают необратимо отмирать наиболее чувствительные к аноксии ткани – в первую очередь, кора головного мозга.
Мы понимаем, что этот вариант является предельным, фатальным, – хотя и он, при всем трагизме, отнюдь не уникален в нашем несовершенном мире: летальность острой дыхательной недостаточности составляет примерно 35-40% (лет двести назад этот показатель практически не отличался от стопроцентного). Гораздо чаще встречается более или менее выраженная гипоксия, частичный «недобор» кислорода тканями. Человек об этом зачастую даже не знает, продолжая, например, курить табачные палочки. Но это до поры, до первой вынужденной остановки на лестнице, по которой раньше мы взлетали на пятый этаж бегом.
Если сложное электронное устройство работает «от розетки», а напряжение в сети по каким-то причинам постепенно снижается, то с определенного момента электроника не просто начинает сбоить, – она может самопроизвольно отключиться и/или серьезно повредиться.
Примерно то же самое происходит с тканями в условиях хронической гипоксии, нехватки кислорода, недостаточности тканевого дыхания. Но отчего возникает сама гипоксия?