Кратко о методе лечения
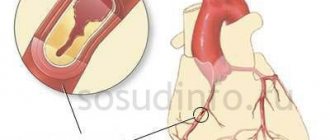
Эндоваскулярное лечение аневризмы брюшной аорты (EVAR) — это минимально инвазивная альтернатива большой открытой операции при аневризме брюшной аорты при которой уменьшается риск операции, ускоряется срок реабилитации и повышается выживаемость при этом опасном заболевании. Эндоваскулярная операция — предполагает только маленькие разрезы на бедре, через который внутри аневризмы устанавливается искусственный сосуд, называемый стент-графтом. Стент-графт представляет собой металлическую сетку особой конструкции (стент), которая покрыта изнутри герметичной полимерной тканью (графт). Металлическая сетка фиксирует это устройство к стенкам аорты и подвздошных артерий, а полимерная ткань изолирует просвет искусственного сосуда от полости аневризмы. Таким образом, аневризматический мешок изолируется от потока крови, а риск продолжения роста и разрыва аневризмы после установки стент-графта значительно уменьшается. Операция проводится без использования общего наркоза и не сопровождается значительной кровопотерей. Установка стент-графта при аневризме аорты значительно безопаснее классической открытой операции.
Открытое хирургическое вмешательство при аневризме аорты
Операция выполняется под общим наркозом. Суть операции в удалении аневризматического расширения и замещении его синтетическим протезом. В большинстве случаев последствия операции благоприятные. Средний показатель серьёзных осложнений и летального исхода при открытых вмешательствах составляет от 2 до 5 %. Однако, может быть выше при вовлечении в аневризму почечных и/или подвздошных артерий, а также в силу имеющейся у пациента сопутствующей патологии.
Послеоперационное наблюдение в стационаре, как правило, составляет от 10 до 14 дней. Реабилитация в раннем послеоперационном периоде занимает около 1-2 месяцев.
Подробную информацию можно найти на странице посвящённой открытому хирургическому вмешательству.
Преимущества лечения в ИСЦ
Инновационный сосудистый центр всегда стремится внедрять в свою практику самые передовые технологии сосудистой хирургии. Учитывая, что эндопротезирование является более безопасной альтернативой открытой операции при аневризме, мы с 2015 года практически заменили этим вмешательством операции резекции аневризмы. В своей практике мы используем лучшие стент-графты западных производителей, которые подбираются индивидуально под каждого пациента. Наши специалисты успешно выполняют операции эндопротезирования при самых сложных формах аневризм брюшной аорты.
Показания и противопоказания к методу лечения
Показания
- Стандартная процедура эндопротезирования подходит для аневризмы, которая начинается на 2-3 сантиметра ниже устьев почечных артерий, то есть имеет шейку для надежного крепления эндопротеза не допускающую протечку крови вокруг эндопротеза -«эндолика».
- Операция показана тогда, когда аневризма достигает достаточно большого диаметра (обычно более 5 см), так что риск осложнения (разрыва или тромбоза) превышает риск операции.
- Установка стент-графта в аневризму аорты так же проводится при быстром росте аневризмы (диаметр по УЗИ увеличивается более чем на 0,5 см в год)
- При эмболиях (переносе тромбов кровотоком из аневризматического мешка в артерии на ногах).
- Аневризмы аорты, которые вызывают боли животе, что может свидетельствовать о готовящемся разрыве.
При отборе пациентов на эндопротезирование аорты мы исходим из оценки риска открытой операции. Исследования, которые сравнивают EVAR с открытой операцией, продемонстрировали меньшее количество ранних осложнений при использовании эндоваскулярного подхода, более низкий уровень смертности в целом. Эндоваскулярное лечение требует более тщательного наблюдения, а иногда и дополнительных вмешательств при выявлении различных подтеканий. Если операция планируется у молодых пациентов с хорошим общим здоровьем, то предпочтительнее открытая операция. У пожилых больных эндоваскулярная операция является методом выбора, так как летальность после открытой операции превышает у них 10%. По мере развития технологии изготовления стент-графтов показания к открытым операциям становятся все реже.
Установка стент-графта при разрыве аневризмы брюшной аорты дает значительно больше шансов на выживание по сравнению с экстренной открытой операцией, так же как и помогает выжить пациентам с расслоением грудной и брюшной аорты, если выполнена своевременно.
Противопоказания
Анатомически непригодное строение аневризмы аорты для эндопротезирования. Чаще всего это отсутствие или очень короткий отрезок нормальной брюшной аорты ниже почечных артерий (отсутствие «шейки» аневризмы). В этом случае нет возможности хорошо закрепить верхний участок стент-графта для избежания подтеканий. Однако сейчас предложены к использованию стент-графты с боковыми ветвями для почечных артерий, которые позволяют размещать стент-графт выше, восстанавливая поток в почечные артерии.
Относительными противопоказаниями являются малый диаметр или аневризмы подвздошных артерий, выраженный кальциноз и окклюзии бедренных артерий, однако современные стент-графты и возможности гибридной (открытой и эндоваскулярной совместно) хирургии позволяют решать эти проблемы.
Осложнения при операции на аорте
Открытые операции имеют больший риск ранних послеоперационных осложнений и смертности, чем эндоваскулярная установка стент-графта в аорту. Летальность после открытых операций составляет около 5%, в то время как после эндопротезирования 0,5%.
Другие возможные осложнения после резекции аневризмы аорты:
- Острая почечная недостаточность
- Инсульт спинного мозга с параличом ног
- Высокая перемежающаяся хромота (боль в ягодицах при ходьбе) хромота
- Ишемия толстой кишки
- Эмболия нижних конечностей с острой ишемией
- Кровотечение из места операции и геморрагический шок
- Нагноение сосудистого протеза
Эти осложнения встречаются достаточно редко. В нашей клинике наблюдались единичные случаи подобных осложнений.
Подготовка к лечению
Для определения показаний к эндоваскулярному лечению аневризмы аорты пациенты должны быть должным образом обследованы.
- Общеклинические анализы крови и мочи
- Биохимический анализ крови (мочевина и креатинин)
- Анализы крови на инфекции (гепатит, вич, сифилис)
- УЗИ брюшной полости и аорты
- УЗИ сонных артерий
- ЭХО кардиография
- Исследование желудка (гастроскопию) для предупреждения кровотечения из язвы.
- Мультиспиральная компьютерная томография (МСКТ) аорты и артерий нижних конечностей. Это исследование должно показать грудную и брюшную аорту с ветвями и артерии нижних конечностей. На основании МСКТ планируется операция и выбирается размер и вид стент-графта.
Диагностика
Очень часто пациенты не предъявляют никаких жалоб. Но если симптомы появляются, то они носят неспецифичный характер. Среди наиболее распространенных симптомов следует отметить боль в брюшной полости, спине или в области грудной клетки. Пациенты описывают эту боль по-разному: одни чувствуют умеренную или сильную боль или болезненные ощущения в средней или верхней части живота, или же в пояснице, другие — ощущают саму аневризму, как бьющуюся и пульсирующую массу в брюшной полости. Но, как отмечалось, многие могут не ощущать никаких симптомов. Иногда аневризма брюшной аорты
может быть обнаружена во время обычного физического осмотра. При пальпации живота врач может обнаружить выпуклость или пульсацию в брюшной полости. Но наиболее часто аневризму выявляют во время таких медицинских исследований, как ультразвуковое исследование (УЗИ) брюшной полости или компьютерная томография (КТ). Размер и локализация аневризмы брюшной аорты, а также общее состояние пациента помогают правильно выбрать метод лечения. Если аневризма небольшая, врач может рекомендовать динамическое наблюдение (регулярные осмотры с целью наблюдения за ее размерами). Аневризма больших размеров или быстро увеличивающаяся аневризма имеет высокую вероятность разрыва и требует лечения.
Обезболивание при лечении
Для доступа к аорте обычно используются бедренные артерии, которые выделяются открыто через небольшие разрезы. Для обезболивания используется эпидуральная анестезия (введение катетера в область позвоночника, через который подается раствор для анестезии). В обязательном порядке проводится полноценное мониторирование пациента. Наготове находится респираторно-дыхательная аппаратура для искусственной вентиляции легких. Для внутривенных инфузий используется подключичный венозный катетер.
Как проходит метод лечения
Операция проводится в стерильных условиях, под контролем рентгеновской ангиографической установки, совместной бригадой в составе сосудистого и эндоваскулярного хирурга.
Доступ к бедренным артериям пациента осуществляет сосудистый хирург с использованием 4-5 сантиметровых разрезов. Бедренные артерии выделяются и берутся на держалки, позволяющие манипулировать с ними.
Через плечевую или лучевую артерию на руке проводится диагностический катетер в брюшную аорту для ангиографической оценки аневризмы, состояния и места отхождения почечных артерий. Это очень важно, поскольку закрывать почечные артерии стент-графтом нельзя, так как разовьется почечная недостаточность.
Эндопротез надежно закрывает полость аневризмы изнутри, проводя кровь без контакта с аневризматическим мешком, что со временем приводит к тромбозу аневризмы и уменьшению ее размеров.
После открытия бедренных артерий в них устанавливаются специальные трубочки (интрадьюссеры) через которые в аорту выше аневризмы проводятся специальные проводники. Затем по проводнику через небольшой разрез в правой бедренной артерии проводится основное тело стент-графта. Это основной протез размещаемый в аорте и правая ножка, которая должна располагаться в правой подвздошной артерии. Далее проводится тщательное позиционирование основного тела эндопротеза в области «шейки» аневризмы, чтобы при раскрытии в области почечных артерий размещалась только специальная корона эндопротеза, но не закрытый участок стент-графта. С помощью диагностического катетера размещенного выше аневризмы проводится контроль.
После раскрытия основной бранши и правой ножки проводится проводник в отверстие, предназначенное для второй ветви и выводится за пределы стент-графта. По этому проводнику проводится левая ножка стент-графта для размещения в левой подвздошной артерии. После раскрытия этой ножки конструкция является собранной.
Для плотного прилегания стентграфта к стенкам аорты его дополнительно распрямляют специальными баллонами. После этого выполняется контрольная ангиография, которая должна показать равномерное заполнение эндопротеза, отсутствие подтекания контраста помимо протеза и нормальную проходимость артерий ниже протезов.
После этого устройства доставки стент-графта извлекаются из артерий. Отверстия в них ушиваются сосудистым швом. В рану вводятся контрольные дренажи. Кровоток в нижних конечностях и почках контролируется с помощью ангиографии из верхнего катетера.
Введение
По данным L. Bickerstaff и соавт. [1], ежегодная частота выявления аневризм грудной аорты составляет 5,9 на 100 тыс. населения. Более 60% из них являются аневризмами восходящего отдела и дуги аорты.
Впервые успешное протезирование дуги аорты c использованием искусственного кровообращения было выполнено M. DeBakey и D. Cooley [2]. Важными вехами в эволюции операций на дуге аорты явились применение антеградной перфузии головного мозга (DeBakey, 1957) [3], разработка метода длительной остановки кровообращения (циркуляторный арест) в условиях глубокой гипотермии (Griepp, 1975) [4], использование ретроградной перфузии головного мозга (Mills, Ochsner, 1980) [5], внедрение операции «хобот слона» (Borst, 1983) [6] и операции «замороженный хобот слона» (2003) [7].
Показания к хирургическому вмешательству на восходящей аорте и дуге аорты сегодня четко определены. Отработаны различные технические аспекты выполнения операций. Тем не менее остается не до конца решенной проблема защиты головного мозга и внутренних органов от ишемических повреждений [8, 9].
Для защиты головного мозга в настоящее время принято использование таких технологий, как глубокая гипотермия с остановкой кровообращения (ГЦА), селективная антеградная перфузия головного мозга с умеренной гипотермией, ретроградная перфузия головного мозга, антеградная нормотермическая перфузия головного мозга по принципу «теплая голова — холодное тело» [9]. Все перечисленные методы предполагают временную остановку кровообращения (циркуляторный арест).
Посредством антеградной (моно- и бигемисферальной) перфузии головного мозга при умеренной гипотермии возможно нивелировать отрицательные эффекты, связанные с глубокой гипотермией, и уменьшить время реконструкции дистальной части дуги аорты [10].
В 2011 г. G. Matalanis и соавт. [11] была описана методика branch-first с канюляцией бедренных сосудов, унилатеральной перфузией головного мозга и пережатием нисходящей аорты. Были прооперированы 30 пациентов. Погиб 1 больной. Неврологические осложнения развились у 2 пациентов.
Следует констатировать, что преимущество какого-либо метода защиты головного мозга сегодня не доказано. Именно поэтому клинические центры ориентируются прежде всего на собственный опыт [10, 12, 13].
Клиническое наблюдение
Больная Е., 67 лет, поступила в отделение в плановом порядке 12.08.2018 с жалобами на периодическую боль за грудиной, чувство перебоев в работе сердца, подъем АД до 140/90 мм рт.ст., общую слабость. Считает себя больной в течение 6 мес, когда при обследовании по поводу заболевания пищевода выполнялась компьютерная томография (КТ). Было выявлено расширение восходящего отдела аорты до 47 мм, наблюдалась у сердечно-сосудистого хирурга. Через 6 мес выполнена контрольная КТ-ангиография, было отмечено увеличение диаметра восходящей аорты до 52 мм с признаками расслоения и флотации интимы в просвете восходящей и дуги аорты. Расстояние от грудины до восходящей аорты — не более 5 мм (рис. 1, 2). При поступлении установлен диагноз: «Аневризма восходящего отдела и дуги аорты. Расслоение аорты А типа по Stanford. Недостаточность аортального клапана I ст. Атеросклероз аорты и ее ветвей. Стеноз сонных артерий справа. Артериальная гипертензия II ст., 2 ст., риск 4. Состояние после острого нарушения мозгового кровообращения в правой гемисфере мозжечка по геморрагическому типу (2011). Эрозивный гастрит. Полип пищевода».
Рис. 1. 3D-реконструкция восходящей и дуги аорты до операции.
Рис. 2. Дуга аорты с хронической диссекцией А типа по Stanford (КТ-ангиография).
Для исключения патологии коронарных артерий выполнена коронарная ангиография, значимого коронарного поражения не выявлено.
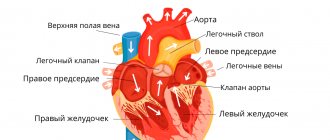
Больная оперирована 14.08.2018. Для исключения повреждения аневризмы при стернотомии принято решение о подключении аппарата искусственного кровообращения (АИК) до основного доступа. Выделена подключичная артерия (ПклА) справа. Сформирован анастомоз между правой ПклА и дакроновым протезом 8 мм. Установлена артериальная канюля через синтетический протез. Подключение АИК по схеме «бедренная вена — бедренная артерия + подключичная артерия» (рис. 3). Выполнена полная продольная стернотомия.
Рис. 3. Схема подключения АИК «бедренная вена — бедренная артерия + правая подключичная артерия».
Определяется выраженный спаечный процесс в полости перикарда, выполнен кардиолиз. Отмечается аневризма восходящей аорты с переходом на дугу диаметром до 6 см.
Из стернотомного доступа выделена восходящая аорта, дуга аорты, брахиоцефальный ствол (БЦС), левая общая сонная артерия (ОСА), левая ПклА. Для адекватного венозного забора через ушко правого предсердия установлена двухпросветная венозная канюля. Переключение ИК по схеме «правое предсердие — бедренная артерия + правая подключичная артерия» (моногемисферальная перфузия). Аорта пережата дистальнее левой ПклА. Пережаты БЦС, левая ОСА, левая ПклА. Вскрыт просвет восходящей и дуги аорты до левой ОСА. Фармакохолодовая кардиоплегия через устья коронарных артерий (рис. 4).
Рис. 4. Схема ИК «правое предсердие — бедренная артерия + правая подключичная артерия» с антеградной моногемисферальной перфузией головного мозга.
После пережатия прецеребральных артерий было отмечено снижение уровня церебральной оксигенации левой гемисферы головного мозга с 60 до 42%. Объемный кровоток унилатеральной перфузии при этом составлял 500 мл/мин.
Через дополнительный отвод артериальной канюли с использованием катетера Фолея налажена перфузия левой ОСА. Схема ИК: «правое предсердие — бедренная артерия + правая подключичная артерия + левая общая сонная артерия» (бигемисферальная перфузия) (рис. 5).
Рис. 5. Схема ИК «правое предсердие — бедренная артерия + правая подключичная артерия + левая общая сонная артерия» с антеградной бигемисферальной перфузией головного мозга.
После подключения показатели газообмена головного мозга выровнялись. При бигемисферальной перфузии объемный кровоток увеличили до 800 мл/мин.
При ревизии отмечено распространение диссекции в аневризме от синотубулярного гребня до левой ОСА по передней стенке аорты. Синусы Вальсальвы не расширены, аортальный клапан состоятелен. В ложном канале – тромботические массы. Стенки аневризмы иссечены вместе с тромбами. Сформирован дистальный скошенный анастомоз между аортой и синтетическим протезом по типу hemiarch с использованием фетровой прокладки. Снят зажим с БЦС и левой ПклА, удален перфузионный катетер из левой ОСА. Профилактика воздушной эмболии. Аортальный зажим переложен на протез. Сформирован проксимальный анастомоз между аортой на уровне синотубулярного гребня и синтетическим протезом с использованием фетровой прокладки. Профилактика воздушной эмболии. Снят зажим с аорты (длительность пережатия — 58 мин). ИК остановлено на адекватной гемодинамике (время ИК — 103 мин). Синусовый ритм восстановился самостоятельно. Деканюляция. Подшит электрод к передней стенке правого желудочка. Послойное ушивание ран. Асептические повязки.
Длительность операции составила 330 мин. На протяжении всего вмешательства выполнялась непрямая церебральная оксиметрия. Систолическое АД до начала ИК поддерживалось на уровне 100—110 мм рт.ст. Перфузионное давление во время ИК составляло от 70 до 100 мм рт.ст. на фоне умеренной инотропной и вазопрессорной поддержки.
В течение всей операции сохранялся отток мочи по уретральному катетеру. Объем кровопотери — 400 мл. Объем трансфузии препаратов крови в интра- и раннем послеоперационном периодах составил 500 мл эритроцитарной взвеси, 1800 мл свежезамороженной плазмы и 400 мл тромбоконцентрата. После операции больная была переведена в отделение реанимации и интенсивной терапии. Через 12 ч экстубирована, гемодинамика оставалась стабильной. На 3 сутки пациентка переведена в отделение сосудистой хирургии. В послеоперационном периоде отмечалось нарушение функции правой верхней конечности вследствие травмы плечевого сплетения при канюляции правой подключичной артерии. Лечебные мероприятия сопровождались полным регрессом неврологической симптоматики. В остальном послеоперационный период протекал без особенностей. Заживление ран первичным натяжением (рис. 6). Пациентка выписана на 12 сутки после выполнения контрольной КТ (рис. 7,
Рис. 6. Доступы к правой подключичной артерии, восходящей аорте и брахиоцефальным сосудам.
Рис. 7. 3D-реконструкция восходящей и дуги аорты после операции.
Рис. 8. Аксиальный срез на уровне дуги аорты после операции (КТ-ангиография).
Возможные осложнения при лечении
Осложнения вмешательства можно разделить на те, которые относятся к ходу самой операции или к конструкции и расположению эндопротеза. Так инфаркт миокарда, возникающий сразу после вмешательства, является осложнением операции, а не протеза. Напротив, развитие подтеканий вдоль стент-графта является осложнением связанным с эндопротезом.
Долговечность результатов эндоваскулярного лечения аневризмы аорты зависит от тщательного наблюдения за состоянием протезированного участка аорты и принятия мер при выявлении осложнений.
Одна из основных причин осложнений при EVAR заключается в том, что контакт между проксимальной шейкой аневризмы и стент-графтом является неплотным, вследствие сложной анатомии шейки, несоответствия диаметра стент-графта размерам шейки. Чаще всего это связано с анатомическими особенностями шейки и можно рассчитывать, что с появлением специальных окончатых или ветвистых стент-графтов это осложнение уйдет в прошлое. В настоящее время использование таких стент-графтов возможно, но их установка является более сложной, а сами устройства значительно дороже стандартных. При неплотном контакте аневризма полностью не выключается и может дальше расти и даже подвергнуться разрыву. Поэтому подтекания (эндолики) необходимо ликвидировать, сразу после их появления.
Осложнения, связанные с операцией
- Расслоение аорты
- Почечная недостаточность, связанная с контрастом
- Тромбоэмболии — перенос тромбов с током крови в низлежащие артерии ног.
- Острая непроходимость артерий кишечника — мезентериальный тромбоз
- Кровотечения в области доступов в паховой области
- Инфекция в области доступов
- Инфаркт миокарда, нарушения сердечного ритма, дыхательная недостаточность.
Осложнения связанные с стент-графтом
- Миграция эндопротеза
- Разрыв аневризмы
- Тромбоз стент-графта
- Подтекания (эндолики) в полость аневризмы
Существует 5 типов подтеканий:
Тип I — Протекание в верхем и нижнем местах крепления стент-графта ( в области почечных и подвздошных артерий). Последний практически свободно лежит в аорте и аневризме не выполняя своей защитной функции для аневризмы. Тип II — Ретроградный кровоток в полость аневризматического мешка из ветвей аорты таких как поясничные и нижняя брыжеечная артерия. Такой тип подтеканий возникает чаще всего и несет меньше всего рисков. Немедленного лечения не требуется, так как полость может затромбироваться и эндолик спонтанно исчезнет. Тип III — протекание между перекрывающимися частями стента (например между основным телом стент-графта и левой ножкой) или разрыв покрытия эндопротеза. Тип IV — протекание через стенку стент-графта из-за пористости материала покрытия. С развитием технологии изготовления стент-графтов такой вид эндоликов исчезает. Тип V — расширение аневризматического мешка без выявленных подтеканий. Спонтанный рост аневризмы, причины которого не ясны.
Ход операции резекции аневризмы аорты
- Хирургический доступ
Во время предоперационного обследования принимается решение о хирургическом доступе. Чаще всего выполняется три доступа. Два из них в паховой области на бедре, для выделения общих бедренных артерий, один доступ — срединная лапаротомия (разрез посередине живота) или доступ на левом боку. При высоких аневризмах верхний доступ может быть продлён на грудную клетку. Это вмешательство — торакофренолюмботомия.
- Смысл операции
После выделения аневризматического мешка проводится пережатие брюшной аорты. Время перекрытия кровотока надо обязательно сокращать. Для этого, до установки зажима на аорту выполняется хорошее выделение аневризмы и всех артериальных ветвей до бифуркации аорты на подвздошные артерии. Когда наложены сосудистые зажимы производится вскрытие просвета аневризмы, удаление тромботических сгустков из полости аневризмы и остановка кровотечения из ветвей, впадающих в аневризму.
Открытое вмешательство заключается в замене расширенного участка аорты синтетическим сосудистым протезом. Последний вшивается в верхний участок аорты (выше аневризмы), затем ветви протеза проводятся на бедренные артерии и пришиваются к ним. После этого протез укрывается стенками аневризматического мешка. Основной проблемой является выделение аневризматического мешка и ветвей исходящих из него. Делать это надо достаточно быстро, если эти ветви проходимы, так как длительное пережатие может вызвать нарушение питания кишечника или спинного мозга.
После соединения аорты с бедренными артериями надо решить вопрос о необходимости трансплантации нижней брыжеечной артерии. Эта артерия кровоснабжает толстую кишку, и иногда её перевязка может привести к нарушению кишечного кровоснабжения. Для принятия решения необходимо оценить кровоток по этой артерии. Если после снятия с неё зажима идёт хороший обратный кровоток, то артерию можно не пришивать к сосудистому протезу, если же она проходима, но кровоток очень слабый, значит обходные пути неразвиты и артерии необходимо реплантировать в сосудистый протез.
После завершения сосудистого этапа операции в забрюшинное пространство и в область доступов на бёдрах устанавливаются трубчатые дренажи, а раны послойно ушиваются.
Средняя продолжительность операции по поводу аневризмы аорты составляет 3 часа. Средний объём кровопотери около одного литра. Кровопотеря восполняется донорской кровью, плазмой и солевыми растворами.
Прогноз после метода лечения
Если операция эндопротезирования выполнена корректно и с хорошим непосредственным результатом, то риск разрыва аневризмы уменьшается во много раз и через год после этой процедуры сравнивается с результатами открытой операции резекции аневризмы. Через 2-3 дня после операции пациент может быть выписан домой. С учетом низкой послеоперационной летальности после эндоваскулярного метода лечения риск эндопротезирования значительно меньше, чем риск открытой операции. Поэтому в западных странах эндоваскулярным методом оперируется более 80% больных с аневризмой брюшной аорты. Однако для стойкого положительного результата пациент должен находиться под динамическим наблюдением.
На порядок лучше: эндопротезирование аневризмы аорты
Эндопротезирование аневризмы аорты, как отмечают сосудистые хирурги, это современное направление лечения больных с этой с этой тяжелой патологией. В целом, это и явилось поводом к написанию данной статьи.
В Межрегиональном клинико-диагностическом центре с 2007 года с высокой эффективностью проводятся данные операции. Неделю назад был проведен мастер-класс, посвященный установлению стентграфтов нового поколения. Об этом в интервью с заведующим отделением сосудистой хирургии, заведующим курсом сердечно-сосудистой хирургии КГМУ, доктором медицинских наук, профессором Игорем Михайловичем Игнатьевым.
— При участии М.И. Генералова (федеральный диагностический центр г. Санкт-Петербург) и Лучникова В.М. (институт им. Вишневского г. Москва) был проведен мастер-класс, на котором мы прооперировали четырех пациентов с аневризмой брюшной аорты, с использованием стентграфтов нового поколения.
— Какова суть методики?
— Пациентов с аневризмами — патологическим расширением аорты, которое может привести к разрыву аневризмы с летальным исходом достаточно много. Эта категория больных нуждается в эндопротезировании аорты, то есть, изнутри, через небольшие доступы, малотравматично «вставляется» в аорту эндопротез, который «раскрывается» и блокирует аневризму. Операция малоинвазивная и больными, как правило, переносится хорошо.
— Есть ли аналог эндопротезированию для устранения аневризмы?
— Открытые операции. Но здесь существуют некоторые нюансы. У большинства наших пациентов часто встречается тяжелая сопутствующая патология- патология сердца, почек, легких и других органов. Поэтому такие больные обычно не переносят открытое, оперативное вмешательство, представляющий высокий риск.
— А если говорить о новых протезах, которые были продемонстрированы на мастер-классе?
— Это протезы нового поколения, которые достаточно хорошо моделируются, позиционируются в просвете аорты. Мы установили протезы в брюшную аорту производства Англии. Они существенно модернизированы и благодаря этому позволяют выполнить более сложные варианты эндопротезирования. Эндопротез по своим размерам и характеристикам подбирается индивидуально для каждого больного.
— В ходе мастер-класса были прооперированы четыре пациента. Расскажите, пожалуйста, о результатах.
— Все четыре пациента поступили с достаточно тяжелой формой аневризмы брюшной аорты. Одна операция была технически очень сложной – гибридная, в ходе которой помимо протезирования аорты выполнялся сосудистый этап – перекрестное шунтирование.
Подобные хирургические вмешательства выполняются двумя бригадами – сосудистыми хирургами и рентгенхирургами.
— То есть, можно сказать, вы работаете в симбиозе…
— Да. Эндоваскулярные операции достаточно сложные в техническом исполнении и требуют определенного мастерства и опыта.
— С какой целью был организован мастер-класс?
— Наши хирурги владеют данной методикой, и опыт, в принципе, уже накоплен не малый, но поскольку применяются эндопротезы нового поколения, мы должны были познакомиться с определенными их характеристиками и особенностями. М.И. Генералов (федеральный диагностический центр г. Санкт-Петербург) обладает хорошим опытом по установке новых протезов и готов был им с нами поделиться.
— Сколько подобных операций планируется сделать в этом году?
— Около десяти.
— Ваши коллеги из РКБ делают подобные операции, или вы в этом отношении имеете прерогативу?
— Тоже делают, но, насколько мне известно, в меньшем объеме, чем в Межрегиональном клинико-диагностическом центре. Подобные хирургические вмешательства по сей день сохраняют уникальность в клиниках России, потому что их количество к сожалению не велико. С каждым годом темпы по данному оперативному вмешательству наращиваются. Если сравнить российскую клинику и европейскую, или США, то в год такого уровня операции производятся по нескольку сот. Именно поэтому данное направление должно развиваться и у нас.
— Много ли пациентов с данной патологией?
— Достаточно много и она трудно диагностируются. В некоторых случаях смерть больного наступает до постановки диагноза «аневризма аорты».
— Каким образом можно диагностировать пациентов, чтобы не допустить катастрофы и вовремя провести эндоваскулярное вмешательство?
-Мы работаем в районах республики, выезжаем и диагностируем. Самый доступный диагностический метод – это ультразвуковое исследование. С его помощью можно достаточно четко увидеть расширение аорты.
— А симптомы какие-либо имеются? Что может сделать врач общей практики?
— К сожалению, в самом начале заболевание протекает бессимптомно. Это еще в большей степени усложняет диагностику. Приведу пример. Один из наших пациентов имел аневризму диаметром около 15 см., показывался врачам-терапевтам, но никто не догадался пропальпировать живот. В фонендоскопе аневризма «шумит», поэтому ее можно и нащупать, и увидеть и услышать, главное – вовремя заподозрить, обнаружить и провести оперативное вмешательство.
— Какие возможные осложнения встречаются в ходе операции и в послеоперационном течении? Какова их вероятность?
— Осложнения могут быть при любом, даже самом незначительном вмешательстве, но если технически все сделано грамотно, риск возникновения осложнений минимален. Немаловажным является опыт самого сосудистого хирурга, чем он выше, тем риск каких-либо неприятностей меньше. Фатальных каких-то вещей при проведении эндоваскулярного вмешательства не наблюдается, но некоторые нюансы в виде, например, повторных операций, иногда встречаются. Но все эти ситуации исправимы.
— Говоря об опыте, вы не могли бы рассказать, где проходили обучение специалисты вашего отделения?
— В ведущих клиниках США и Германии.
— Каковы преимущества эндоваскулярного вмешательства перед открытыми хирургическими вмешательствами, которые выполнялись ранее при данной патологии?
— Эндоваскулярное вмешательство менее травматично, легче переноситься пациентами, срок послеоперационной реабилитации и восстановления меньше и, что самое важное летальность значительно ниже, чем при открытом вмешательстве.
— Какая проводится медикаментозная терапия после данного оперативного вмешательства?
— Пациентам назначаются аспиринсодержащие препараты, которые работают на улучшение реологических свойств крови.
— Каким образом можно профилактировать аневризму аорты?
— Природа возникновения аневризмы аорты по сей день вопрос дискутабельный. С одной стороны, есть мнение, что это врожденная патология матрикса сосудистой стенки, с другой – немаловажную роль играет и атеросклероз. Поэтому говоря о профилактике своим пациентам, необходимо упомянуть о профилактических мероприятиях, направленных на предотвращение развития атеросклероза.
Екатерина Лобанова
Программа наблюдения после метода лечения
На следующий день после операции проводится осмотр сосудистым хирургом, перевязка ран в паховых областях, удаление дренажей. Для оценки эффективности операции проводится УЗИ брюшной аорты и артерий нижних конечностей.
Через каждые 3 месяца после операции необходимо выполнять МСКТ аорты, для выявления возможных подтеканий. Такие исследования проводятся в течение первого года. Затем их нужно повторять ежегодно. При недоступности МСКТ возможно проведение УЗИ брюшной аорты.
При выявлении подтеканий пациент госпитализируется в клинику для выполнения коррекции, так как возникнув, эти осложнения не проходят самостоятельно, а требуют вмешательства для коррекции и профилактики разрыва аневризмы.
Результаты
Интраоперационная, госпитальная и 30-дневная летальность отсутствовала после первого и второго этапов ретроградного протезирования. У 1 пациента после протезирования ТАА на 7-е послеоперационные сутки развилось ретроградное расслоение. Пациенту в экстренном порядке выполнена реконструкция ВОА и ее дуги. Интраоперационные данные и спектр послеоперационных осложнений представлены в табл. 3.
Таблица 3. Интраоперационные данные и послеоперационные осложнения
Госпитальная летальность после второго этапа антеградного протезирования аорты составила 5% (n
=1). У данного пациента послеоперационный период осложнился полиорганной недостаточностью на фоне гипокоагуляционного кровотечения. Повторная торакотомия выполнена у 3 больных, ревизия забрюшинного пространства по поводу кровотечения — у 3. Дыхательная недостаточность, требующая продленной вентиляции легких (в течение 72 ч), развилась у 5 пациентов. Наложение трахеостомы потребовалось 1 пациенту. Острая почечная недостаточность, потребовавшая гемодиализа, развилась у 1 пациента. Случаи ОНМК и параплегии отсутствовали.
Интервал между операциями составил 7±2 мес, продолжительность госпитализации — 14±9 сут.
За период наблюдения не было ни одного летального исхода среди выписанных пациентов. При МСКТ аорты через 3 и 6 мес после операции затеков контрастного вещества ни у одного из пациентов не выявлено, протезированные сегменты без перегибов и деформаций, проходимы на всем протяжении. В одном случае выявлен стеноз левой почечной артерии без признаков нефросклероза. После стентирования проходимость артерии была восстановлена.