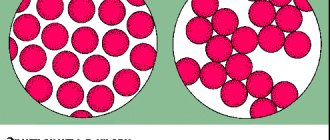
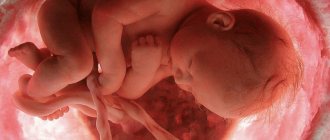
Историческая справка
Первая пересадка сердца произведена в 1964 году Джеймсом Харди. Больному досталось сердце шимпанзе. После этого удалось поддерживать жизнь пациента только полтора часа.
Значимой вехой в успешной трансплантологии считается пересадка человеческого сердца донора, проведенная в ЮАР в 1967 году Кристианом Бернардом. Донором была погибшая в ДТП молодая женщина 25 лет. А реципиентом — больной мужчина 55 лет, не имеющий шансов в дальнейшем лечении. Несмотря на мастерство хирурга, пациент скончался от двусторонней пневмонии спустя 18 суток.
Главной проблемой выживания считается степень отторжения донорского органа иммунной системой человека. В настоящее время оперативной техникой владеют многие профильные кардиологические центры.
История вопроса
Успехи трансплантологии связаны с развитием двух независимых сфер медицины: совершенствованием хирургической техники и методов анестезии с одной стороны, и достижениями иммунологии и фармакологии — с другой. Первое обеспечило удачное проведение операций, а второе — благополучное протекание послеоперационного периода.
Первые шаги
Еще в XVI веке итальянский хирург Гаспаро Тальякоцци после ряда неудачных экспериментов с пересадкой кожи от человека к человеку представил публике успешный результат аутотрансплантации (пересадки собственного органа реципиента, в данном случае — кожи). В 1596 году он описал свои наблюдения «силы и мощи индивидуальности» в труде «De Curtorum Chirurgia per Insitionem» (Замещающая хирургия с использованием пересадки).
Однако широкий интерес идея трансплантации органов вызвала лишь спустя 300 лет, когда хирурги массово приступили к практическим опытам. Вновь столкнувшись с проблемой отторжения, они обогатили медицину тремя важными выводами: межвидовые пересадки органов (ксенотрансплантации) всегда неуспешны; пересадки между представителями одного вида (аллогенетические трансплантации) в большинстве случаев тоже, причем повторные пересадки органов между одними и теми же донорами и реципиентами ускоряли отторжение; если между донором и реципиентом было кровное родство, вероятность благоприятного исхода операции значительно увеличивалась, причем пересадка собственных органов (аутотрансплантация) почти всегда были удачна.
Первая описанная в литературе успешная трансплантация датируется II веком нашей эры: индийский хирург Шушрата произвел пересадку кожи в ходе ринопластики.
А в III веке, если верить хроникам римской католической церкви, святые Дамиан и Косма пересадили потерявшему ногу от гангрены римскому дьякону Юстиниану конечность недавно умершего эфиопа.
Собачье сердце
В 1905 году в череде опытов по пересадке органов очередь дошла и до сердца. Первую трансплантацию сердца собаки-донора на сосуды шеи собаки-реципиента осуществили хирург, биолог и патофизиолог Алексис Каррель и физиолог Шарль Гатри, американцы французского происхождения. Донорское сердце проработало 2 часа.
В 1933 году американский физиолог Фрэнк Манн с коллегами повторил опыт Карреля и показал возможность функционирования гетеротопически (то есть размещенного в нетипичном месте) трансплантированного сердца собаки вплоть до 8 суток (собственное сердце собаки оставалось на месте и продолжало работать).
В ногу со временем шли и советские хирурги. Наиболее весомый вклад в экспериментальные основы трансплантации сердца в СССР внес Владимир Петрович Демихов. С 1946 по 1955 год он в нескольких сотнях экспериментов разработал 24 (!) варианта хирургической техники гетеротопической трансплантации сердца в грудную клетку. В некоторых опытах донорское сердце эффективно обеспечивало кровообращение собаки-реципиента в течение более чем 15 часов.
Борьба с ишемией
Самой явной проблемой, вставшей на пути хирургов, стала ишемия: в условиях недостаточного кровотока повреждались и ткани реципиента, и донорские сердца. Трансплантацию невозможно провести в сжатые сроки, поэтому хирурги и анестезиологи стали искать способы, позволяющие продлить время операции. Так были разработаны методы управляемой гипотермии и спроектированы аппараты искусственного кровообращения (ИК).
Управляемая гипотермия позволяет снизить кровопотерю, а также продлить время операции без повышения риска ишемизации тканей.
В 1953 году американские хирурги Уилфорд Нептун и Брайан Куксон с коллегами выполнили первую трансплантацию сердечно-легочного комплекса собаки в условиях глубокой гипотермии (во время операции в комнате поддерживалась температура порядка минус 4 °С).
В 1957 году американцы Уильям Вебб и Хизер Говард повторили этот эксперимент, подключив собаку-реципиента к аппарату ИК. Позднее они сообщили о пересадке в тех же условиях изолированного сердца. Они накладывали девять анастомозов между аортой, легочной артерией, легочной и полой венами. Правда, этот трансплантат профункционировал всего 7 часов.
К середине 60-х Норман Шумуэй и Ричард Лоуэр с коллегами из клиники при Стэнфордском университете разработали методику трансплантации сердца, которая используется по сей день: с использованием «локальной гипотермии» — местного охлаждения до 18–21 °С. С этого момента для успешного проведения операции осталось только одно препятствие — иммунологическое отторжение.
Причины отторжения
В 1952 году иммунологи Жан Доссе (Франция) и Барух Бенасерраф (США) вместе с генетиком Джорджем Снеллом (США) обнаружили, что важнейшие антигены, участвующие в отторжении трансплантата, – антигены главного комплекса гистосовместимости (HLA). За это открытие в 1980 году они были удостоены Нобелевской премии.
Существует порядка 150 вариантов антигенов HLA, и у каждого человека на мембранах клеток присутствует по шесть вариантов таких антигенов. Следовательно, возможно более триллиона их комбинаций – вероятность существования двух людей с одинаковыми комплексами HLA-антигенов близка к нулю, конечно, если они не однояйцевые близнецы. Идеально, если у донора и реципиента наблюдается несовпадение лишь одного антигена из шести. Операции проводят и в том случае, если не совпадают два, однако при этом увеличивается риск развития иммунологического отторжения.
На практике определение совместимости тканей — гистотипирование — осуществляется по лимфоцитам крови.
Со стороны «хозяина» основные эффекторы трансплантационного отторжения – это цитотоксические CD8 T-клетки и CD4 Т-клетки. Последние привлекают в зону отторжения трансплантата клетки воспаления (в том числе макрофаги). Распознание трансплантационных антигенов происходит либо непосредственно на клетках трансплантата, либо в ближайшей лимфоидной ткани.
Немалую роль в отторжении трансплантата могут сыграть и антитела в организме реципиента (например, появившиеся из-за предшествующего переливания цельной крови). Взаимодействуя с антигенами эндотелия сосудов, пронизывающих трансплантат, они инициируют систему комплемента и каскад реакций, приводящий к закупорке сосудов.
Иммуносупрессия
Первыми веществами, которые начали использовать для подавления иммунного ответа, стали кортикостероиды.
В 1948 году американский врач Филип Хенч, применив кортизон в лечении ревматоидного артрита, показал, что препарат обладает выраженным противовоспалительным действием. В 1952 году американский хирург Роджер Бэйкер с коллегами продемонстрировал, что кортизон может использоваться и для иммуносупрессии после трансплантации.
В 1962 году американцы Уиллард Гудвин и Мэтт Мимс впервые использовали азатиоприн — иммуносупрессивный препарат, обладающий наибольшей активностью в отношении Т-лимфоцитов, для предотвращения острого отторжения трансплантированной почки. Пациентам с пересаженным сердцем также планировалось назначать азатиоприн в сочетании с кортикостероидами.
Очередь человека
Человеку сердце было впервые пересажено в 1964 году. Джеймс Харди с коллегами трансплантировали сердце крупного шимпанзе, весившего более 43 кг, больному 68 лет с тяжелой формой ИБС в терминальной стадии прогрессирующей сердечной недостаточности. Вначале трансплантат работал удовлетворительно, однако через час после отключения аппарата ИК развилась острая сердечная недостаточность, обусловленная объемной перегрузкой трансплантата, и больной погиб.
Первая аллогенетическая трансплантация сердца человеку была проведена три года спустя в Кейптауне южноафриканским хирургом Кристианом Барнардом, прошедшим стажировку под руководством Нормана Шумуэя. Бригада доктора Барнарда пересадила сердце 25-летней девушки, погибшей в автомобильной аварии, 55-летнему диабетику, перенесшему три инфаркта и страдавшему от застойной сердечной недостаточности. Трансплантация прошла удачно, но на 18-е сутки после операции пациент умер от двусторонней пневмонии. Через месяц в этой же клинике была выполнена вторая трансплантация донорского сердца, после которой реципиент прожил полтора года, умерев от хронического отторжения.
В СССР первая успешная трансплантация сердца была осуществлена в 1987 году знаменитым врачом-трансплантологом академиком АМН СССР Валерием Ивановичем Шумаковым (1931–2008).
Успех первого клинического опыта увлек медицинское сообщество, и к решению задачи трансплантации сердца обратились хирурги всего мира. Однако большинство пациентов умирало вскоре после проведения операции, и интерес исследователей начал угасать: если в 1968 году было проведено 100 трансплантаций сердца, то в 1970 — всего 18. Главной причиной смерти оставалось отторжение пересаженных органов.
Лишь четверо из прооперированных в период с 1967 по 1973 год прожили с новым сердцем дольше года; с 1974 по 1983 год годичная выживаемость увеличилась до 60 %, а вот пятилетняя составила лишь 21 %.
Иммунологи и фармакологи берутся за дело
В 1983 году увенчались успехом клинические исследования нового иммуносупрессора — циклоспорина, нерибосомного полипептида, получаемого из почвенных грибов вида Beauveria nivea. Его выделили в 1970 году в рамках программы по скринингу новых антибиотиков. В 1972 году бельгийский иммунолог Жан-Франсуа Борель открыл способность циклоспорина ингибировать культуру лимфоцитов при отсутствии общего цитостатического эффекта. В конце 70-х британский хирург Рой Калне провел первые испытания эффективности циклоспорина после трансплантации сердца и почек на экспериментальных животных. Его внедрение в широкую практику открыло новую эру в трансплантации сердца, поскольку позволило значительно продлить жизнь пациентов после трансплантации. В 1994 году было одобрено использование для послеоперационной терапии еще одного нового иммуносупрессора — такролимуса (FK-506) из группы макролидов, продуцируемого актиномицетом Streptomyces tsukubaensis. В 1987 году японские иммунологи Шиничи Савада и Джен Судзуки в экспериментах in vitro обнаружили, что такролимус в 100 раз активнее циклоспорина подавляет пролиферацию Т-лимфоцитов. В исследованиях на крысах, собаках и приматах, проводившихся с 1988 по 1993 год, такролимус обеспечивал профилактику отторжения трансплантата в дозах в 10–100 раз более низких, чем циклоспорин, и с меньшим количеством побочных эффектов. Впрочем, модификации циклоспорина, разработанные в то же время, обладали аналогичными преимуществами.
Последние успехи иммуносупрессии связаны с поли- и моноклональными антителами (подробно об этом мы рассказывали в КС № 5 (118) 2013, статья «Достижения фармацевтики: моноклональные антитела»), позволяющими предотвратить стероид-резистентное — не купируемое даже пульс-терапией метилпреднизолоном — отторжение тканей, которое встречается с частотой 10–18 %.
В настоящее время используется трехкомпонентная схема иммуносупрессивной терапии: циклоспорин А или такролимус в сочетании с метилпреднизолоном и микофенолата мофетилом (цитостатиком, который наиболее эффективен в отношении лимфоцитов). Препараты антилимфоцитарных антител (ALG, ATG, ОКТ-3) применяются в качестве вводной терапии, а также при выраженных признаках отторжения или стероид-резистентном отторжении.
Что представляет собой искусственное сердце?
Совместными усилиями кардиохирургов и инженеров разработаны механизмы, получившие название «искусственное сердце». Они делятся на 2 группы:
- гемооксигенаторы — обеспечивающие насыщение кислородом во время работы специального насоса для перекачивания крови из венозной системы в артериальную, их называют аппаратами для искусственного кровообращения и широко используют для операций на открытом сердце;
- кардиопротезы — технические механизмы для имплантации и замены работы сердечной мышцы, они должны соответствовать параметрам деятельности, обеспечивающей достаточное качество жизни человека.
В настоящее время технические устройства продолжают усовершенствоваться, до внедрения в практику они должны выдержать эксперименты на животных и пройти клинические испытания
Эра разработки искусственного сердца началась в 1937 году с работ советского ученого В. Демихова. Он провел опыт с подключением кровообращения собаки к пластиковому насосу собственной разработки. Она прожила 2,5 часа. Кристиан Бернард считал В. Демихова своим учителем.
Через 20 лет американские ученые В. Кольф и Т. Акутсу разработали первый аппарат из полихлорвинила с четырьмя клапанами.
В 1969 году проведена первая двухэтапная операция: сначала пациента 64 часа поддерживали аппаратом для искусственного кровообращения, затем пересадили донорское сердце. До настоящего времени основным применением искусственного сердца остается временная замена естественного кровообращения.
Работа над полными аналогами осложняется большой массой аппарата, необходимостью частой подзарядки, высокой стоимостью подобной операции.
Почему в России не хватает доноров?
И даже при действующей презумпции согласия в России катастрофически не хватает доноров. Ожидание почки может растянуться на долгие годы. На искусственном сердце, которое подходит лишь единицам, человек может продержаться год, два и даже три. А тяжелые осложнения оборачиваются высокой смертностью. При этом пересадки легких и поджелудочной железы до сих пор остаются очень редкими операциями. А ведь один донор может спасти как минимум восемь жизней.
— У нас всего 32 региона занимаются трансплантацией, и мы сейчас из кожи вон лезем, чтобы увеличить их число. Ездим по субъектам, говорим с больницами, администрациями. Говорим, что органный ресурс пропадает — люди ждут этих органов. Мы не можем говорить о дефиците как таковом. Правильно говорить об отсутствии административного ресурса для организации донорских программ, — уверяет Сергей Готье, директор НМИЦ трансплантологии и искусственных органов.
Ответственности для больниц, в которых появляются доноры, нет. Никто не понесет никакого наказания, если человек не стал донором, хотя мог бы им стать.
— Трансплантологи — это люди, которые хотели бы обладать этим ресурсом для спасения населения. Но организовать этот процесс мы не можем. Это ответственность главных врачей больниц, в которых констатируется смерть тех или иных пациентов. Этот механизм работает с большим трудом, — говорит врач.
Его коллега Александр Чернявский убежден, что причина кроется и в том, что у таких больниц нет никакой заинтересованности в развитии донорства.
— Законы есть, положение принято. Но их невыполнение ничем не карается, никто за это не отвечает — за то, что у нас не хватает донорских органов, — недоволен Александр Чернявский. — Мы рассчитали, сколько потенциальных доноров может быть в Новосибирске, например. Есть определенные формулы, известные во всем мире и используемые для расчета. И у нас примерно в Новосибирске от 50 до 70 реальных доноров в год. Я думаю, в этом случае мы могли бы вообще решить проблемы с оказанием помощи пациентам с почечной недостаточностью. Это примерно 140 трансплантаций почек в год.
Если рассматривать этот вопрос только с финансовой точки зрения, то эксперты убеждают — трансплантация органа намного выгоднее для государства, чем тот же диализ, на котором должны находиться пациенты с почечной недостаточностью.
— Если бы наши донорские базы работали достаточно эффективно и продуктивно, мы могли бы вообще отказаться от диализов. Мы же думаем только о сиюминутных затратах, а когда смотрим, что этому пациенту нужно делать диализ 10–15 лет, то понимаем, что это огромные суммы. Они складываются в миллиарды рублей. Пациент, которому трансплантирована почка, обходится государству в несколько раз дешевле. И это посчитано уже давно. Мы вообще не умеем деньги считать.
Кому показана пересадка?
Кандидатами на пересадку сердца являются больные с патологией, не позволяющей прогнозировать более года жизни при использовании других методов лечения. К ним относятся больные с:
- выраженными признаками сердечной недостаточности при малейших движениях, в покое, если фракция выброса при ультразвуковом исследовании ниже 20%;
- дилатационной и ишемической кардиомиопатией;
- злокачественными аритмиями;
- врожденными сердечными пороками.
Существовавшие ранее ограничения по возрасту (до 65 лет) в настоящее время не считаются определяющими. Для ребенка срок операции определяется наиболее оптимальной подготовкой, способностью обеспечить полноценную иммунную защиту.
Такой малыш нуждается в срочной операции для сохранения жизни
Мировой опыт и цены
Как показывает практика, пересаженное сердце при соблюдении всех медицинских рекомендаций, способно без перебоев работать в течение 5-7 лет. Однако процессы старения в донорском органе идут быстрее, чем в собственном, а потому рано или поздно пациент отметит возвращение всех симптомов сердечной недостаточности.
Реальная практика пересадки сердца в разных значительно отличается. В некоторых странах данные операции совсем не проводятся, потому что не урегулированы на законодательном уровне. В других странах такие операции четко регламентируются и к ней могут прибегнуть, как жители самой страны, так иностранные граждане. Например, в Республике Беларусь органная трансплантация осуществляется в соответствии с законом, в основе которого лежит «презумпция согласия»: забор органа у донора может быть осуществлен после констатации смерти мозга, если пожелания обратного не выражены пациентом до смерти. Орган может быть использован в дальнейшим нуждающимся пациентам.
БЕСПЛАТНО ПОДОБРАТЬ КЛИНИКУ ДЛЯ ПРОВЕДЕНИЯ ТРАНСПЛАНТАЦИИ (ПЕРЕСАДКИ) СЕРДЦА
Противопоказания к проведению операции
В медицинских учреждениях, где проводится пересадка сердца, всех кандидатов вносят в «Лист ожидания». Отказывают больным при наличии:
- легочной гипертензии;
- системных болезней (коллагенозы, васкулиты);
- хронических инфекционных заболеваний (туберкулез, вирусный гепатит, бруцеллез);
- ВИЧ-инфицирования;
- злокачественного образования;
- алкоголизма, зависимости от табака, наркотиков;
- нестабильного психического состояния.
Проводится оценка возможности и желания пациента поддерживать дальнейший план терапии и следовать указаниям врача по обследованию, режиму. Если характер больного делает контакт с лечащим врачом мало вероятным, то на него не стоит затрачивать усилия врачей и стоимость донорского сердца.
Есть ли шанс на перемены? Что изменит новый закон
Действующий закон о трансплантации был принят почти 30 лет назад. И в нем много пробелов, которые в том числе и настраивают людей против трансплантации. Новый закон должен создать единый лист ожидания по всей стране, а также регистр отказов и согласия на посмертное донорство. Это должно сделать систему более прозрачной — и для пациентов, и для врачей. А также закон должен полностью исключить ситуации, когда орган взяли после смерти человека, который не хотел этого.
Также документ определяет время, за которое родственники должны принять решение, — разрешать или нет трансплантацию. Посмертному донорству посвящена целая глава — № 3. В статье 14 говорится, что родственники могут заявить, что несогласны с изъятием органов у умершего. На это им дается два часа, и при таком заявлении тело трогать не будут.
При этом для разрешения споров по этому вопросу, когда человек дал согласие на донорство еще при жизни, а родственники выступили против, — была прописана отдельная статья № 15. В ней говорится, что если родственник не согласен, чтобы у умершего забрали орган, а при этом сам пациент давал такое согласие при жизни, то мнение родственника учитывать не будут. Орган возьмут. И наоборот.
Новый закон детально прописывает механизм детского донорства. Врачи должны будут заручиться согласием одного из родителей. При этом если мнение папы и мамы разойдутся, то пересадка будет невозможна. Запрещена она также, если возможный донор — сирота. Новый закон обсуждают уже больше пяти лет. Но он до сих пор не принят.
— Новый закон, если его примут, будет содержать элементы контроля за всеми компонентами трансплантации. Речь идет о включении в такую контрольную систему листов ожиданий и о чем мы постоянно говорим — о регистре прижизненных волеизъявлений. Фактически нам нужен регистр отказов, — объясняет Сергей Готье.
Как бы ни было много проблем в трансплантологии — врачи в России спасают сотни жизней. В ожидании нового закона они пытаются убедить людей, что пересадка для многих — единственный шанс на жизнь.
— Часто говорят, что, мол, это ужасно, что люди надеются на лучшее и ждут чьей-то смерти. Конечно, это не так. Они не ждут никакой смерти. Они ждут возможности, что им смогут помочь. Невозможно такими ожиданиями повлиять на смертность других людей. Мы все можем оказаться в ситуации, когда мы сегодня живы и здоровы, а завтра нам вдруг нужна пересадка, не дай бог. Поэтому нужно с уважением относиться друг к другу и стараться помогать друг другу, — считает Александр Быков, главный трансплантолог Новосибирской области.
Какое обследование проводится перед операцией?
В программу подготовки входит перечень клинических видов обследования. Часть из них имеет инвазивный характер, подразумевает введение катетера внутрь сердца и крупных сосудов. Поэтому они проводятся в стационарных условиях.
- Стандартные лабораторные анализы, позволяющие контролировать функцию почек, печени, исключить воспаление.
- Обязательные обследования на инфекционные болезни (туберкулез, ВИЧ, вирусы, грибы).
- Исследования на скрытые онкологические заболевания (маркеры ПСА на опухоль простаты, цитология мазка шейки матки и маммография у женщин).
Инструментальные виды исследования определяются врачом, к ним относятся:
- эхокардиография,
- коронароангиография,
- рентгенография,
- определение функций дыхания;
- показатель максимального потребления кислорода позволяет установить уровень сердечной недостаточности, степень тканевой гипоксии, спрогнозировать выживаемость после операции;
- эндомиокардиальная биопсия клеток миокарда назначается при подозрении на системное заболевание.
Специальным исследованием с помощью введения катетера в полость правого предсердия и желудочка устанавливают возможность сосудистых изменений, измеряют сопротивление в легочных сосудах.
Учет показателя проводится в единицах Вуда:
- при более 4 — пересадка сердца противопоказана, изменения в легких носят необратимый характер;
- при значении 2–4 — назначают дополнительные пробы с вазодилататорами и кардиотониками для выяснения обратимости повышенного сопротивления сосудов, если изменения подтверждают обратимый характер, то остается высоким риск осложнений.
Со всеми выясненными рисками знакомят пациента перед получением письменного согласия на операцию.
Процесс подготовки к оперативному вмешательству
Если пациента направляют в трансплантационный центр и принимают решение о постановке его в очередь на пересадку органа, ему назначают специальный план обследования. Необходимыми в данном случае анализами являются:
- Осмотр уролога, гинеколога.
- Осмотр стоматолога, оториноларинголога (это необходимо, чтобы исключить наличие хронических инфекционных очагов в полости рта и носоглотки).
- Осмотр кардиохирурга.
- ЭКГ, УЗИ сердца, КАГ (при необходимости).
- Общее лабораторное исследование образцов мочи.
- Клиническое лабораторное исследование образцов крови, определение группы крови, свертывающей системы.
- Исследования крови на маркеры сифилиса, вирусных гепатитов, ВИЧ-инфекции.
- Рентгенографическое исследование органов грудной полости или флюорография.
Для госпитализации в трансплантационный центр на операцию в случае наличия донора у пациента всегда должны быть в наличии копии и оригиналы следующей документации:
- Паспорт, полис медицинского страхования, СНИЛС.
- Выписка, полученная в направляющем учреждении и содержащая в себе результаты всех проведенных обследований.
- Направление, полученное в лечебно-профилактическом учреждении по месту регистрации реципиента. О стоимости операции по пересадке сердца информация должна быть собрана.
Ход и техника операции
Под общим наркозом больному рассекают грудину, вскрывают полость перикарда, подключают к искусственному кровообращению.
Опыт показал, что «доработки» требует донорское сердце:
- осматривают отверстие между предсердиями и желудочками, при его неполном открытии проводят ушивание;
- укрепляют кольцом трехстворчатые клапаны для снижения риска обострения легочной гипертензии, перегрузки правых отделов сердца и предупреждения возникновения недостаточности (через 5 лет после пересадки возникает у половины пациентов).
Удаляют желудочки сердца реципиента, предсердия и крупные сосуды остаются на месте.
Имплантируемое сердце донора сшивается с собственными остатками больного
Используют 2 метода расположения трансплантанта:
- Гетеротопический — его называют «двойным сердцем», действительно, оно у больного не удаляется, а трансплантат помещают рядом, выбирается положение, позволяющее соединить камеры с сосудами. В случае отторжения сердце донора может быть удалено. Негативные последствия метода — сдавление легких и нового сердца, создание благоприятных условий для образования пристеночных тромбов.
- Ортотопический — донорское сердце полностью замещает удаленный больной орган.
Трансплантированный орган может начать работу самостоятельно при подключении к кровотоку. В некоторых случаях для запуска применяется электрошок.
Для поддержки и контроля ритма устанавливается временный кардиостимулятор. В грудной полости помещаются дренажные трубки для отвода скопившейся крови и жидкости.
Грудину закрепляют специальными скобами (срастется спустя 1,5 месяца), а на кожу накладывают швы.
Разные клиники применяют видоизмененные техники операции. Их цель – снизить травматизацию органов и сосудов, предотвратить повышение давления в легких и тромбозы.
Трансплантация сердца: взгляд терапевта
С каждым годом количество пациентов с сердечнососудистыми заболеваниями (ССЗ) увеличивается в геометрической прогрессии. Результатом течения большинства заболеваний сердечно-сосудистой системы чаще всего становится снижение насосной функции сердца, т. е. развитие хронической сердечной недостаточности (ХСН) [1, 2].
По данным эпидемиологических исследований последних 10 лет, проведенных в нашей стране, стало известно, что в РФ ХСН I–IV функционального класса страдают 7,9 млн человек среди общей популяции, что составляет 7% случаев [1]. В настоящее время достигнуты значительные успехи в области лекарственной терапии данной патологии. Тем не менее, хирургическое вмешательство, а именно ортотопическая пересадка сердца, позволяет добиться хороших результатов при лечении кардиологических заболеваний в стадии декомпенсации с неблагоприятным прогнозом [3]. По последним данным продолжительность функционирования трансплантированного сердца может достигать в среднем 5 и даже 10 лет [3]. Только за 2012 г. количество операций пересадки сердца составило около 4000 в мире, и это число постоянно увеличивается [2]. В России в том же году было выполнено 132 подобных трансплантации [4].
Основными причинами для проведения данной процедуры становятся проявления тяжелой недостаточности кровообращения при дилатационной кардиомиопатии и ишемической болезни сердца. Понятно, что ведется тщательный отбор больных для подобной операции, однако реальную возможность получить этот вид помощи может лишь часть нуждающихся [3].
Такие пациенты входят в категорию повышенного риска по ряду болезней, прежде всего ССЗ и инфекционной природы, что заставляет их чаще остальных обращаться к врачам различных специальностей. При этом важна грамотность медицинского персонала относительно данного состояния, что необходимо для выбора оптимальной тактики ведения подобных пациентов [5].
В настоящей работе мы представили пациента с ортотопической трансплантацией сердца по поводу дилатационной кардиомиопатии, а также описали самые частые заболевания, встречающиеся в посттрансплантационном периоде, о чем следует помнить и врачам амбулаторно-поликлинического звена, прежде всего терапевтам.
Клиническое наблюдение
Пациент К., 30 лет, впервые обратился в поликлинику по месту жительства в 2000 г. в возрасте 17 лет, с жалобами на головную боль, головокружение, тошноту. При обследовании впервые зарегистрированы повышенные цифры артериального давления (АД) (табл. 1), что послужило поводом для его госпитализации. Для исключения поражения органов-мишеней было проведено полное обследование пациента, в частности ультразвуковое исследование, сцинтиграфия и электронно-лучевая томография почек и почечных артерий, по результатам которых обнаружено сморщивание правой почки, полное удвоение ее чашечно-лоханочной системы. Другой патологии выявлено не было. В стационаре проводилось лечение гипотензивными препаратами (эналаприл).
С 2005 по 2009 гг. пациент неоднократно госпитализировался по поводу повторяющихся подъемов АД (табл. 1). Регулярную медикаментозную терапию не принимал. В апреле 2009 г. на фоне протекающей острой респираторно-вирусной инфекции (ОРВИ) возникла сильная сдавливающая боль. При госпитализации был диагностирован острый Q-образующий переднеперегородочный инфаркт миокарда левого желудочка с переходом на верхушку и боковую стенку, было проведено стентирование передней межжелудочковой ветви коронарной артерии. При проведении эхокардиографии (ЭХО-КГ) были обнаружены признаки аневризмы верхушки левого желудочка. Фракция выброса — 35%. Была назначена терапия клопидогрелем (Плавикс), ацетилсалициловой кислотой (Тромбо АСС), бисопрололом (Конкор), аторвастатином (Торвакард). В течение последующих 1,5 лет самочувствие пациента было относительно удовлетворительным.
Осенью 2010 г. также на фоне острой респираторной вирусной инфекции (ОРВИ) перенес повторный Q-образующий инфаркт миокарда боковой стенки, осложнившийся острой левожелудочковой недостаточностью Killip II, острой аневризмой левого желудочка, синдромом Дресслера. Проводился системный тромболизис алтеплазой.
С начала 2011 г. стал отмечать нарастающую одышку, ощущение нехватки воздуха. При обследовании впервые выявлен двусторонний гидроторакс, удалено 1,4 л жидкости невоспалительного характера. По данным ЭХО-КГ обнаружено значительное увеличение всех камер сердца, уменьшение толщины межжелудочковой перегородки и передней стенки левого желудочка, снижение фракции выброса до 21%, увеличение систолического давления в легочной артерии до 40 мм рт. ст., впервые диагностирована дилатационная кардиомиопатия и недостаточность кровообращение 3 ст., III–IV функциональный класс по NYHA (Нью-Йоркская ассоциация кардиологов, New York Heart Association).
Проводимая терапия (торасемид, спиронолактон, карведилол, дигоксин) четкого клинического эффекта не давала. В течение последующих 2,5 лет пациент К. многократно госпитализировался по поводу декомпенсации ХСН.
В связи с нарастающими симптомами ХСН и отсутствием выраженного эффекта консервативной терапии в октябре 2013 г. пациенту была предложена пересадка сердца в Федеральном научном центре трансплантологии и искусственных органов им. академика В. И. Шумакова. При поступлении в институт — состояние больного средней степени тяжести, пастозность голеней, отеки стоп. При аускультации легких дыхание ослаблено в нижних отделах. Границы сердца влево +3,5 см, вправо +1,5 см, вверх +1 см. Пульс сниженного наполнения и напряжения, дефицита пульса нет. Печень при перкуссии 17×12×10 см, при пальпации нижний край плотный безболезненный. Другой патологии при обследовании выявлено не было.
Перед проведением операции в числе основных манипуляций проводилось исследование центральной гемодинамики (табл. 2), по результатам которой выявлялись небольшие признаки легочной гипертензии, что могло осложнить течение операции и посттрансплантационного периода.
В ноябре 2013 г. пациенту была выполнена ортотопическая трансплантация сердца. Ранний послеоперационный период осложнился на 3-и сутки острой почечной недостаточностью. Пациент К. был переведен на гемодиализ в течение 5 дней. Впоследствии диурез был восстановлен.
Была назначена пожизненная иммунодепрессивная терапия такролимусом (Програф), метилпреднизолоном, микофеноловой кислотой (Майфортик) и профилактическая терапия валганцикловиром (Вальцит) в течение 6 месяцев после операции с последующим переходом на ацикловир, а также сопроводительная гастропротективная терапия. Рекомендовано плановое амбулаторное обследование пациента каждый месяц в течение всей жизни, ежегодная госпитализация с обязательным полным обследованием, которое включает клинический и биохимическим анализ крови, эхокардиографию и коронароангиографию с внутрикоронарным ультразвуковым исследованием (каждые 1–2 года).
В настоящее время (июнь 2014 г.) при последнем осмотре в поликлинике по месту жительства: состояние пациента удовлетворительное, тургор тканей сохранен, отеков нет. Дыхание везикулярное, проводится во все отделы. Границы сердца увеличены влево на 1 см. Пульс ритмичный, удовлетворительного наполнения и напряжения, частота сердечных сокращений 78 в минуту, АД 130/80 мм рт. ст. Печень при перкуссии не увеличена, при пальпации ее край мягкий безболезненный. Для исследования психоэмоционального состояния пациенту К. было предложен психологический тест HADS [6], по результатам которого данных за наличие тревоги и депрессии нет.
В оценке и сравнении электрокардиографии (ЭКГ) до и после операции также можно выявить значительные изменения (рис.).
В настоящий момент помимо вышеуказанной терапии больной постоянно принимает ацетилсалициловую кислоту (Тромбо АСС) и периндоприл (Престариум), ивабрадин (Кораксан) для предупреждения приступов тахикардии.
Интерес настоящего наблюдения состоит в том, что в дебюте заболевание проявлялось артериальной гипертензией, видимо связанной с патологией почек. Клиническая картина ишемической болезни сердца манифестировала повторными инфарктами миокарда, осложнившимися аневризмой левого желудочка, синдромом Дресслера и вследствие этого тяжелой недостаточностью кровообращения. Таким образом, диагноз «дилатационная кардиомиопатия» был установлен лишь через 11 лет после дебюта клинических проявлений артериальной гипертензии, ишемической болезни сердца, тромбоэмболического синдрома, ХСН.
Обсуждение
Дилатационная кардиомиопатия (ДКМП) — заболевание, поражающее миокард и характеризующееся выраженным расширением камер сердца, снижением систолической функции левого и правого желудочков, диастолической дисфункцией. Ежегодно регистрируется 5–8 случаев впервые выявленной дилатационной кардиомиопатии на 100 тыс. населения. Наиболее часто манифестация данного заболевания регистрируется в возрасте 30–45 лет. Этиология данного заболевания остается неизвестной, хотя большое значение придают наличию вирусного миокардита в анамнезе, отягощенной наследственности (в 40% случаев заболевание носит семейный характер), иммунологическим нарушениям. При подозрении ДКМП для подтверждения диагноза необходимо проведение ЭКГ, ЭХО-КГ, стресс ЭХО-КГ с добутамином, катетеризация сердца и ангиография, эндомиокардиальная биопсия. В большинстве случаев достаточно двух из всех перечисленных исследований, для того чтобы подтвердить у пациента наличие данного заболевания [7].
Количество пациентов, у которых выполнена пересадка сердца, неуклонно растет. После подобной операции качество жизни людей с ССЗ значительно улучшается, а также просматривается тенденция к снижению количества смертей от данной патологии как в мире, так и в нашей стране. Однако для большинства врачей терапевтической специализации многие вопросы относительно того, кому необходимо рекомендовать подобную операцию, а также заболеваний, ассоциированных с посттрансплантационным периодом, остаются открытыми [1, 8].
Привлекает также к себе внимание относительная редкость подобных больных в общеклинической практике работы участкового терапевта. В табл. 3 представлены основные показания и противопоказания для пересадки сердца.
В процессе наблюдения за пациентами следует помнить о возможных поздних осложнениях после пересадки сердца, таких как послеоперационная инфекция, развитие патологии коронарных артерий, артериальная гипертензия и др. Также имеется вероятность развития хронического отторжения донорского органа. Все это требует высококвалифицированного регулярного наблюдения в центре, где проводилась трансплантация [9].
Патология коронарных артерий (ПКА) — основная причина смерти в посттрансплантационном периоде. Так как трансплантированное сердце денервировано, стенокардии обычно нет. Единственными проявлениями данной патологии могут быть лишь безболевая ишемия и внезапная сердечная смерть. При гистологическом исследовании в артериях сердца происходит прогрессирующая диффузная концентрическая гиперплазия гладких мышц и интимы. Исследования показывают, что при изначальной ишемии донорского органа повышается риск поражения коронарных артерий. Для предупреждения подобных осложнений всем пациентам при обращении в поликлинику необходимо тщательное исследование сердца с целью ранней диагностики патологии коронарных артерий [2, 3, 10].
Инфекционные заболевания стоят на первом месте по частоте встречаемости у пациентов на всем протяжении всего посттрансплантационного периода. Среди них вирус Эпштейна–Барр (ВЭБ), цитомегаловирус (ЦМВ), вирус простого герпеса (ВПГ), Toxoplasma gondii, Pseudomonas aeruginosa, Staphуlococcus aureus, Pneumocystis carinii, Candida albicans, Aspergillus spp., наиболее часто выявляемые микроорганизмы [2, 5].
ЦМВ остается главной причиной инфекционных заболеваний при пересадке сердца. Считается, что цитомегаловирус играет важную роль в ускоренном развитии ПКА и реакции отторжения. С целью профилактики этого назначается соответствующая терапия в течение длительного времени. У всех пациентов исследуется плазма крови методом полимеразной цепной реакции для выявления ДНК вируса. Чаще всего кандидозы и аспергилезы являются этиологическим фактором развития тяжелой пневмонии [5].
Различные неоплазии, чаще опухоли кожи и лимфопролиферативные заболевания, остаются серьезной проблемой у пациентов в посттрансплантационном периоде. Через 8 лет после трансплантации у 25% пациентов встречаются карциномы эпителия [9]. Основной теорией развития подобных патологий считается длительный прием иммуносупрессивных препаратов. Носительство ЦМВ и ВЭБ возможно играет роль в опухолевой трансформации тканей [2, 4].
Всем пациентам с пересаженным сердцем, при обращении за медицинской помощью в поликлинику по любым вопросам, необходим тщательный осмотр кожных покровов с обязательной биопсией подозрительных образований, а также исследование лимфатической системы, с последующей консультацией гематологом, если это необходимо [3].
После трансплантации помимо новых болезней возможно прогрессирование уже существующих заболеваний. Так, у 75% пациентов развивается АГ в течение первого года после операции. Это число возрастает до 95% за последующие пять лет. Почечная недостаточность (ПН), возникающая после трансплантации сердца, развивается вследствие постоянного приема циклоспорина А. Около 2–3% пациентов, перенесших такую операцию, нуждается в диализе, а в конечном счете, в необходимости трансплантации почки. Гиперлипидемия встречается у 85% больных подобного профиля. У 35% пациентов развивается сахарный диабет через 2–5 лет после трансплантации. Это, возможно, происходит за счет постоянной терапии иммуносупрессивными препаратами, стимулирующими глюконеогенез. Кроме того, вследствиеприема данной терапии может развиваться остеопороз, некроз бедра и другие заболевания опорно-двигательного аппарата, а также неврологические нарушения, эпилепсия и очаговые неврологические приступы [9].
Тем не менее, посттрансплантационная медикаментозная терапия назначается пациентам по витальным показаниям и ее отмена по каким-либо причинам или нарушение приема могут иметь фатальные последствия. Ни один из клинических специалистов, помимо врача трансплантолога, не может вносить в нее какие-либо изменения. Значительные усилия сейчас прилагаются к разработке оптимальных режимов иммуносупрессии, где нежелательные лекарственные реакции в виде указанных выше заболеваний были бы нивелированы настолько, насколько это возможно. Именно поэтому важен прицельный осмотр указанных органов и систем у всех пациентов с пересадкой сердца в анамнезе для выявления и исключения специфических посттрансплантационных осложнений [8].
Заключение
Таким образом, на данный момент пересадка донорского сердца стала методом выбора у большинства пациентов с сердечно-сосудистыми заболеваниями в стадии декомпенсации. Количество пациентов, у которых такая операция уже проведена, увеличивается с каждым годом. Несмотря на то, что трансплантация сердца и медикаментозная терапия после нее несут большое количество осложнений, такая процедура значительно повышает качество жизни (по нашим наблюдениям) и ее продолжительность. Для предупреждения и выявления различных заболеваний, ассоциированных с операцией трансплантации сердца, очень важна грамотность медицинского персонала, в первую очередь терапевтического профиля, т. к. пациенты чаще всего обращаются за помощью к врачам этой специальности. Следует отметить, что проблема трансплантации органов затрагивает многие аспекты, включая этические, и является не только медицинской, но и общесоциальной.
Литература
- Фролова Э. Б., Яушев М. Ф. Современное представление о хронической сердечной недостаточности // Вестник современной клинической медицины. 2013. Т. 6, № 2. С. 87–93.
- Toyoda Y., Guy T. S., Kashem A. Present status and future perspectives of heart transplantation // Circulation Journal. 2013. V. 77, № 5. P. 1097–1110.
- Shah M. R. et al. Heart transplantation research in the next decade-a goal to achieving evidence-based outcomes: national heart, lung, and blood institute working group // Journal of the American College of Cardiology. 2012. V. 59, № 14. P. 1263–1269.
- Национальные клинические рекомендации: трансплантация сердца / Под ред. С. В. Готье и др. М.: Российское трансплантологическое общество, 2013. С. 93.
- Ensor C. R. et al. Induction immunosuppression for orthotopic heart transplantation: a review // Progress in Transplantation. 2009. V. 19, № 4. P. 333–341.
- Zigmond A. S., Snaith R. P. The Hospital Anxiety and Depression scale // Acta Psychiatrica Scandinavica. 1983. V. 67. P. 361–370. Адаптирована Дробижевым М. Ю., 1993.
- Сабиров Л. Ф. и др. Дилатационная кардиомиопатия // Вестник современной клинической медицины. 2012. Т. 5, № 3. С. 56–63.
- Radovancevi B., Frazier O. H. Heart transplantation: approaching a new century // Texas Heart Institute Journal. 1999. V. 26, № 1. P. 60–70.
- Hetzer R., Delmo Walter E. M. Trends and outcomes in heart transplantation: the Berlin experience // HSR Proceeding in Intensive Care Cardiovascular Anesthesia. 2013. V. 5, № 2. P. 76–80.
- Kaufman B. D., Shaddy R. E. Immunologic considerations in heart transplantation for congenital heart disease // Current Cardiology Reviews. 2011. V. 7, № 2. P. 67–71.
Ю. А. Ливандовский, кандидат медицинских наук О. В. Рыбина1
ГБОУ ВПО МГМСУ им. А. И. Евдокимова МЗ РФ, Москва
1 Контактная информация
Что делают после пересадки сердца?
Пациент переводится в отделение реанимации или интенсивной терапии. Здесь к нему подключают кардиомонитор для контроля за ритмом.
Искусственное дыхание поддерживается до полного восстановления самостоятельного.
При достаточном собственном объеме дыхательных движений интубационная трубка извлекается, но постоянно подается кислород через маску или носовые катетеры
- Контролируется артериальное давление, отток мочи.
- Для обезболивания показаны наркотические аналгетики.
- С целью профилактики застойной пневмонии больному необходимы форсированные дыхательные движения, назначаются антибиотики.
- Для предупреждения тромбообразования показаны антикоагулянты.
- В зависимости от электролитного состава крови назначаются препараты калия, магния.
- С помощью щелочного раствора поддерживается нормальный кислотно-щелочной баланс.
Какие осложнения могут последовать после пересадки?
Наиболее известные осложнения хорошо изучены клиницистами, поэтому распознаются на ранних этапах. К ним относятся:
- присоединение инфекции;
- реакция отторжения к тканям пересаженного сердца;
- сужение коронарных артерий, признаки ишемии;
- застойные явления в легких и нижнедолевая пневмония;
- образование тромбов;
- аритмии;
- послеоперационное кровотечение;
- нарушение функций мозга;
- за счет временной ишемии возможно повреждение разных органов (почек, печени).
Для подавления отторжения донорских тканей пациенту назначаются сильные препараты, воздействующие на иммунные клетки крови. Этим одновременно создаются благоприятные условия для заражения любой инфекцией и ракового перерождения.
Образ жизни после операции
Образ жизни после операции по пересадке сердца складывается из следующих составляющих:
- Прием медикаментов. Эта часть жизни пациента после операции является, пожалуй, самой важной. Пациент должен тщательно следить за временем приема лекарств и точно соблюдать предписанную врачом дозировку. В основном речь идет о приеме цитостатиков и гормональных препаратов, угнетающих собственный иммунитет, направленный против чужеродных тканей сердца.
- Физическая активность. В первый месяц пациент должен соблюдать строгий ограничительный режим, но повседневная обычная активность все-таки должна присутствовать. Уже через пару месяцев пациент может снова начать водить автомобиль, а еще через несколько может приступить к легким физическим упражнениям (гимнастика, ходьба и др).
- Питание. Необходимо вести здоровый образ жизни, полностью исключить употребление алкоголя, табакокурение и соблюдать диету с исключением вредных продуктов питания (жирное, жареное, копченое и т. д).
- Защита от инфекций. Пациенту следует избегать посещения людных мест в первые месяцы после операции, избегать контакта с заболевшими инфекционными заболеваниями в дальнейшем, тщательно мыть руки перед едой, употреблять только кипяченую воду и термически хорошо обработанные продукты питания. Это связано с тем, что угнетение иммунитета может привести к повышению заболеваемости бактериальными, грибковыми и вирусными заболеваниями после начала иммуносупрессивной терапии.
В целом можно отметить, что жизнь после операции, несомненно, сильно меняется, но и качество жизни без одышки, сердцебиения и отеков изменяется к лучшему.
Как проводится реабилитация послеоперационного больного?
Реабилитация начинается с восстановления вентиляции легких.
- Пациенту рекомендуют заниматься дыхательными упражнениями по нескольку раз в день, надувать воздушный шар.
- Для предупреждения тромбоза вен ног проводят массаж и пассивные движения в голеностопах, сгибание поочередное коленей.
- Наиболее полный комплекс реабилитационных мероприятий больной может получить в специальном центре или санатории. Вопрос о направлении следует обсудить с врачом.
- Не рекомендуется быстро увеличивать нагрузку на сердце.
- Исключаются горячие ванны. Для мытья можно использовать теплый душ.
Все препараты, назначаемые врачом, необходимо принимать в нужной дозировке.