1.Общие сведения
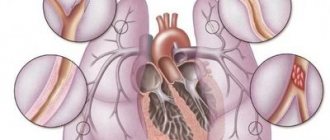
Ревматическая группа заболеваний объединена общим этиопатогенезом и поражаемыми «мишенями»: имеет место системная, касающаяся всего организма патология соединительной ткани и ассоциированный с ней воспалительный процесс, обычно в крупных суставах. Однако наиболее опасным последствием ревматического процесса является поражение миокарда, которое при ревматизме имеет место всегда, – в той или иной степени выраженности (согласно известной и весьма точной медицинской поговорке, «ревматизм лижет суставы и кусает сердце»). В ряде случаев ревматическое воспаление протекает в форме острой лихорадки, которая после купирования основной симптоматики осложняется формированием специфического порока сердца. Имеется в виду повреждение и нарушение сложной клапанной биомеханики миокарда, которая в норме обеспечивает его бесперебойную насосную функцию. В таких случаях говорят о хронической ревматической болезни сердца (ХРБС).
Проблема по ряду причин является весьма серьезной во всем мире. Во-первых, ревматическая болезнь сердца достаточно широко распространена: в статистике ВОЗ она занимает четвертое место среди всех сердечно-сосудистых заболеваний. Во-вторых, ХРБС является одним из главных факторов высокой летальности в данной категории. В-третьих, ревматический порок сердца формируется обычно у детей, подростков и молодых людей, – т.е. поражает наиболее перспективную, активную и трудоспособную часть населения, зачастую приводя к инвалидизациям и «выключая» эту выборку из социального функционирования (по крайней мере, резко ограничивая ее активность и снижая качество жизни).
Обязательно для ознакомления! Помощь в лечении и госпитализации!
2.Причины
Почти все доступные источники главной (или единственной) причиной ревматического порока сердца называют пережитую острую ревматическую лихорадку – различные варианты ревмокардита, т.е. ревматического воспаления тех или иных структурных элементов сердца. В свою очередь, острое развитие сердечного ревматизма связывают с патогенной активностью гемолитического стрептококка. Однако в специальных публикациях можно встретить данные о том, что от 30% до 50% пациентов не обнаруживают подобных эпизодов в анамнезе. Даже если предположить, что часть острых ревматических лихорадок просто не была диагностирована или зарегистрирована, проценты слишком велики для того, чтобы говорить о полной ясности причин хронической ревматической болезни сердца.
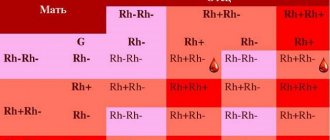
К факторам риска обычно относят принадлежность к женскому полу, частые респираторные инфекции на фоне общей иммунной слабости, наследственность, систематическое длительное пребывание в холодных помещениях с высокой влажностью воздуха.
Посетите нашу страницу Кардиология
Каковы методы дополнительной диагностики ревматизма?
Постановка диагноза острой ревматической лихорадки достаточно сложное задание, поскольку наиболее частые его проявления неспецифичны.
Диагностические критерии ревматизма:
Большие критерии:
- Кардит;
- Полиартрит;
- Хорея;
- Кольцевидная эритема;
- Подкожные ревматические узелки.
Малые критерии:
- Клинические – ревматический анамнез, суставные боли, гипертермия;
- Лабораторные анализы – острофазные маркеры: ускорение СОЭ, С-реактивного белка, нейтрофильный лейкоцитоз;
- Инструментальные – удлинённый интервал P-R по данным ЭКГ.
Дополнительно в крови обнаруживается повышенное содержание серомукоидных белков, фибриногена, α-1, α-2 глобулинов, гипоальбуминемия, высокий титр АСЛ-О, АСК, АСГ, выявляют антистрептококковые антитела.
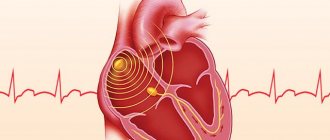
Также на ЭКГ отмечаются нарушения проводимости (АВ-блокада I-II степени), экстрасистолия, мерцательная аритмия, изменения зубца Т, депресия сегмента ST, низкий вольтаж зубцов R.
На Ro ОГК отмечается расширение сердечной тени во все стороны. На ЭхоКГ определяются краевые булавовидные утолщения клапанов, гипокинезию створок митрального клапана, аортальная регургитация.
Так же определяют время свертывания, ПТИ, толерантность к гепарину, коагулограмму.
3.Симптоматика, диагностика
Различают несколько вариантов клапанного порока, обусловливающего ХРБС. В одних случаях несостоятельность заключается в неполном смыкании, в других имеет место сужение просвета (стеноз) и, соответственно, снижение пропускной способности клапана; о сочетанном пороке говорят при одновременном наличии первых двух аномалий; о комбинированном – при пороке двух и более клапанов.
Длительное время (до нескольких лет) хроническая ревматическая болезнь сердца может протекать мало- или бессимптомно; иногда она диагностируется случайно при обследовании по другим поводам. Однако с нарастанием клапанной несостоятельности появляется слабость и утомляемость, характерный румянец с цианозным оттенком и синюшность пальцев, одышка, кашель, эпизоды ночного удушья, отечность нижних конечностей. Нередко больные жалуются на боли в печени, которая при обследовании оказывается увеличенной. Многие пациенты отмечают усиленное сердцебиение и боль в сердце при физической нагрузке, периодические головокружения, предоморочные состояния и/или обмороки.
Правильная диагностика ХРБС требует не только внимательного осмотра и подробного сбора жалоб, но и тщательного изучения анамнеза. Информативны стандартные аускультация и перкуссия, дополнительно назначают электрокардиографическое и эхокардиографическое исследования (в том числе в допплерографическом режиме для оценки пропускной способности крупных сосудов).
О нашей клинике м. Чистые пруды Страница Мединтерком!
ПОРАЖЕНИЕ СЕРДЦА И СОСУДОВ при ревматоидном артрите
При обнаружении у больного РА митрального стеноза всегда необходимо исключать его ревматическую этиологию, так как сочетание РА с предшествующим ревматическим пороком признается многими авторами. Патогмоничным признаком ревматоидного артрита являются ревматоидные узелки в миокарде, перикарде и в эндокарде в основании митрального и аортального клапанов, в области фиброзного кольца
Ревматоидный артрит (РА) — хроническое системное воспалительное заболевание соединительной ткани с прогрессирующим поражением преимущественно периферических (синовиальных) суставов по типу симметричного эрозивно-деструктивного полиартрита с частыми внесуставными проявлениями, среди которых поражение сердца, по данным вскрытия, отмечается в 50-60% случаев [1, 4, 7]. Изменения в сердце при РА в недавнем прошлом выделяли в суставно-сердечную форму заболевания. При поражении суставов, когда заметно снижается физическая активность, сердечная патология часто маскируется, что требует от врача более внимательного и тщательного обследования больного. При этом клинические изменения со стороны сердца, как правило, минимальные и редко выходят на первый план в общей картине основной болезни. Системные проявления РА, в том числе и поражение сердца, определяют прогноз в целом, поэтому важно их раннее распознавание и целенаправленное лечение.
Морфологическая картина
| Рисунок 1. Интерстициальный миокардит, умеренный васкулит. Окр. гематоксилином и эозином. Х 150 |
Частота поражения миокарда при РА в форме миокардита не выяснена. Это обусловлено, с одной стороны, трудностью диагностики миокардита у лиц с ограниченной двигательной активностью, с другой — отставанием клинических проявлений от морфологических изменений сердца [6, 7]. Патология миокарда носит полиморфный характер в связи с наличием различной давности сосудистых поражений [7]. В одних сосудах имеется васкулит, в других — гиалиноз, в третьих — склероз. Характер васкулита может быть пролиферативным и редко пролиферативно-деструктивным. В воспалительном инфильтрате преобладают лимфогистиоцитарные элементы как в периваскулярном пространстве (рис. 1), так и в стенке сосудов. Следует отметить, что при активации основного процесса наблюдается сочетание старых и свежих сосудистых изменений. Наряду с этим встречается очаговый, или диффузный, интерстициальный миокардит, заканчивающийся развитием мелкоочагового кардиосклероза. У больных ревматоидным артритом нередко развивается бурая атрофия миокарда с накоплением липофусцина в кардиомиоцитах (рис. 2). Эти изменения могут являться причиной стенокардии. Патогмоничным признаком ревматоидного артрита являются ревматоидные узелки в миокарде, перикарде и эндокарде в основании митрального и аортального клапанов, в области фиброзного кольца. В исходе узелка развивается склероз, вызывающий формирование недостаточности клапанов. Миокардит проявляется и диагностируется, как правило, на высоте активности основного ревматоидного процесса, то есть при очередном выраженном обострении суставного синдрома.
Клиника
| Рисунок 2. Интерстициальный миокардит. Отложения липофусцина в перинуклеарных пространствах. Окр. гематоксилином и эозином. Х 400 |
Ведущей жалобой при миокардите в дебюте поражения сердца являются неприятные ощущения в области сердца (кардиалгии), невыраженные, длительные, разлитые и без четкой локализации, как правило, без иррадиации и не купирующиеся нитратами. К основным жалобам относятся сердцебиение, перебои и реже одышка при физической нагрузке. Быструю утомляемость, повышенную потливость и субфебрилитет врачи обычно связывают с очередным обострением РА, а не с кардиальной патологией [3].
При аускультации физикальные данные выявляют тахикардию и ослабление I тона с систолическим шумом, нередко удается выслушать III тон. Как правило, миокардит при РА не склонен к прогрессированию, признаки сердечной недостаточности отсутствуют [4].
Данные ЭКГ
При обычном ЭКГ-исследовании могут отмечаться снижение зубцов Т, опущение интервалов ST, небольшие нарушения внутрижелудочковой проводимости. Эти изменения неспецифичны и могут сопровождать различные заболевания. Более характерное для миокардитов замедление атриовентрикулярной проводимости бывает редко.
В литературе описано значительное число наблюдений, когда нарушение ритма сердца служит единственным патологическим симптомом поражения коронарных артерий. Нарушение ритма и проводимости при активном РА существенно чаще определяется при суточном мониторировании ЭКГ и чреспищеводном электрофизиологическом исследовании, чем при обычной ЭКГ. Так,
И. Б. Виноградова [2] при исследовании больных РА с использованием вышеуказанной методики выявила нарушение ритма и проводимости у 60% больных, в том числе предсердную (18%) и желудочковую (10%) экстрасистолию, пароксизмальную тахикардию (4%), мерцательную аритмию (6%), проходящую блокаду правой ножки пучка Гиса (20%) и атриовентрикулярную блокаду II степени (2%). Также было высказано предположение, что депрессия ST, выявляемая при чреспищеводном электрофизиологическом исследовании, является косвенным признаком изменения коронарной микроциркуляции вследствие ревматоидного васкулита. Поэтому у данных больных отмечены высокие уровни циркулирующих иммунных комплексов, ревматоидного фактора, антител к кардиолипину Ig M. Важно отметить, что в этой же группе больных имелись другие признаки васкулита: дигитальный артериит, сетчатое ливедо, синдром Рейно и ревматоидные узелки. Следовательно, если рутинные клинические методы исследования не выявляют достаточно убедительных признаков ревматоидного миокардита, то современные электрофизиологические исследования обнаруживают факты нарушений функции сердца, что указывает на связь этих изменений с активностью ревматоидного процесса. Подтверждением этому может служить положительная динамика изменений под влиянием адекватного лечения основного заболевания, обычно отмечаемая при регрессе суставного синдрома.
Дифференциальная диагностика
Дифференциальная диагностика миокардита и миокардиодистрофии, нередко проводящаяся у больных РА, длительно получающих массивную лекарственную терапию, затруднена, т. к. клинические проявления в том и другом случае близки [5, 6]. Наличие миокардита подтвердит положительная динамика его проявлений под влиянием правильно подобранного и назначаемого в адекватных дозах противоревматического лечения.
| Рисунок 3. Утолщение перикарда. Склероз. Окр. гематоксилином и эозином. Х 150 |
Перикардит является наиболее характерным поражением сердца при РА [1]. Патологоанатомически он выявляется в подавляющем большинстве случаев в виде фиброзного, реже геморрагического перикардита; нередко обнаружение характерных ревматических гранулем. Отличительной особенностью перикардита при ревматоидном артрите является участие в воспалении крупных базофильных гистиоцитов под зоной фибринозных наложений. Глубже формируется грануляционная ткань, содержащая лимфоциты и плазматические клетки, с утолщением перикарда и формированием грубого склероза (рис. 3).
Больной может предъявлять жалобы на боли в области сердца разной интенсивности и длительности. Частота клинической диагностики перикардита различна (20-40%) и зависит в основном от тщательности клинического изучения больного и уровня компетентности клинициста. В большинстве случаев анатомически определяются спайки в полости перикарда и утолщение последнего за счет склеротического процессса, нередко рецидивирующего. Выпот обычно небольшой, без признаков тампонады. Подтверждается, как правило, данными рентгенологического исследования, указывающими на нечеткость и неровность контуров сердца. Шумы трения перикарда непостоянны, выслушиваются далеко не у всех больных, хотя в некоторых случаях остаются длительно в виде перикардиальных щелчков в различные фазы сердечного цикла, что фиксируется качественным ФКГ-исследованием. ЭКГ-изменения у большинства больных неспецифичны для перикардита. Но в случае появления даже умеренного экссудата можно наблюдать снижение вольтажа QRS с положительной динамикой при уменьшении выпота. Перикардиты при РА склонны к рецидивированию. В части случаев перикардиты сопровождаются появлением конкордантных отрицательных зубцов Т на многих ЭКГ-отведениях, что может приводить к постановке ошибочного диагноза инфаркта миокарда. Большое значение в обнаружении РА-перикардитов имеет эхокардиография, позволяющая выявлять изменения перикарда (его уплотнение, утолщение, наличие жидкости) и динамику этих изменений при повторных исследованиях. Во многих случаях ЭХО-изменения перикардита являются неожиданной находкой как для больного, так и для лечащего врача [8].
Эндокардит при РА отмечается значительно реже, чем перикардит. Патологоанатомические данные свидетельствуют о нередком вовлечении в процесс эндокарда, в том числе клапанного, в виде неспецифических воспалительных изменений в створках и клапанном кольце, а также специфических гранулем. У большинства больных вальвулит протекает благоприятно, не приводит к значительной деформации створок и не имеет ярких клинических проявлений. Однако у некоторых больных течение вальвулита может осложняться деформацией створок и сопровождаться выраженной недостаточностью пораженного клапана, чаще митрального, что диктует необходимость хирургической коррекции порока. Обычно эндокардит сочетается с миокардитом и перикардитом. В литературе обсуждается возможность образования стенозов митрального и аортального клапанов, но единого мнения по этому вопросу нет [6]. При обнаружении у больного РА митрального стеноза всегда необходимо исключать ревматическую этиологию его, т. к. сочетание РА с предшествующим ревматическим пороком признается многими авторами [4].
С целью изучения характера клапанной патологии сердца при РА проанализированы результаты лечения 297 больных с достоверным РА по критериям АРА. Анализ показал, что чаще всего — в 61,6% случаев — имеет место митральная регургитация. При этом у 17,2% больных она была умеренной или выраженной. У 152 (51,2%) больных полипроекционное ЭХО-КГ-исследование структурных изменений створок клапанов не выявило. Более детальный анализ позволил выделить в отдельную группу 14 больных, которые имели в анамнезе ревматизм и ревматический порок сердца. РА эти больные заболели за 1–24 года до исследования (в среднем через 8,9 года). 7 человек из них имели характерные признаки ревматического митрального стеноза (у 3 — выраженного) в сочетании с митральной регургитацией разной выраженности и признаки аортального порока, который у 1 больной был диагностирован как сочетанный. У 2 больных митральный порок был в виде умеренной митральной недостаточности и комбинировался с недостаточностью аортального клапана. У 3 больных выявлены признаки ревматической недостаточности митрального клапана. У 2 больных отмечался выраженный сочетанный аортальный порок в комбинации с относительной недостаточностью митрального клапана.
Таким образом, наши данные подтверждают возможность заболевания РА лиц, ранее болевших ревматизмом и имеющих ревматические пороки сердца.
В отдельную группу были выделены 38 больных (средний возраст 58,7 года, давность РА 12,8 года) с наличием структурных изменений клапанного аппарата сердца в виде тотального краевого утолщения створок или отдельных очагов утолщения, нередко достигающих больших величин (13х6 мм), признаков кальциноза и ограничения подвижности створок. Створки митрального кольца оказались измененными у 19, аортального — у 33, трикуспидального — у 1 больной, причем у 16 пациентов были сочетанные изменения митрального и аортального клапанов, у 1 — митрального и трикуспидального. У 17 из 19 больных структурные изменения митральных створок сопровождались митральной регургитацией.
У 17 из 33 больных с изменениями аортальных створок диагностировалась аортальная регургитация, при этом у 12 она была умеренной или выраженной. У 16 больных, в том числе у 2 с признаками кальциноза, имел место склероз аортальных створок без нарушения функции клапана, что нашло свое подтверждение и неизмененным трансаортальным кровотоком. У 1 больной со значительным утолщением створок и умеренной аортальной регургитацией имелось ограничение открытия их (1-2 см) и повышение трансаортального градиента давления, т. е. признаки аортального стеноза. И еще у 1 больной 33-летнего возраста был диагностирован врожденный двухстворчатый аортальный клапан с признаками умеренной аортальной регургитации. Выраженная трикуспидальная регургитация была диагностирована у 3 больных с очаговым утолщением трикуспидальных створок, причем у 1 из них было диагностировано легочное сердце как осложнение ревматоидного поражения легких.
Возникает вопрос: все ли обнаруженные изменения у этой группы, состоящей из 33 больных, являются следствием РА? Анализ наших данных показал, что большинство больных этой группы были в возрасте 51–74 лет. У 19 из них диагностировалась артериальная гипертензия, имелись признаки ишемической болезни сердца, 4 больных перенесли инфаркт миокарда, 1 — острое нарушение мозгового кровообращения. Результаты исследования показали, что у лиц с высокими цифрами артериального давления изменения клапанного аппарата были более выраженными, и только у них диагностировался кальциноз митрального клапана и/или аортального клапана, признаки аортальной регургитации, гипертрофия стенки левого желудочка и межжелудочковой перегородки, а также утолщение стенок аорты с признаками дилятации и диастолическая дисфункция левого желудочка. Выявленные ЭХО-КГ-изменения в этой группе больных не отличаются от таковых при атеросклеротическом кардиосклерозе, атеросклерозе аорты и являются классическими. Поэтому в этой группе больных не представляется возможным исключить атеросклеротический генез пороков сердца. Вместе с тем вполне вероятно, что собственно ревматоидное поражение клапанов может служить тем благоприятным фоном, на котором в дальнейшем развиваются выраженные структурные изменения створок, патология которых доминирует как в клинической, так и в ЭХО-КГ-картине атеросклеротического поражения клапанов сердца. В каждом случае вопрос о генезе порока при РА требует учета всех имеющихся клинических данных.
Литература
1. Балабанова Р. М. Ревматоидный артрит. В кн.: Ревматические болезни (руководство по внутренним болезням)/ Под ред. В. А. Насоновой и Н. В. Бунчука. — М.: Медицина, 1997. С. 257-295. 2. Виноградова И. Б. Нарушение сердечного ритма и проводимости у больных ревматоидным артритом// Автореф. дис. … канд. мед. наук. М., 1998. С. 21. 3. Елисеев О. М. Амилоидоз сердца// Тер. арх. 1980. № 12. С. 116-121. 4. Котельникова Г. П. Поражение сердца при ревматоидном артрите// В сб.: Ревматоидный артрит. — М.: Медицина, 1983. С. 89-90. 5. Котельникова Г. П., Лукина Г. В., Муравьев Ю. В. Кардиальная патология при вторичном амилоидозе у больных ревматическими заболеваниями// Клин. ревматол. 1993. № 2. С. 5-8. 6. Немчинов Е. Н., Каневская М. З., Чичасова Н. В. и др. Пороки сердца у больных ревматоидным артритом (результаты многолетнего проспективного клинико-эхокардиографического исследования)// Тер. арх. 1994. № 5. С. 33-37. 7. Раденска-Лоповок С. Г. Морфологические методы исследования и диагностики в ревматологии В кн.: Ревматические болезни (руководство по внутренним болезням) под ред. В. А. Насоновой и Н. В. Бунчука. М.: Медицина, 1997. С. 80-94. 8. Цурко В.В. Асептический некроз головок бедренных костей при ревматоидном артрите и системной красной волчанке. Клинико-инструментальная диагностика и исходы: Автореф. дис. … д-ра мед. наук. М., 1997. С. 50
4.Лечение
Терапевтические схемы могут существенно различаться в зависимости от клинических особенностей конкретного случая. К наиболее общим принципам относится назначение антиаритмических и гипотензивных средств, сердечных гликозидов, антикоагулянтов, – в целом, первоочередной задачей выступает разгрузка пораженного ревматическим воспалением клапана(ов) и профилактика тромбоза.
Однако даже при грамотной и адекватной терапевтической стратегии хроническая ревматическая болезнь сердца может усугубляться дальнейшими осложнениями: прогрессированием сердечной недостаточности, тромбоэмболиями (в т.ч. в бассейне кровоснабжения головного мозга, т.е. развивается ишемический инсульт), обострениями тлеющего ревматического миокардита и т.п.
При неэффективности консервативного лечения и/или угрожающе быстром нарастании сердечной недостаточности прибегают к одной из методик кардиохирургической коррекции (обычно ставится вопрос о протезировании клапана).