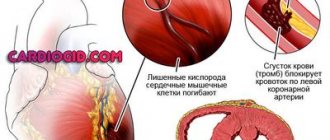
Роль гистамина в аллергической реакции
Гистамин – это биологически активное вещество, вырабатываемое организмом для регулирования жизненно важных функций (кровообращения, дыхания, пищеварения). Он концентрируется в мастоцитах – белых кровяных клетках, являющихся частью иммунной системы.
В нормальных условиях в теле человека гистамина немного, и он неактивен. Но при попадании в организм некоторых веществ начинается его активная выработка. Когда аллерген связывается с иммунноглобулином, происходит дегрануляция мастоцитов (выделение веществ, вызывающих воспалительную реакцию). Гистамин высвобождается, выходит за пределы клеток, и организм попадает под его воздействие. Это вызывает:
- крапивницу;
- отеки слизистых оболочек;
- спазмы бронхов;
- снижение артериального давления;
- расстройства пищеварения;
- спутанность сознания;
- замедление проведения нервных импульсов.
Первые три реакции являются аллергическими. Они являются ответом иммунной системы на контакт с раздражителем. Большинство аллергических реакций развиваются незамедлительно.
Что может спровоцировать повышение гистамина
Аллергенами называют вещества, провоцирующие усиленное высвобождение гистамина. Медициной изучено множество аллергенов, которые можно разделить на такие группы.
Экзогенные инфекционныеЭкзогенные неинфекционныеЭндогенныеВирусыПищевыеБелкосодержащие соединения, входящие в состав клеток организмаБактерииПыльцевыеГрибкиПромышленныеБытовыеЛекарственные
Эндогенные аллергены вырабатываются самим организмом. Они становятся причиной аутоиммунных заболеваний (атак иммунной системы на здоровые ткани).
Экзогенные попадают в организм из окружающей среды – через продукты питания, пыльцу растений, домашнюю пыль. К промышленным аллергенам относят разнообразные химические вещества (красители, чистящие средства, ароматизаторы).
Особенности применения и дозировки Н2-гистаминоблокаторов
Препараты этой группы назначаются индивидуально, отталкиваясь от диагноза и степени развитости заболевания.
Дозировка и длительность терапии определяются исходя из того, какая группа Н2-блокаторов оптимальна для лечения.
Попадая в организм при одинаковых условиях, действующие вещества препаратов разных поколений всасываются из желудочно-кишечного тракта в разных количествах.
Кроме того, все компоненты отличаются по показателю эффективности.
| Действующее вещество | Всасываемость при приеме внутрь (в %) | Эквивалентные дозировки вещества (в мг) | Длительность угнетения выработки соляной кислоты в ночное время (в часах) | Частота побочных эффектов (в % случаев) |
| Циметидин | 65-85 | 800-1000 за 3 приема в сутки | 2,5-5 | 3,2 |
| Ранитидин | 45-60 | 200-300 за 2-3 приема | 7-10 | 2,7 |
| Фамотидин | 30-60 | 40 за 1-2 приема | 10-12 | 1,4 |
| Низатидин | 75-100 | 300 за 1-2 приема | 10-12 | Очень редко |
| Роксатидин | 90-100 | 75-150 за 1-2 приема | 13-16 | Очень редко |
По общим рекомендациям Н2-блокаторы противопоказаны людям с гиперчувствительностью. Особо осторожно их следует принимать при хронической сердечной или почечной недостаточности, патологиях кроветворных органов, а также детям младше 16 лет, беременным и кормящим матерям.
Симптомы аллергической реакции
Известен широкий спектр симптомов, однако это не значит, что при контакте со всеми аллергенами имеет место одна и та же клиническая картина. В зависимости от типа гиперчувствительности, организм реагирует по-разному:
- атопический: ринит, конъюнктивит, дерматит, астма, отек Квинке;
- реагиновый: воспаление слизистых оболочек, вегетативные расстройства;
- цитотоксический иммунный: повреждение клеток и тканей (иммунная тромбоцитопения, гемолитическая анемия и др.);
- иммунокомплексный: воспаление суставов, почек, кожные проявления.
Существуют также реакции замедленного типа, которые не дают о себе знать сразу же при контакте с раздражителем. Через двое суток аллерген соединяется с лимфоцитами, что приводит к развитию инфекционно-аллергического заболевания, например, хронического нейродермита.
Как устранить проявления аллергии
Чем больше выделилось свободного гистамина, тем сильнее выражена аллергическая реакция. В одних случаях она доставляет неудобство (постоянное чихание, зуд в глазах), в других – представляет угрозу жизни (при бронхоспазме человек не может дышать). Остановить реакцию можно:
- прекратив контакт с аллергеном;
- нейтрализовав гистамин с помощью антигистаминного препарата;
- симптоматической терапией (например, ингаляцией для моментального расширения просветов бронхов).
В случае развития анафилактического шока, сопровождающегося уменьшением кровотока и отеком гортани, важно оперативно устранить угрозу жизни. В комплекс мер входят введение адреналина и обеспечение поступления воздуха в легкие (интубация).
Виды антигистаминных препаратов
Препараты первого поколения могли заблокировать сигналы гистаминовых рецепторов только после проникновения за барьер между кровеносной и центральной нервной системами. В результате нельзя было избежать воздействия на ЦНС. Из-за этого антигистамины вызывали сонливость и потерю координации.
Фармакологи учли этот недостаток при создании препаратов второго поколения. Они за упомянутый барьер не проникают, действуют избирательно, седативного эффекта не оказывают.
Антигистамины третьего поколения являются метаболитами своих предшественников. Они дают тот же эффект при меньшей дозировке и не влияют на работу сердечно-сосудистой системы. Однако некоторые аллергологи и иммунологи не согласны с выделением их в отдельную группу и причисляют ко второму поколению.
В 2015 году рабочая группа Консенсуса по антигистаминным препаратам нового поколения под руководством профессора С.Т. Холгейта пришла к выводу, что ни один из существующих препаратов не может быть отнесен к третьему поколению.
Примеры АГП разных поколений
АГП 1 поколенияАГП 2 поколенияАГП 3 поколения*ДимедролЛоратадинЦетиризинТавегилКларитинЗиртекСупрастинКестинЦетринДрамаминВизин и Тизин АлерджиТелфастДиазолинАллергодилФексофенадинАтаркcФенистилАллерфекс
*по мнению сторонников их существования
Применение блокаторов Н2-рецепторов гистамина в гастроэнтерологии
Охлобыстин А.В.
Блокаторы Н2-рецепторов гистамина до сих пор являются одними из наиболее распространенных лекарственных препаратов, которые используются при лечении язвенной болезни. Это связано прежде всего с их выраженными антисекреторными свойствами, но кроме того, Н2-блокаторы подавляют базальную и стимулированную выработку пепсина, увеличивают продукцию желудочной слизи, повышают синтез простагландинов в слизистой желудка, увеличивают секрецию бикарбонатов, улучшают микроциркуляцию в слизистой оболочке, нормализуют моторную функцию желудка и двенадцатиперстной кишки. Обнаружено также положительное влияние Н2-блокаторов на нормализацию ультраструктурных показателей желудочного эпителия [1].
Первые препараты данного класса были синтезированы в 1972 г., однако они имели большое количество побочных эффектов, в частности, токсическое влияние на костный мозг [8]. В то же время циметидин — первый препарат, вошедший в широкую клиническую практику, также обладает серьезными побочными действиями. Так, введение этого препарата стимулирует секрецию пролактина, что может вызывать появление гинекомастии; наблюдается снижение уровня инсулина в плазме крови, что вызывает появление сниженной толерантности к глюкозе на фоне приема циметидина [8]. Циметидин блокирует также периферические рецепторы мужских половых гормонов [3], он может вызвать повышение тестостерона в крови, оказывать гепатотоксическое действие (снижение кровотока в печени, повышение уровня трансаминаз), блокирование системы цитохрома Р-450, повышение уровня креатинина в крови, поражение центральной нервной системы, гематологические изменения, кардиотоксические эффекты, иммуносупрессивное действие [7].
Изменение внутрижелудочного рН у больных язвенной болезнью двенадцатиперстной кишки после однократного приема 200 мг циметидина внутрь исследовал В. Матов [4]. Начало ответа рН наблюдалось в среднем через 45 минут после приема таблетки циметидина, эффект достигал максимума через 135 минут и продолжался в течение 3,5 часов. Во время действия препарата в теле желудка рН поддерживался на уровне выше 3,0 ед (т.е. на слабокислом уровне, необходимом для заживления язв желудка и двенадцатиперстной кишки), в антральном отделе — выше 5,0 ед в течение 2 ч 45 мин. Эффективность циметидина в значительной степени зависит от исходного уровня кислотности: активность препарата была значительно более высокой у больных с нормацидностью (8 человек) и компенсированной гиперацидностью (11 человек) по сравнению с пациентами, у которых наблюдалась декомпенсированная гиперацидность (11 человек). При декомпенсированной гиперацидности внутрижелудочный рН превышал 3,0 ед в теле желудка лишь в течение 0,5 ч, а 5,0 ед в антральном отделе — в течение 1 ч. У остальных пациентов удавалось поддерживать рН в желудке на этих уровнях в течение 3,5 часов. В другом исследовании прием 1 таблетки (200 мг) циметидина вызывал повышение внутрижелудочного рН у больных язвенной болезнью двенадцатиперстной кишки уже через 30 минут с достижением максимального значения 8,26±0,77 ед через 90 минут. Уровень рН сохранялся на щелочных значениях в течение 2,5 часов [9].
На фоне приема циметидина в дозе 800-1000 мг в сутки рубцевание язв двенадцатиперстной кишки через 4 недели наблюдалось у 78% больных [2]. Применение циметидина у больных язвенной болезнью двенадцатиперстной кишки вызывает рубцевание язв через 3 недели у 58,8% пациентов, средние сроки рубцевания составляют при этом 27,3±3,4 дня [8].
Низатидин при однократном приеме в дозе 300 мг на ночь вызывал достоверное повышение среднего рН тела желудка у больных с дуоденальными язвами как за ночной период, так и за полные сутки по сравнению с записью до лечения [23].
На выраженность эффекта Н2-блокаторов оказывают влияние время их приема и зависимость от приема пищи. При относительно раннем приеме низатидина и раннем ужине (18.00) достигался достоверно более высокий уровень рН за 21 час (2,50 ед) по сравнению с ранним приемом препарата и поздним ужином (21.00) [14].
Прием ранитидина по 150 мг 2 раза в сутки способствует восстановлению спонтанного ночного защелачивания желудка у больных язвенной болезнью [12]. Прием Н2-блокаторов в дозах, превышающих средние (напр., по 300 мг ранитидина 2 раза в сутки), позволяет добиться антисекреторного эффекта, сопоставимого с таковым омепразола [15], что подтверждает положение о взаимосвязи между выраженностью антисекреторного и противоязвенного эффектов. Было показано, что у курящих больных Н2-блокаторы менее эффективно подавляют секрецию соляной кислоты [31].
Средние сроки исчезновения болей в животе при приеме 300 мг ранитидина в сутки составляют 2,6±0,5 дня. Прием 300 мг ранитидина в сутки, по данным разных авторов, обеспечивает рубцевание язв двенадцатиперстной кишки у 46-60% больных через 2 недели лечения и у 74-89% — через 4 недели [18,19].
Фамотидин (Квамател) относится к 3-му поколению блокаторов Н2-рецепторов гистамина. Этот препарат может использоваться у больных с почечной недостаточностью (в более низких дозах — в соответствии со степенью снижения клиренса креатинина). Известно, что фамотидин превосходит по своей активности ранитидин, роксатидин и циметидин. Доза фамотидина, равная 5 мг, эквивалентна 300 мг циметидина. Эффект циметидина, ранитидина и фамотидина наступает примерно в одинаковые сроки после приема, однако продолжительность действия фамотидина значительно больше — в 2 раза по сравнению с циметидином [10]. После внутривенного ведения 20 мг фамотидина период полужизни препарата составляет 3,8 ч [17]. Широкое применение, которое находит фамотидин в современной клинической практике, связано с тем, что этот препарат имеет очень небольшое количество побочных эффектов. Фамотидин на оказывает гепатотоксического действия, не блокирует систему цитохрома Р-450, не повышает уровень креатинина в плазме, не проникает через гематоэнцефалический барьер и не вызывает нервно-психических нарушений. При ежедневном приеме 40 мг фамотидина в течение 4-х недель не происходит изменения уровней пролактина, тестостерона, фолликулостимулирующего и лютеинизирующего гормонов. После перорального приема 40 мг фамотидина или внутривенного введения 20 мг препарата не происходит изменения уровня артериального давления, частоты сердечных сокращений и картины ЭКГ. Прием фамотидина в дозе 40 мг дважды в сутки не нарушает процесс эвакуации из желудка и не влияет на функцию поджелудочной железы. Как свидетельствует H.-G. Dammann [13], на основании данных о применении фамотидина в дозе 40 мг/сут у 10814 больных в Германии, вздутие живота возникает лишь в 1,17 % случаев, запоры — в 0,20 %, поносы — в 0,31 %, кожные реакции — в 1,12 %.
У здоровых добровольцев однократный прием фамотидина в дозе от 5 до 20 мг вызывал снижение базального кислотообразования соответственно на 94 и 97% (J.L. Smith и соавт. [209] и R.W. McCallum и соавт. [1,6,7]). Продукция соляной кислоты после стимуляции пентагастрином снижалась соответственно на 41-90%. Фамотидин в разовой дозе 10 и 20 мг оказывал достоверно более выраженное ингибирующее действие на выработку соляной кислоты в желудке по сравнению с циметидином в дозе 300 мг (р<0,05). По свидетельству R. Ryan [22], пероральный прием 20 и 40 мг фамотидина обеспечивает эффективный контроль секреции соляной кислоты в течение 9,5 часов. Прием 20 мг фамотидина в 20 ч на ночную секрецию соляной кислоты у 10 здоровых лиц вызвал снижение продукции соляной кислоты по сравнению с приемом плацебо на 93,8 % (p<0,01), которое сохранялось в течение 12 часов (Y. Fukuda и соавт. 1987). После перорального приема 1 таблетки фамотидина (40 мг), покрытой оболочкой, повышение рН более 3,5 ед в теле желудка у здоровых добровольцев наступает через 56,5 мин, после этого происходит стабилизация рН на протяжении 11 часов [20].
Исследования, которые выполнялись с использованием внутривенных инъекций фамотидина, также показали высокую эффективность этого препарата. Тем не менее в исследовании L.S. Welage (1988) наблюдалась достоверно более высокая эффективность фамотидина в дозе 20 мг дважды в день по сравнению с циметидином в дозе 300 мг 4 раза в день при внутривенном введении у 42-х больных отделения интенсивной терапии (p<0,001). В работе A. Al-Quorain и соавт. (1994) показана более высокая эффективность фамотидина по сравнению с ранитидином при внутривенном введении больным, находящимся в критическом состоянии. При введении 20 мг фамотидина каждые 12 часов уровень рН желудочного сока был достоверно выше (p<0,05), чем при введении 50 мг ранитидина каждые 8 часов.
При внутривенном введении 20 мг фамотидина здоровым испытуемым начало действия препарата наблюдалось в среднем через 36,3±11,9 мин, если инъекция проводилась в 14.00, и через 53,6±22,3 мин при введении в 20.00. Продолжительность действия препарата составляла 6,0±1,1 ч и 11,4±1,6 ч соответственно [16]. Данные, которые были получены в ходе исследования с помощью двойного слепого метода при внутривенном капельном введении фамотидина в дозе 3,2 или 4 мг/час, показывают высокую эффективность данного препарата как в периоды между приемами пищи, так и на высоте пищеварения [21].
Фамотидин обладает клинической эффективностью. Так, у больных язвенной болезнью при приеме препарата в дозе 40 мг/сут боли в животе исчезают в среднем через 2,4±0,8 дня. При использовании Кваматела у группы больных язвенной болезнью (11 больных язвенной болезнью двенадцатиперстной кишки, 3 больных язвенной болезнью желудка) в дозе 40 мг однократно на ночь уменьшение болей в животе наблюдалось в среднем через 3,9 дня, исчезновение — через 6,8 дня. У двух пациентов боли полностью не купировались в течение 14 дней терапии. В сроки до 2-х недель язвы зарубцевались у 13 больных (93%). Применение фамотидина в дозе 40 мг/сут в качестве монотерапии у больных язвенной болезнью двенадцатиперстной кишки вызывает исчезновение болей в животе в среднем через 7,8±4,6 дней, пальпаторной болезненности — через 9,6±5,3 дня, рубцевание язв — через 20,5±2,2 дня (сроки достоверно более короткие по сравнению с контрольной группой, получавшей терапию холинолитиками, антацидами, репарантами) [6]. Прием фамотидина в дозе 40 мг/сут позволяет достичь рубцевания язв двенадцатиперстной кишки в течение 4 нед. у 79-95% больных, в течение 6 нед. — у 95-97%. По другим данным фамотидин в дозе 40 мг/сут вызывал рубцевание язв двенадцатиперстной кишки у 86,3% больных через 4 недели приема [5]. По данным А.А. Шептулина, прием Н2-блокаторов в средних дозах (ранитидин 300 мг/сут или фамотидин 40 мг/сут) вызывает рубцевание язв двенадцатиперстной кишки за 4 недели у 75-93% больных язвенной болезнью двенадцатиперстной кишки, при этом различий в терапевтической эффективности двух препаратов не наблюдается.
Поддерживающая терапия с использованием однократного приема Н2-блокаторов на ночь с успехом может использоваться для профилактики рецидивов язвенной болезни или для купирования симптомов гиперацидности. В течение 1 года симптомы обострения развиваются у 20% больных по сравнению с 60-70% больных, которые не получали лечения. Поддерживающий прием Н2-блокаторов достоверно снижает частоту развития осложнений язвенной болезни, в частности, достоверно снижает риск развития повторных кровотечений. В то же время следует учитывать, что при отмене приема язвенная болезнь рецидивирует с той же частотой, как и у больных, не получавших лечения. В связи с этим в настоящее время больным проводят эрадикацию инфекции H.pylori (в том числе и с использованием Н2-блокаторов), которая дает стойкий противорецидивный эффект. Интересно, что по данным некоторых исследователей применение фамотидина в схемах эрадикационной терапии столь же эффективно, как и использование омепразола [25].
Эффективность Н2-блокаторов неодинакова у различных групп пациентов, в частности, серьезным фактором, снижающим эффективность этих препаратов, является курение. Прием низатидина по 300 мг/сут у больных язвенной болезнью двенадцатиперстной кишки (21 человек) и желудка (4) привел к исчезновению болей в животе в среднем через 5,8±0,4 дня (от 2 до 12), при этом у некурящих больных наблюдалось более быстрое исчезновение болей — 3,2±0,2 (от 1 до 4 дней), чем у курящих — 7,6±0,6 (от 5 до 12 дней). Таким образом, курение оказывает влияние не только на возникновение язвенной болезни, но и ухудшает эффективность терапии. Как свидетельствуют данные The RUDER study group [11], факторами, определяющими более высокую частоту рецидивов язвенной болезни двенадцатиперстной кишки на фоне поддерживающего приема Н2-блокаторов (ранитидин в дозе 150 мг в сутки), являются наличие эрозий вне зоны локализации зарубцевавшейся язвы, курение в настоящем или прошлом и некоторые другие.
К сожалению, существует группа пациентов, резистентных к Н2-блокаторам гистамина (так же как и существуют больные, например, резистентные к ингибиторам протонной помпы). Резистентность к Н2-блокаторам наблюдается по клиническим данным у 15-25% всех больных язвенной болезнью. По данным лекарственной пробы с циметидином при внутрижелудочной рН-метрии это наблюдалось у 11,5% больных язвенной болезнью двенадцатиперстной кишки и хроническим гастродуоденитом.
При лечении язвенной болезни у большинства пациентов бывает достаточно приема Н2-блокаторов 1 или 2 раза в сутки. При этом состояния, которые сопровождаются более выраженной гиперацидностью, такие как синдром Золлингера-Эллисона, требуют более частого назначения — каждые 4 часа.
Частый прием блокаторов Н2-рецепторов гистамина у больных рефлюкс-эзофагитом приближает их эффективность к действию омепразола. Н2-блокаторы позволяют достоверно уменьшить изжогу, хотя эндоскопические признаки эзофагита стихают лишь у 60% больных через 12 недель терапии. Использование Н2-блокаторов при рефлюкс-эзофагите по эффективности находится на одном уровне с монотерапией цизапридом и может быть рекомендовано у больных эзофагитом легкой степени тяжести. Кроме того, добавление Н2-блокаторов в вечернее время к терапии ингибиторами протонной помпы позволяет лучше контролировать ночные симптомы гастроэзофагеальной рефлюксной болезни [24].
Н2-блокаторы находят применение при лечении больных хроническим панкреатитом, поскольку угнетение желудочной секреции уменьшает освобождение секретина слизистой оболочкой двенадцатиперстной кишки и в результате снижается объем секрета поджелудочной железы, уменьшается внутрипротоковая гипертензия. С этой целью используют двукратный прием Н2-блокаторов в дозах, применяемых для лечения язвенной болезни (например, по 20 мг фамотидина в утренние часы + 40 мг в вечернее время).
Блокаторы Н2-гистаминовых рецепторов широко применяются в ревматологии для профилактики образования «лекарственных» язв двенадцатиперстной кишки и желудка (в более высоких дозах) у больных, принимающих нестероидные противовоспалительные препараты. При этом они более эффективны, чем антациды, сукральфат и простагландины (мизопростол).
Таким образом, несмотря на появление новых, более мощных антисекреторных препаратов, таких как ингибиторы протонной помпы, Н2-блокаторы остаются широко распространенной группой средств, которые находят применение во многих областях гастроэнтерологии, прежде всего благодаря очень привлекательному соотношению цена/эффективность.
Литература 1. Дамианов Б., Матов В., Жейнова Д. Ултраструктурни механизми на на антиацидния эфект на биомет при болни с дуоденална язва // Вутр.Болес.- 1985.- т.24.- №1.- с. 22-30. 2. Дегтярева И.И., Семеунович С., Харченко Н.В. и др. Возможности применения современного антисекреторного препарата омепразола // Клин. мед. — 1994.- т. 72.- №6.- С.38-40. 3. Дедов И.И., Шилин Д.Е., Арефьева О.А. Эндокринные эффекты циметидина // Клин. мед.- 1993.- т. 71.- №2.- С. 11-16. 4. Матов В. Эфект на еднократна доза симетидин «Фармахим» вурху рН на стомаха // Вутр. Болес.- 1987.- т.26.- №3.- с. 50-56. 5. Мягкова Л.П., Голочевская В.С., Лапина Т.Л. Блокаторы Н2-гистаминовых рецепторов 2-3-го поколений в лечении язвенной болезни // Клин. фармакология и терапия.- 1993.- №2.- с. 33-35. 6. Огурцов П.П., Жарков О.Б., Моисеев В.С. Сравнение эффективности ульфамида и энпростила в лечении язвенной болезни // Клин. фармакология и терапия.- 1993.- №2.- с. 22-25. 7. Серебрянская М.В., Масенко В.П. Динамика содержания простагландина Е у больных язвенной болезнью двенадцатиперстной кишки при различных видах лечения // Клин. мед.- 1993.- т.71.- №71.- С. 45-47. 8. Смагин В.Г., Минушкин О.Н., Булгаков С.А. и др. Опыт лечения язвенной болезни двенадцатиперстной кишки блокаторами Н2-гистаминовых рецепторов / Тер. архив.- 1986.- том 58.- №2.- С. 25-30. 9. Циммерман Я.С., Сыман Л.Н., Голованова Е.С. Опыт объективной оценки действия циметидина — блокатора Н2-рецепторов гистамина — у больных язвенной болезнью двенадцатиперстной кишки. // Тер. архив.- 1986.- т. 58.- №2.- С. 31-35. 10. Шептулин А.А. Современные антисекреторные препараты в лечении язвенной болезни // Клин. мед.- 1994.- т. 72.- № 1.- стр. 12-15. 11. Armstrong D., Arnold R., Classen M. et al., The RUDER Study group RUDER — a prospective, two-year, multicenter study of risk factors for duodenal ulcer relapse during maintenance therapy with ranitidine // Dig Dis Sci.- 1994.- vol 39.- P.1425-1433. 12. Bianco A., Cagossi M., Piraccini R., Greco A.V. Twenty four hour intragastric pH metry: H2-receptor antagonist restoration of nightly gastric spontaneous alkalinization in duodenal ulcer healing. // Riv. Eur. Sci. Med. Farmacol.- 1992.- vol.14.- ?5.- P. 281-291. 13. Dammann H.-G. et al. Compatibility profile of famotidine. In Famotidine heute (Dammann H.-G. et al., eds). Springer-Verlag, Berlin.- 1989, P. 93-102. 14. Duroux P., Emde C., Bauerfeind P. et al. Early evening nizatidine intake with a meal optimizes the antisecretory effect. // Aliment. Pharmacol. Ther.- 1993.- Feb; ?7(1).- P. 47-54. 15. Fiorucci S., Santucci L., Morelli A. Effect of omeprazole and high doses of ranitidine on gastric acidity and gastroesophageal reflux in patients with moderate-severe esophagitis // Am. J. Gastroenterol.- 1990.- ?85 (11) P. 1458-1462. 16. Gladziwa U., Wagner S., Dakshinamurty K.V. et al. Intragastric long-term pH-metry in hemodialysis patients: A study with famotidine. // Clin. Nephrol.- 1991.- Aug; ?36 (2).- P. 97-102. 17. Gladziwa U., Wagner S., Dakshinamurty K.V. et al. Pharmacokinetics and pharmacodynamics of famotidine in patients with reflux oesophagitis. // Eur. J. Clin. Pharmacol.- 1993.- ? 44(4).- P. 357-360. 18. Licht H., Lemaire M. Lansoprasole versus ranitidine in duodenal ulcer (DU): a French multicenter study // Gastroenterology.- 1992.- vol.98.- A78. 19. Londong W., Barth H., Damman H.G. et al. Dose-related healing of duodenal ulcer with the proton pump inhibitor lansoprasole // Aliment. Pharmacol. Ther.- 1991.- vol. 5.- P. 245-254. 20. Loser C., Burlage M., Folsch U.R. Einfluss von Ranitidin und Famotidin auf das intragastrale pH-Profil von gesunden Probanden. Randomisierte Cross-over-Prufung mit Ranitidin-Brausetabletten (300 mg) versus Famotidin-Filmtabletten (40 mg). // Arzneimittelforschung.- 1994.- May ?44 (5).- P. 626-629. 21. Merki H.S., Witzel L., Walt R.P. et al. Double blind comparison of the effects of cimetidine, ranitidine, famotidine and placebo on intragastric acidity in 30 normal volunteers // Gut.- 1988,- N29.- P.81-84. 22. Ryan R. Clinical pharmacology of phamotidine: Summary of data from the United States // Ital. J. Gastroenterolgy.- 1984.- ?16.- P. 171-174. 23. Savarino V., Mela G.S., Zentilin P. et al. Lack of gastric acid rebound after stopping a successful short-term course of nizatidine in duodenal ulcer patients. // Am. J. Gastroenterol.- 1991.- vol.86.- ?3.- P. 281-284. 24. Xue S, Katz PO, Banerjee P, Tutuian R, Castell DO. Bedtime H2 blockers improve nocturnal gastric acid control in GERD patients on proton pump inhibitors. Aliment Pharmacol Ther 2001 Sep;15(9):1351-6 25. Hsu CC, Chen JJ, Hu TH, Lu SN, Changchien CS. Famotidine versus omeprazole, in combination with amoxycillin and tinidazole, for eradication of Helicobacter pylori infection. Eur J Gastroenterol Hepatol 2001 Aug;13(8):921-6
Особенности действия антигистаминных препаратов
Антигистамины первого поколения не ограничиваются угнетением деятельности ЦНС. Они блокируют рецепторы разных нейромедиаторов, а не только гистамина, поэтому имеют ряд побочных эффектов:
- учащение пульса;
- тошноту и рвоту;
- повышение глазного давления;
- боли в желудке;
- нарушение мочеиспускания;
- сухость слизистых оболочек.
При длительном приеме пациент может терять вес, впадать в состояние перевозбуждения, терять сознание. При передозировке возможны судороги.
АГП второго поколения действуют более избирательно, а потому их прием не вызывает нежелательных реакций со стороны других органов, кроме сердца. Пациентам следует учесть риск синусовой и рефлекторной тахикардии, а также аритмии.
Н1‑блокаторы II поколения
Антигистаминные препараты II поколения были разработаны для устранения недостатков их предшественников. В отличие от последних, современные Н1‑блокаторы связываются и диссоциируют с Н1‑рецепторами медленно. Благодаря продолжительной связи с гистаминовыми рецепторами они способны обеспечивать длительный эффект, позволяющий применять их 1–2 раза в сутки. Доказано, что при регулярном приёме всех препаратов II поколения на протяжении месяца их терапевтический ответ не снижается, то есть тахифилаксия не развивается.
Показания
Неседативные антигистаминные препараты являются препаратами первой линии для лечения лёгких и умеренных форм аллергического ринита. Их уместно рекомендовать клиентам с незначительными симптомами аллергических заболеваний, а также аллергией средней тяжести.
Преимущества
Будучи сопоставимыми с первыми Н1‑блокаторами по антиаллергической активности, представители II поколения не проявляют седативный эффект и многие другие неблагоприятные реакции, что связано с их высокой селективностью и значительно меньшей способностью проникать через гематоэнцефалический барьер.
К преимуществам следует отнести длительное действие, возможность однократного применения в сутки, а также отсутствие тахифилаксии.
Переносимость
Несмотря на очевидные преимущества, некоторые препараты II поколения обладают редким, но серьёзным побочным эффектом, — способность вызывать нарушения сердечного ритма в виде удлинения интервала QT, развития желудочковой ари), атриовентрикулярной блокады и блокады ножек пучка Гиса. Подобные аритмии проявляются эпизодами головокружения, обмороками, однако нередко могут протекать бессимптомно.
Кардиотоксический эффект носит дозозависимый характер. При применении препаратов в терапевтических дозах аритмогенные свойства практически не проявляются. Это связано с тем, что большинство антигистаминных II поколения представляют собой пролекарства, которые почти не определяются в кровотоке из‑за быстрой биотрансформации с образованием активных и длительно действующих метаболитов. Следует отметить, что биотрансформация антигистаминных препаратов II поколения происходит с помощью изофермента системы цитохрома Р450, активность которого могут угнетать некоторые препараты, в частности, кетоконазол, итраконазол, флуоксетин, флавоноид, содержащийся в соке грейпфрута и ряд других.
При передозировке, повышении концентрации пролекарства в крови, а также состояниях, при которых снижается скорость биотрансформации препарата (например, циррозе печени, одновременном назначении с препаратами, угнетающими активность изофермента системы цитохрома Р450), выраженность кардиотоксического эффекта Н1‑блокаторов II поколения увеличивается. Дополнительными факторами риска служат уже существующий синдром удлинённого интервала QT, одновременный приём препаратов с аритмогенной активностью, электролитные нарушения.
В то же время при правильном применении, соблюдении режима дозирования и противопоказаний антигистаминные II поколения хорошо переносятся и могут считаться безопасными для лечения аллергических заболеваний.
Аритмогенных свойств лишены лоратадин — как сам препарат, так и его активный метаболит, — а также дезлоратадин и фексофенадин. Кстати, последние не метаболизируются с участием изофермента системы цитохрома Р450 и не вступают в лекарственные взаимодействия с препаратами, угнетающими его активность.
О чём предупредить клиента?
Отпуская препараты этой подгруппы, важно напомнить о необходимости соблюдения режима дозирования во избежание развития побочных эффектов, в частности, кардиотоксического действия.
Кроме того, уместно обратить внимание клиента на то, что антигистаминные II поколения не следует принимать одновременно с препаратами, которые конкурируют с ними за печёночный метаболизм (кетоконазол, итраконазол, ранитидин, флуоксетин и другие).
Антигистамины и желудок
Сам по себе гистамин активизирует выработку желудочного сока. Поэтому есть мнение, будто его блокировка угнетает секрецию. Это не совсем так. Для устранения симптомов аллергической реакции используются H1-блокаторы. Выработку желудочного сока могут уменьшить H2-блокаторы:
- Циметидин;
- Ранитидин;
- Фамотидин;
- Роксатидин.
Это другая группа антигистаминных препаратов, используемых для лечения гастрита, язвенной болезни желудка, рефлюкс-эзофагита. Аллергики ими не пользуются. Поэтому нарушить пищеварение в попытке борьбы с крапивницей или конъюнктивитом риска нет.
Механизм действия Н2-блокаторов и показания к применению
На мембране внутри стенки желудка расположены гистаминовые (Н2) клеточные рецепторы. Это париетальные клетки, которые в организме причастны к выработке соляной кислоты.
Ее чрезмерная концентрация вызывает нарушения в функционировании пищеварительной системы и приводит к язве.
Вещества, которые содержатся в Н2-блокаторах
, имеют свойство снижать уровень выработки желудочного сока. Также они угнетают уже готовую кислоту, выработка которой спровоцирована потреблением пищи.
Блокирование гистаминовых рецепторов снижает выработку желудочного сока и помогает справляться с патологиями пищеварительной системы.
В связи с оказываемым действием, Н2-блокаторы назначают при таких состояниях:
- язва (как желудка, так и двенадцатиперстной кишки);
- стрессовая язва — вызванная тяжелыми соматическими заболеваниями;
- язва, возникшая на фоне длительного приема нестероидных противовоспалительных или кортикостероидных препаратов;
- острый панкреатит и обострение хронического;
- в сочетании с ферментными панкреатическими препаратами, с целью их защиты от разрушающего воздействия желудочного сока.
Дозировка и длительность приема Н2-антигистаминных лекарственных препаратов при каждом из перечисленных диагнозов назначается индивидуально.