Противопоказания для коронарной ангиопластики
Существуют полные и относительные противопоказания к проведению такого типа вмешательства. Итак, абсолютные противопоказания для указанной операции:
- Если участок сужения находится в стволе левой артерии, питающей сердце.
- Когда сужение находится в участке артерии, по которой кровь поступает к не пораженному миокарду.
- Если пациент отказывается от такого лечения.
К относительным противопоказаниям можно отнести следующее:
- Тяжелые случаи дисфункции левого желудочка.
- Поражение многих сосудов, при котором наблюдается сложная дисфункция сердечной мышцы.
- Стойкое поражение коронарной артерии, из-за чего нарушается снабжение кровью большого участка миокарда.
- Неконтролируемое или же нестабильное нарушение системного типа. Например, если у больного диагностирована недостаточность функционирования почек, перенесенный апоплексический удар, кровотечение из желудочно-кишечного тракта, лихорадка, вызванная тяжелым инфекционным процессом.
- Плохо контролируемая или терминальная артериальная гипертензия.
- Нарушения обмена электролитов.
- Анафилактические нарушения.
Что такое прямая реваскуляризация
Бывает прямая и непрямая операция. Под прямой реваскуляризацией подразумевается аортокоронарное шунтирование, баллонная ангиопластика и коронарный вид стентирования.
Непрямая же реваскуляризация – это способ восстановления кровообращения в небольших артериях, питающих миокард. Чаще всего проводится операция с использованием лазерного луча. Рассмотрим подробнее особенности аортокоронарного шунтирования.
Это очень сложная и дорогая операция. Ее могут выполнять только высококвалифицированные врачи. В ходе вмешательства специалист образует анастомоз между аортой и артерий, которая поражена болезнью.
К такой операции человека надо тщательно готовить. Необходимо стабилизировать у него количество сердечных сокращений, уровень давления крови, показатель гликемии. Лучше, чем другие, переносят такое вмешательство пациенты в возрасте от 30 до 55 лет. Хотя в последнее время все более успешно проводятся подобные операции и у лиц более старшего возраста.
Шунт берется из подкожных вен (обычно бедренных или предплечных). Наложение шунта позволяет предотвратить необратимые изменения сердечной мышцы и увеличить продолжительность жизни.
Обычно шунт служит приблизительно пять лет. Существует, однако, высокий риск развития послеоперационных осложнений. У пациентов может развиться недостаточность сердца или произойти инфицирование раны. Операция не делается в таких случаях:
- выраженное общее тяжелое состояние;
- злокачественные процессы;
- гипертония;
- состояние после апоплексического удара;
- некоторые типы стенозов.
Прямые вмешательства на брахиоцефальных артериях при остром инсульте
КЭА при малых инсультах и ТИА
Профилактическая направленность КЭА, стремление хирургов нивелировать риск интра- и послеоперационных осложнений и летальности со временем обеспечили определенный статус этой операции. КЭА — это плановое хирургическое вмешательство у больных с нетяжелыми инсультами и отсутствием выраженной сопутствующей патологии. Еще сравнительно недавно КЭА была противопоказана пациентам в сроки до 6 нед после перенесенного инсульта и больным с сохраняющимся грубым неврологическим дефицитом [2]. Причиной отказа от ранних вмешательств являлась убежденность хирургов в высокой вероятности развития гиперперфузионного отека головного мозга, геморрагических осложнений и бесперспективности операции при тяжелых инсультах [2]. Однако риск повторных ишемических нарушений наиболее высок в первые дни и недели после появления симптомов инсульта, составляя 1-2% в первые 7 дней и 2-4% в первые 30 сут [12]. После проведения крупных международных исследований стало понятно, что профилактическая ценность КЭА снижается с увеличением срока до проведения хирургического вмешательства. Так, по данным исследования NASCET [13], повторные ОНМК развились у 9,5% пациентов, ожидавших КЭА [13]. Выполнение КЭА в ранние сроки (1-14 дней) после перенесенного инсульта позволяет предотвратить 1 инсульт у 5 пациентов в течение 5 лет наблюдения, а проведение операции позже 6 мес — 1 инсульт у 125 пациентов за тот же период наблюдения [3, 14]. Было установлено также, что ранняя КЭА у пациентов с малыми инсультами и ТИА не сопровождается повышенным риском ишемических и геморрагических осложнений [4, 5, 15]. Существуют работы, доказывающие безопасность и эффективность проведения КЭА в раннем периоде нетяжелого инсульта [3-5, 16-19]. Так, E. Ballotta и соавт. [18] провели анализ результатов лечения 102 пациентов с острыми инсультами. Операцию выполняли в первые 14 дней (медиана — 8 дней) больным со стабильным неврологическим дефицитом (отсутствует нарастание симптомов в течение 24 ч) и уровнем неврологических расстройств менее 2 баллов по шкале Рэнкина. Авторы показали, что лучшие исходы лечения были у пациентов с нетяжелым инсультом, отсутствием или наличием небольших очагов ишемии по данным компьютерной томографии (КТ). C. Peiper и соавт. [19] сравнили эффективность проведения 26 экстренных и 157 отсроченных (позже 14-х суток) КЭА у пациентов, перенесших малый инсульт. Показаниями для экстренной операции являлись наличие симптомов сосудисто-мозговой недостаточности и осложненная атеросклеротическая бляшка. Лучшие результаты получены у пациентов, оперированных в ранние сроки — случаев летальности и осложнений отмечено не было. У больных, оперированных в отдаленном периоде ОНМК, интра- и послеоперационные ишемические осложнения составили 3,8%, а летальность — 2,7%. По данным S. Annambhotla и соавт. [17], лучшие отдаленные результаты и меньшее количество послеоперационных осложнений наблюдаются у пациентов, оперированных в первые 30 дней после инсульта. Так, в группе пациентов, оперированных в ранние сроки, повторный ИИ был отмечен у 2,3% больных в течение 17 мес наблюдения, летальность в течение 5 лет составила 21%, а в группе пациентов, оперированных в отдаленном периоде (более 30 дней после ИИ), зарегистрировано 8,3% повторных ОНМК в течение 12 мес, летальность за 5 лет составила 30% [17].
КЭА при прогрессирующих инсультах (инсульт в ходу) и crescendo ТИА[1]
Вопрос о возможности и необходимости проведения КЭА у пациентов с прогрессирующим неврологическим дефицитом (инсультом в ходу), инвалидизирующим инсультом и crescendo ТИА (более 2 эпизодов ТИА в течение 24 ч) остается малоизученным и спорным. Крупных рандомизированных исследований, посвященных этой проблеме, нет.
В национальных рекомендациях указано, что у больных, перенесших полный инсульт, оперативное лечение целесообразно выполнять в срок от 6 до 8 нед от начала острого эпизода, однако отсутствует информация о тактике ведения инсульта в ходу и crescendo ТИА [1].
Основной целью проведения КЭА при прогрессирующем инсульте или crescendo ТИА является не только осуществление ранней профилактики повторных ишемических эпизодов, но и экстренное восстановление нормальной перфузии в зоне пенумбры для предотвращения дальнейшего нарастания неврологического дефицита. В данном случае КЭА представляет собой и профилактическую, и лечебную процедуру. Главным препятствием для рутинного использования таких операций является существующий риск геморрагических осложнений, который составляет 0-2% [6, 9, 21].
В последние годы интерес исследователей и хирургов к выполнению ранних КЭА при острых инсультах разных тяжести и течения растет. Обсуждаются сроки, показания, допустимый процент осложнений, техника операции, необходимость использования внутрипросветного шунта и расширяющей заплаты, оптимальные виды анестезиологического пособия у данной категории больных [6-10, 12, 22]. Так, S. Bruls и соавт. [8] считают, что течение инсульта в ходу и crescendo ТИА крайне неблагоприятны (летальность составляет 14-18%, инвалидизация достигает 31-71%) и допускают проведение экстренного хирургического вмешательства пациентам без нарушения сознания. L. Capoccia и соавт. [9] представили опыт лечения 48 пациентов с прогрессирующим инсультом (26 человек) и crescendo ТИА (23). Тяжесть состояния больных при поступлении в среднем составляла 5,3 балла по NIHSS, очаги ишемии при КТ были выявлены у 4 (15,3%) пациентов с инсультом и 8 (34,8%) — с повторными ТИА. Операцию выполняли в первые 24 ч (медиана — 10 ч) от появления ишемического эпизода. Исследователи отметили значительное улучшение функциональных исходов у большинства пациентов; средний уровень неврологических расстройств при выписке составил 0,54 балла по NIHSS. Послеоперационные осложнения наблюдались у 1 (2%) пациента в виде геморрагической трансформации ишемического очага, не выявленного при КТ, что привело к смерти больного.
По мнению R. Brandl и соавт. [7], показаниями для экстренной КЭА при остром прогрессирующем инсульте являются: наличие симптомов острого инсульта с нестабильным неврологическим дефицитом, но отсутствием расстройств сознания; наличие значительной каротидной патологии; отсутствие геморрагических изменений в веществе головного мозга; стабильные гемодинамика и респираторные функции у больного.
Продемонстрирована возможность выполнения экстренных КЭА пациентам со средним и тяжелым неврологическим дефицитом [6, 10, 11, 20]. Например, E. Sbarigia и соавт. [20] проанализировали результаты лечения 96 пациентов с острым ИИ и выраженным неврологическим дефицитом. Все пациенты были прооперированы в течение первых 2 сут от начала заболевания (медиана — 1,5 сут). От операции воздерживались у пациентов с тяжестью неврологических расстройств более 22 баллов по NIHSS и инфарктами головного мозга, распространяющимися более чем на ⅔ бассейна кровоснабжения соответствующей средней мозговой артерии (СМА). У 85 (88,5%) пациентов отмечено уменьшение неврологического дефицита в послеоперационном периоде. Комбинированный показатель «летальность + осложнения» составил 7,3%, геморрагических осложнений и увеличения объема ишемического очага не было.
L. Capoccia и соавт. [10] описали 62 наблюдения экстренных КЭА (медиана — 34 ч). Авторы отметили более значимую динамику регресса неврологического дефицита в группе пациентов с исходно более тяжелыми неврологическими расстройствами (более 8 баллов по NIHSS) в сравнении с пациентами с менее выраженными нарушениями (4-7 баллов по NIHSS).
Наряду со сторонниками активной хирургической тактики при остром тяжелом или нестабильном инсульте, ее противники заявляют о слишком высоком уровне послеоперационных осложнений и летальности. R. Huber и соавт. [23] и S. Welsh и соавт. [13] сообщили о 16% летальности и 21% осложнений у данной категории больных. K. Rerkasem и соавт. [24] изучили 47 источников литературы, посвященных КЭА у пациентов с инсультом в ходу; по данным исследователей, проведение операции в острой стадии инсульта может сопровождаться осложнениями в 20,2% случаев и 11,4% летальностью. Согласно последним рекомендациям американской ассоциации инсульта (AHA/ASA) [25], экстренную КЭА при тяжелых инсультах и нестабильном неврологическом дефиците необходимо выполнять только с целью устранения причины острого тромбоза или дефицита кровотока. КЭА не показана при обширном инсульте в связи с высоким риском повреждения ткани мозга при восстановлении кровотока.
H. Bazan и соавт. [26] изучали факторы, влияющие на исходы экстренных КЭА. Летальные исходы и ишемические осложнения при экстренных вмешательствах встречались чаще, чем в группе пациентов, перенесших плановые операции: летальность — 2,0 и 0,3%, ИИ — 2,9 и 1,1% соответственно. Количество кардиологических осложнений было статистически сопоставимо в обеих группах и составило 2,2-3,0%. У пациентов с тяжелой сопутствующей патологией риск послеоперационных осложнений и летальности был значительно выше — 10,9 и 7,8% в рассматриваемых группах. Авторы заключили, что риск экстренной КЭА выше у пациентов с высокой коморбидностью; эти пациенты требуют тщательного отбора и лечения в крупных многопрофильных центрах. По данным G. Leseche и соавт. [27], среди 27 пациентов с острым прогрессирующим инсультом наиболее распространенной соматической патологией были артериальная гипертензия — 77,7%, курение в анамнезе — 70,3%, гиперхолестеринемия — 63,0%, хронические обструктивные заболевания легких — 40,7%, мерцательная аритмия — 18,5%, стенокардия — 14,8%, болезни почек — 14,8%. Всем больным была выполнена экстренная КЭА. Послеоперационное осложнение имело место у 1 (3,7%) больного, у которого развился нефатальный инфаркт миокарда. Летальных исходов не было.
Селективное внутрипросветное шунтирование при остром инсульте является предметом дискуссии в литературе; существуют работы, указывающие на необходимость обязательного внутрипросветного шунтирования во время КЭА. Использование данной методики обеспечивает дополнительную защиту ткани мозга от ишемии и гемодинамического удара после пуска кровотока [28]. Использование расширяющей заплаты при закрытии артериотомического дефекта у экстренных пациентов предпочитают большинство хирургов, ссылаясь на лучшую профилактику сужения и тромбирования артерии [14, 28, 29]. С целью уменьшения риска интра- и послеоперационных осложнений предлагают также следующие технические действия: более широкий разрез мягких тканей; наличие готового к использованию внутрипросветного шунта; предварительное пережатие общей (ОСА) и наружной сонных артерий перед диссекцией каротидной луковицы для исключения тромбоэмболии; широкую артериотомию, достаточную для визуализации всей поверхности эндартерэктомии; пуск ретроградного кровотока из внутренней сонной артерии (ВСА) перед наложением зажима, если стеноз сопровождается наличием флотирующего тромба [27].
Экстренная тромбинтимэктомия (ТИЭ) при неокклюзионных тромбозах ВСА
Пристеночный, неокклюзионный, неполный тромбоз экстракраниальных отделов ВСА и ОСА — редкая патология, которая встречается у 0,5 — 0,9% пациентов с ОНМК и поражением брахиоцефальных артерий [16, 30, 31]. Как правило, страдают пациенты молодого и среднего возраста. Причинами возникновения неокклюзионного тромбоза могут служить атеросклероз, повреждение сосудистой стенки, активация тромбоцитов и факторов свертывания. Среди заболеваний, способствующих тромбообразованию, выделяют различные васкулопатии, антифосфолипидный синдром, системные заболевания соединительной ткани, болезни крови [16]. Несмотря на редкую встречаемость, пристеночный тромбоз, особенно в случае наличия флотирующего фрагмента тромба, является опасным состоянием, так как в 87,5-100% он приводит к тромбоэмболии и ишемическим нарушениям в головном мозге [16, 30, 31]. Применение дуплексного сканирования позволяет диагностировать неполный тромбоз в 62,5 — 100% случаев, а дигитальная субтракционная ангиография — в 100% [16, 30]. Компьютерная и магнитно-резонансная ангиография не способна выявить тромбоз у 33,4 и 66,7% пациентов соответственно [30].
До сих пор нет единой точки зрения на тактику лечения этого заболевания [16, 30, 31]. Существуют мнения о необходимости консервативного ведения таких пациентов [16, 31]. Так, Y. Inatomi и соавт. [31] наблюдали 14 пациентов с ИИ и пристеночным тромбозом ВСА; пациентов лечили консервативно с хорошими результатами. А.О. Чечёткин и О.В. Лагода [16] проанализировали исходы лечения 6 пациентов; 4 больных получали антикоагулянтную и антиагрегантную терапию, 2 — хирургическое лечение. Повторный тромбоз был отмечен у 1 (50%) больного после выполнения КЭА. Возможной причиной осложнения авторы считают гипергомоцистеинемию, выявленную у больного. В группе консервативного лечения у 3 (75%) пациентов достигнуты положительный эффект и регресс тромбоза в течение 1 мес лечения. E. Ferrero и соавт. [30], напротив, использовали хирургическую тактику у 16 пациентов с флотирующим тромбозом бифуркации ВСА. Всем пациентам была выполнена экстренная КЭА. У 75% больных отмечено улучшение неврологической симптоматики, послеоперационная летальность составила 6,25%.
Остается нерешенным также вопрос о безопасности выполнения КЭА после проведения тромболизиса при наличии остаточного значимого стеноза ВСА тромботическими массами [27, 29, 31].
М. Rubiera и соавт. [32] установили, что остаточный выраженный стеноз сонной артерии является независимым предиктором ранней реокклюзии прецеребральных и интракраниальных артерий.
G. Leseche и соавт. [27] прооперировали 7 пациентов после проведения тромболизиса, у 4 из которых отмечался флотирующий тромбоз ВСА. Уровень неврологических расстройств до операции в среднем составлял 9 баллов по NIНSS. Пациенты с флотирующим тромбозом получали предварительную терапию антикоагулянтами и были прооперированы под наркозом. Послеоперационных осложнений отмечено не было, у всех пациентов наблюдался частичный или полный регресс неврологической симптоматики (до 2 баллов и менее по шкале Рэнкина в течение 3 мес наблюдения). J. Crozier и соавт. [29] также подтверждают безопасность выполнения КЭА в срок от 1 до 22 сут после проведения тромболизиса. В своей серии наблюдений авторы отметили отсутствие летальности и серьезных осложнений.
Экстренная ТИЭ при окклюзионных тромбозах ВСА
Этиология острых окклюзионных и неокклюзионных тромбозов ВСА похожа, однако есть и различия. Частота окклюзионного тромбоза ВСА достигает 1,9% среди пациентов с ИИ, ему больше подвержены пациенты среднего и пожилого возраста, а основными причинами являются атеросклеротическое поражение, диссекция интимы артерии, кардиоэмболия [16, 33, 34]. Острая окклюзия ВСА может протекать бессимптомно, а может стать причиной мозговой катастрофы [2, 16]. Согласно немецкому мультицентровому исследованию [35], среди 4157 пациентов, перенесших инсульт, 366 (8,8%) имели острую окклюзию ВСА. Из них у 7,4% было отмечено возникновение повторных ишемических эпизодов в течение первых 72 ч наблюдения. Летальность составила 21,2% в первые 3 мес заболевания.
В последние годы в связи с развитием нейровизуализационных и интервенционных методик с помощью эндоваскулярной экстракции тромба стало возможным добиваться восстановления просвета артерии у 53-63% пациентов. Существующие ограничения применяемых методов оставляют нерешенной проблему распространенных экстра-интракраниальных тромбозов, при которых летальность достигает 30-79% [33, 34, 36].
Рандомизированных исследований, посвященных открытой ТИЭ при острых окклюзиях ВСА, пока нет. В серии отдельных работ предлагаются следующие критерии отбора пациентов для хирургического лечения: наличие острой окклюзии экстракраниального отдела ВСА; выявление перфузионно-диффузионного дефицита по данным МРТ; первые 3 сут от начала заболевания. Противопоказаниями для операции считаются: глубокий неврологический дефицит, нарушение сознания, тяжелое соматическое состояние, очаги геморрагической трансформации, острый дефицит перфузии более чем в ⅓ бассейна СМА по данным МРТ, очаг инфаркта более 1 см по данным КТ, окклюзия интракраниального отдела ВСА, окклюзия СМА [33, 34].
G. Kasper и соавт. [33] в серии из 29 наблюдений показали успешные результаты ТИЭ в первые 39 ч от развития ишемического эпизода. Восстановление антеградного кровотока по ВСА получено у 83% пациентов. Частичный или полный регресс неврологической симптоматики отмечен у 48% пациентов; нарастание неврологического дефицита — у 7%; геморрагическая трансформация инсульта, послужившая причиной смерти, развилась у 3,6%.
B. Weis-Müller и соавт. [34] указывают на необходимость определения диффузионно-перфузионной разницы и проходимости супраклиноидных отделов ВСА у пациентов с острым инсультом (35 наблюдений). В данной серии наблюдений у 27 (77%) больных тяжесть неврологического дефицита соответствовала 3-5 баллам по шкале Рэнкина. Операцию выполняли в первые 72 ч от развития симптомов ишемии головного мозга. В предоперационном периоде 6 (17%) пациентам проведен тромболизис тканевым активатором плазминогена. ТИЭ выполняли из широкой артериотомии, по показаниям использовали катетер Фогарти и интраоперационную ангиографию. Восстановление антеградного кровотока по сонным артериям достигнуто у 30 (86%) пациентов, у 4 (11,4%) больных в связи с отсутствием ретроградного кровотока из дистальных отделов ВСА осуществлено ее лигирование. В послеоперационном периоде улучшение отмечено в 57% случаев, в 6% — нарастание неврологического дефицита. Летальность составила 6%, геморрагические осложнения наблюдали у 2 (6%) больных.
J. Berthet и соавт. [28] рекомендуют выполнять ТИЭ в первые 6 ч от развития окклюзии ВСА, использовать внутрипросветное шунтрирование и расширяющую пластику артерии у всех пациентов. Т. Murata и соавт. [37] представили опыт лечения 3 кардиоэмболических тромбозов ВСА, которые составили 0,47% от общей выборки пациентов с ОНМК (640 больных). У всех пациентов были выявлены тяжелый неврологический дефицит и мерцательная аритмия. Хирургическая реканализация достигнута в 100% наблюдений, у 2 (66,7%) пациентов отмечен регресс неврологической симптоматики.
Трофика миокарда — причины возникновения ишемической болезни
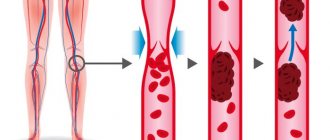
Как и любой другой орган, сердце нуждается в питании — сокращение этого органа требует значительное количество кислорода и энергии. Все эти вещества поступают по коронарным сосудам прямо к миокарду, что и обеспечивает стабильное снабжение сердца всеми необходимыми ему веществами. Однако на определенном этапе это благополучие заканчивается — из-за атеросклеротических бляшек, которые в значительных количествах скапливаются в просвете коронарных сосудов, происходит нарушение кровоснабжения сердца.
Все очень просто — коронарные сосуды становятся не в состоянии обеспечить долженствующий уровень кровотока, а потому возникает сердечная недостаточность, которая проявляется выраженным болевым синдромом (ишемической болезнью сердца).
При физической нагрузке, значительных эмоциональных переживаниях и действии некоторых других факторов болевой синдром значительно усиливается, что однозначно говорит в пользу того, что возрастающая нагрузка требует большего количества кислорода и питательных веществ, обеспечить которые закупоренные артерии не в состоянии.
- Операция при артрозе тазобедренного сустава
Читайте по теме: Дисметаболические изменения в миокарде — что это такое
До определенной степени использование нитроглицерина помогает снять эту симптоматику — под влиянием препарата происходит выраженная вазодилатация, что помогает пропустить кровь через патологически суженный сосуд, тем самым обеспечив должный объем трофики.
Однако подобного рода вмешательства допустимы до поры – до времени: иногда получается и так, что сосуд становится абсолютно непроницаем, и он полностью выводится из кровотока.
Никакие препараты ему уже не помогут — требуется проведение оперативного вмешательства, которое может быть выполнено несколькими путями:
- Коронарная реваскуляризация миокарда с применением ангиоплатики.
- Устранение бляшек различными способами (как правило, используется ультразвук, однако в последнее время стало популярно и лазерное вмешательство).
- Способ прямого воздействия на артерии путем установления специального стента, который будет поддерживать просвет коронарной артерии в открытом состоянии.
Давайте разберемся в том, что такое реваскуляризация миокарда, какие методы реваскуляризации миокарда существуют на сегодняшний день и для чего нужна коронарография сосудов сердца при выполнении аорто-коронарного шунтирования.
Лазерное лечение
На сегодняшний день существует множество людей с более сложными ишемическими заболеваниями, при которых хирургическое вмешательство будет считаться грубой ошибкой. Например, это касается людей, у которых развиты атеросклеротические бляшки, и находятся они практически во всех сосудах. В данном случае следует подобрать более эффективное лечение, такое как трансмиокардиальная лазерная реваскуляризация миокарда. Суть данного лечения заключается в том, что с помощью лазера создаются специальные каналы, по которым поступает к сердцу кровь, со всеми полезными веществами. Стоит сказать, что диаметр таких каналов не превышает 1 мм, этого вполне достаточно, чтобы достичь положительного результата.
Если говорить об эффективности данной процедуры, то ее действие в силе на протяжении 2 лет, даже, несмотря на то, что за это время некоторые каналы начинают закрываться. Необходимо уточнить, что лазерная реваскуляризация миокарда считается недоскональной, так как исследования этого метода продолжаются до сегодняшнего дня. Но, стоит сказать, что в большинстве случаев другого выхода просто нет.
Шунтирующие операции при остром инсульте
Пациенты с острым ИИ, имеющие острую окклюзию одной из основных церебральных артерий, при невозможности выполнения открытой или эндоваскулярной тромбэктомии могут рассматриваться в качестве кандидатов для проведения экстренных шунтирующих операций [38-40]. Возможности современных диагностических процедур позволяют в ранние сроки от начала заболевания верифицировать пораженный сегмент артерии, идентифицировать область ишемической полутени, очаг инфаркта, выраженность нарушений перфузии и цереброваскулярный резерв. Все это дает возможность определения показаний для выполнения успешной реваскуляризирующей операции. Основным хирургическим вмешательством у данной категории больных по настоящее время остается экстра-интракраниальный микроанастомоз (ЭИКМА) [38-42].
Показаниями к операции ЭИКМА при остром инсульте являются: доказанная окклюзия одной из несущих артерий; острый ИИ (первые 72 ч) со средним и тяжелым неврологическим дефицитом — более 4 баллов по NIHSS; инсульт в ходу; очаг инфаркта головного мозга менее 30 мл по данным диффузионно-взвешенной МРТ; диффузионно-перфузионная разница более 120%; неэффективность или противопоказания для выполнения тромболизиса [38, 39]. Противопоказаниями являются: тяжелая соматическая патология; отсутствие перфузионно-диффузионного дефицита и зоны пенумбры; очаги острой ишемии и отека головного мозга по данным КТ; геморрагическая трансформация [38, 39]. Одним из недавних крупных исследований является работа T. Horiuchi и соавт. [38], в которой авторы описали опыт выполнения 59 экстренных ЭИКМА у пациентов с острым инсультом, инсультом в ходу и crescendo ТИА. У 19 (32,3%) больных выявлена острая окклюзия ВСА, у 40 (67,7%) — окклюзия СМА. Операцию провели согласно представленным показаниям в первые 2 сут 35 (58,6%) больным.
В послеоперационном периоде у 40 (69%) пациентов отмечен частичный или полный регресс симптоматики. Исследователи отметили 6,9% случаев больших и 6,9% малых осложнений. Авторы указывают, что пол, возраст, сторона поражения, заинтересованная артерия, количество анастомозов, выполненных у одного пациента, не влияли на исход заболевания. В другом проспективном исследовании Y. Yoshimoto и S. Kwak [40] сравнили результаты лечения 35 оперированных и 35 неоперированных пациентов с острыми ишемическими нарушениями. Через 7 дней после ЭИКМА улучшение неврологического статуса отмечено у 15 (43%) пациентов, а в группе неоперированных больных — у 10 (29%). Отдаленные результаты лечения у пациентов с выраженным неврологическим дефицитом были значительно лучше в «хирургической» группе. G. Hwang и соавт. [39] проанализировали опыт выполнения 9 экстренных анастомозов и провели сравнительную оценку подобных операций по данным двух источников литературы, включавших 21 наблюдение. Хорошие исходы лечения получены в 83,3% случаев в общей выборке пациентов. Медианой тяжести неврологических расстройств у пациентов при поступлении являлась оценка в 12,4 балла по NIHSS, через 3 дня после операции — 8,6 баллов, при выписке — 5,4 балла, через 3 мес — 3,7 балла, геморрагических осложнений не было. По данным диффузионно-взвешенной МРТ, увеличения зоны инфаркта в послеоперационном периоде не наблюдали, очаг инфаркта в среднем составлял 15 см3. У всех пациентов также отмечен регресс полушарной асимметрии, измеренной по показателю пикового времени транзита крови. В пред- и послеоперационном периодах все пациенты получали антиагреганты, осуществлялся тщательный контроль стабильности гемодинамики. Исследователи заключили, что проведение реперфузии головного мозга с помощью выполнения низкопотоковых анастомозов (30-50 мл/мин) является менее травматичным и более безопасным вмешательством, чем выполнение реканализации крупного несущего сосуда с высокой объемной скоростью кровотока (100-150 мл/мин), которая может привести к нарушению гематоэнцефалического барьера в ишемизированном регионе и послужить причиной геморрагических осложнений [39, 43].