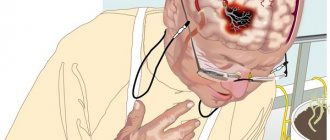
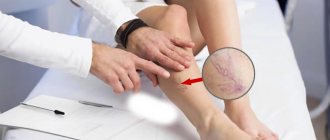
Нарушение кровотока по висцеральным артериям приводит к недостаточному поступлению крови к внутренним органам и, как следствие, к острому или хроническому нарушению их функции. Острое нарушение кровотока развивается при скоротечной закупорке сосуда тромбом либо фрагментами атеросклеротической бляшки. При этом орган, который питала артерия, не успевает компенсировать недостаток крови из соседних, свободных артерий. Например, при закупорке почечной артерии развивается инфаркт почки, при закупорке верхней брыжеечной артерии — омертвение участка тонкой кишки. При данных состояниях высока вероятность смертельного исхода, часто требуется неотложное оперативное лечение.
При хронических нарушениях кровотока (при сужении артерии либо сдавлении ее извне соседними анатомическими структурами) поступление крови к органу сохранено, но значительно снижено. Орган испытывает постоянный недостаток в кислороде и питательных веществах, происходит нарушение его функций, что проявляется симптомами, характерными для многих других заболеваний внутренних органов (хронический гастрит, язвенная болезнь желудка и двенадцатиперстной кишки, хронический панкреатит, колит). Некоторые органы, такие как желудок, поджелудочная железа, печень кровоснабжаются очень хорошо, что позволяет компенсировать недостаток кровотока. Однако, с течением времени, развивается декомпенсация самого органа либо патологические изменения в соседних органах — так называемый «синдром обкрадывания кровотока», когда кровь из общего сосудистого бассейна поступает туда, где есть большая потребность в компонентах крови, вследствие чего другим органам «не достается» обычного объема крови, они испытывают недостаток в кислороде и питательных веществах.
Кратко о методе лечения
Ангиопластика и стентирование чревного ствола и брыжеечных артерий применяется для лечения синдрома хронического нарушения кишечного кровообращения (angina abdomenalis) или при экстренной операции по поводу острого нарушения кровообращения кишечника (мезентериального тромбоза).
Нарушения кишечного кровообращения достаточно редко диагностируются без прицельного акцента на определенных жалобах и часто устанавливаются опытным клиницистом только после исключения других причин болей в животе.
Раньше при выявлении сужений чревного ствола или брыжеечных артерий хирурги придерживались консервативной выжидательной тактики, так как открытые операции на этих артериях очень сложны и тяжело переносятся пациентами. Сейчас, благодаря развитию эндоваскулярных технологий, стало возможно малотравматичное устранение проблем с висцеральными артериями.
Зачем делать стентирование чревного ствола и брыжеечной артерии
Внутри брюшной полости располагаются органы, которые отвечают за пищеварительные процессы. Они обильно снабжаются кровью крупными сосудами – чревным стволом, верхней и нижней брыжеечной и почечными артериями. Нарушение кровотока в этих артериях затрудняет работу внутренних органов и ухудшает их функциональность. Это нарушение может возникнуть резко, например при закупорке тромбом сосуда, или развиться в хронической форме, когда поступление крови к органу сохраняется, но заметно снижается.
Острое нарушение кровообращения требует немедленного оперативного вмешательства, так как чревато летальным исходом. Хронические формы ухудшают качество жизни человека, вызывают другие заболевания внутренних органов, и также требуют проведения операции.
Преимущества лечения в ИСЦ
При патологии чревного ствола и верхней брыжеечной артерии наши рентгенхирурги могут выполнить ангиопластику и стентирование сужений этих значимых артерий. Чаще всего используется доступ через плечевую или лучевую артерию.
При наличии тромбоза мезентериальной артерии или чревного ствола в нашей клинике выполняются операции тромбэктомии с помощью специального зонда Rotarex или селективный тромболизис. После восстановления кровотока мы выполняем ангиопластику и стентирование.
Причины сужения чревного ствола и диагностика методом ультразвукового дуплексного сканирования
Научный интерес к определению информативности неинвазивных методов исследования обусловлен поиском доступных недорогих способов диагностики и прогнозирования органических и функциональных заболеваний внутренних органов. При поражении висцеральных ветвей брюшного отдела аорты появляются клинические признаки, свойственные заболеваниям гастродуоденальной области, желчного пузыря, поджелудочной железы и кишечника. У пациентов с заболеваниями этой области диагностируют органические и функциональные изменения органов, проводят лечение, несмотря на которое рецидивируют симптомы обострения болезни. Изучение кровотока в непарных висцеральных ветвях брюшного отдела аорты
(НВВА) — чревном стволе, верхней и нижней брыжеечной артерии — нередко позволяет установить причину нарушений деятельности органов и подобрать адекватные эффективные методы лечения. Ультразвуковые исследования, выполненные на современной аппаратуре с использованием доплеровских методик, — новая методология визуализации сосудов брюшной полости, позволяющая изучать анатомические особенности и кровоток на всем протяжении артериовенозного русла и расширить возможности диагностики заболеваний гастродуоденальной области.
При ультразвуковом дуплексном сканировании
визуализируют брюшную аорту, начальные отделы чревного ствола и его ветвей (общую печеночную и селезеночную артерии), а также верхнюю и нижнюю брыжеечные артерии. Исследование позволяет оценить размеры сосудов, расширение или сужение их просвета, изменение толщины стенок и соотношение интимы и медии, аневризматические выпячивания, наличие атеросклеротических бляшек, а также изучить скорость и характер кровотока.
К основным признакам, обусловленным нарушениями кровообращения
в непарных висцеральных ветвях брюшного отдела аорты, относят следующие:
- полное отсутствие кровотока в случае окклюзии сосуда,
- снижение скорости кровотока дистальнее места стеноза,
- усиление скорости кровотока непосредственно в месте стеноза и турбулентность в устье сосуда,
- выявление коллатерального кровотока с противоположным током крови при окклюзии магистрального сосуда,
- уменьшение диаметра пораженного сосуда,
- постстенотическое расширение.
Используя различные позиции датчика, из переднебрюшного доступа визуализируют брюшной отдел аорты и ее непарные висцеральные ветви в продольной и поперечной плоскости. Для получения продольного изображения брюшного отдела аорты датчик располагают левее средней линии тела вдоль вертикальной оси туловища, ориентируя плоскость сканирования перпендикулярно передней брюшной стенке c направлением на позвоночный столб при положении пациента на спине. Сканирование проводят ниже мечевидного отростка на 1-2 см, смещая датчик в каудальном направлении. Для получения поперечного среза брюшного отдела аорты датчик должен быть ориентирован перпендикулярно парамедиальной линии слева.
Брюшной отдел аорты
при ультразвуковом исследовании выглядит как трубчатая пульсирующая структура с ровными, гладкими стенками, однородным анэхогенным просветом. Диаметр аорты ниже диафрагмы составляет 25-28 мм, на уровне висцеральных артерий — 20-24 мм. При доплеровском исследовании кровоток в аорте соответствует магистральному типу с наличием острого систолического антеградного пика с высокой максимальной систолической скоростью и обратным кровотоком в период ранней диастолы.
Визуализация чревного ствола
осуществляется при получении поперечных срезов из эпигастральной области. Датчик перемещается от мечевидного отростка каудально (на 2-3 см) до появления характерного признака «крыльев чайки», который обусловлен делением чревного ствола на общую печеночную и селезеночную артерии. Чревный ствол лоцируется в виде сосуда длиной 2-4 см, отходящего под углом от передней поверхности аорты. При поперечном сканировании визуализируют чревный ствол на всем протяжении, а общую печеночную и селезеночную артерии — в области устьев и в проксимальном отделе. Чревный ствол и его висцеральные ветви относятся к артериям с высоким периферическим сопротивлением.
Для получения изображения верхней брыжеечной артерии
в продольном сечении датчик разворачивают на 90°. На 1-2 см ниже чревного ствола определяют отходящую от передней поверхности аорты верхнюю брыжеечную артерию. На поперечных срезах она лоцируется между селезеночной веной и аортой. Верхняя брыжеечная артерия визуализируется над аортой на протяжении 7 см от места своего отхождения. Для получения спектра кровотока контрольный объем располагают в просвете сосуда в 1-1,5 см от места отхождения от аорты. Регистрацию спектра кровотока в верхней брыжеечной артерии выполняют в устье. Верхняя брыжеечная артерия относится к артериям с высоким периферическим сопротивлением.
Нижняя брыжеечная артерия
берет свое начало непосредственно ниже почечных артерии от левой переднебоковой поверхности брюшной аорты. Визуализация нижней брыжеечной артерии затруднена из-за малого диаметра (3 мм и менее). В ряде случаев ее изображение может быть получено при сканировании брюшного отдела аорты в поперечной либо продольной плоскости, ниже устья левой почечной артерии. Спектр кровотока нижней брыжеечной артерии характеризуется высоким периферическим сопротивлением.
К критериям сужения или окклюзии артериальных сосудов
относятся качественные и количественные показатели спектральных характеристик доплеровского сигнала. Рассчитывают количественные показатели, отражающие гемодинамику артериального русла:
- максимальную, среднюю и минимальную скорости кровотока,
- индекс пульсативности (PI),
- индекс резистентности (RI),
- систолодиастолическое соотношение (S/D).
Оценивают качественные характеристики спектра частот доплеровских кривых. Важным признаком сужения артерии является регистрация турбулентного потока с расширением спектра в систолу и диастолу. В случае отсутствия заметного увеличения максимальной амплитуды скорости кровотока при турбулентности потока крови регистрируют широкое распределение частот и уменьшение площади лоцируемого «окна», характерного для нормального ламинарного движения крови в артериальном сосуде.
Наиболее достоверным и информативным признаком сужения магистральной артерии является увеличение максимальной систолической амплитуды доплерограммы (рис. 1).
Максимальную скорость потока крови или пиковую систолическую скорость кровотока
(ПСС) измеряют в висцеральных артериях на уровне устьев и визуализируемых сегментов чревного ствола и верхней брыжеечной артерии. Помимо пиковой систолической скорости кровотока оценивают низкоскоростные показатели кровотока, отражающие изменения (снижение) сердечного выброса либо указывающие на значительное сужение сосуда.
Непременным условием точного измерения
пиковой систолической скорости кровотока в чревном стволе является коррекция угла доплеровского сканирования кровотока, составляющего 60°.
Измерение параметров кровотока проводится в фазу глубокого вдоха и выдоха
. В норме на высоте выдоха отмечается увеличение пиковой систолической скорости кровотока в чревном стволе в среднем на 35,6 ± 5,9% по сравнению с фазой глубокого вдоха. Среднее значение пиковой систолической скорости кровотока кровотока в чревном стволе составляет 98-115 м/с, в верхней брыжеечной артерии — 98-142 м/с, в нижней брыжеечной артерии — 93-189 см/с. По данным Г. И. Кунцевич и соавт., максимальные значения скорости кровотока в чревном стволе соответствуют 128 ± 12 см/с, в верхней брыжеечной артерии — 136 ± 16 см/с. Вариабельность скоростных показателей кровотока является одной из причин расхождения результатов.
В диагностике стенозов
непарных висцеральных ветвей брюшного отдела аорты к наиболее распространенным относят критерии, предложенные G. L. Moneta и соавт. Авторы показали, что максимальная скорость кровотока в чревном стволе 200 см/с и более, в верхней брыжеечной артерии — 245 см/с и более, что свидетельствует о гемодинамически значимых стенозах (> 70%). Чувствительность, специфичность и предсказующая ценность теста для чревного ствола составили 75%, 89% и 85% соответственно.
Помимо изменений пиковой систолической скорости кровотока установлено значение конечной диастолической скорости кровотока
при гемодинамически значимом стенозе верхней брыжеечной артерии. Поскольку увеличивается диастолическая составляющая, приобретающая характер магистрально-измененного типа, при стенозе более 75% изменяется вид доплерограммы верхней брыжеечной артерии. Сравнительный анализ результатов доплерографии и артериографии показал информативность конечной диастолической скорости кровотока в диагностике стенозов чревного ствола и верхней брыжеечной артерии. В результате исследований установили, что для непарных висцеральных ветвей брюшного отдела аорты стеноз артерий более 50% является гемодинамически значимым.
Существуют различные этиологические факторы
, вызывающие анатомические изменения и нарушения гемодинамики в непарных висцеральных ветвях брюшного отдела аорты. Часто называют две основные группы причин, приводящих к изменению просвета сосуда: интравазальные и экстравазальные.
Интравазальные изменения
обусловлены врожденными или приобретенными заболеваниями артерий. К
врожденным
относят аномалии развития сосудов — гипо-, аплазия, фибромускулярная дисплазия, артериовенозные мальформации; к
приобретенным
— атеросклероз, неспецифический аортоартериит, облитерирующий тромбоангиит, постэмболическая окклюзия. Выделяют следующие формы поражения артерий: окклюзия, патологическая извитость, аневризма, также существуют комбинированные и сочетанные формы. Степень сужения сосуда рассматривают как стеноз до 50%, гемодинамически значимый стеноз — > 50%, 75-90%, > 90%.
Экстравазальную компрессию
непарных висцеральных ветвей брюшного отдела аорты в первую очередь связывают с особенностями строения и развития аортального отверстия диафрагмы, образуемого спереди и с боков сухожильными краями правой и левой ножек диафрагмы, соединенных срединной дугообразной связкой диафрагмы, а сзади — телами позвонков. Происходит сдавление сосудов срединной дугообразной связкой диафрагмы, ее внутренними ножками, при этом воздействие на чревный ствол отмечают чаще, чем на верхнюю и нижнюю брыжеечные артерии. Причинами частого сдавления чревного ствола являются топографические особенности артерии. Поскольку срединная дугообразная связка диафрагмы располагается на уровне устья чревного ствола или ниже на 2/3 позвонка, во время дыхательных движений она смещается и соприкасается с чревным стволом. В результате взаимодействия чревного ствола и дугообразной связки на выдохе происходит сдавление устья и самого ствола (рис. 2).
Иногда компрессия чревного ствола возникает при высоком отхождении сосуда от аорты либо низком прикреплении диафрагмы с нормальным уровнем отхождения артерии. К тому же нарушения кровотока возникают при перегибе чревной артерии, который может произойти в результате ее низкого отхождения от аорты.
Другой частой причиной компрессии непарных висцеральных ветвей брюшного отдела аорты является внесосудистое сдавление
нервными ганглиями солнечного сплетения, нейрофиброзной тканью чревного сплетения, опухолями.
По данным патологоанатомических исследований, изменения непарных висцеральных ветвей брюшного отдела аорты наблюдают в 19,2-70% случаев, по результатам ангиографии — 4,4-53,5%. В неоднородных по возрастному и половому составу контингентах исследуемых пациентов частота встречаемости компрессии непарных висцеральных ветвей брюшного отдела аорты и причин ее развития значительно варьируются.
И. А. Комиссаров и соавт. наблюдали 538 детей в возрасте 5-18 лет с болями в животе. По результатам комплексного исследования, включающего ультразвуковое дуплексное сканирование, компрессию чревного ствола выявили у 109 детей (20,2%), в том числе у 65 (59,7%) девочек и 44 (40,3%) мальчиков. Среди причин компрессии чревного ствола
у детей выявили экстравазальное воздействие дугообразной связки диафрагмы, внутренних ее ножек, а также сдавление нейрофиброзной тканью чревного сплетения.
Л. А. Звенигородская и соавт. по результатам исследования 236 пациентов (средний возраст 53,5 ± 2,7 лет) с хронической ишемической болезнью органов кровообращения показали, что в большинстве случаев (76,8%) встречается внутрисосудистое поражение непарных висцеральных ветвей брюшного отдела аорты, обусловленное атеросклеротическим процессом в артериях. В остальных случаях экстравазальную компрессию чревного ствола связали с воздействием серповидной связки диафрагмы.
А. В. Покровский указывал, что по результатам ультразвукового доплерографического, рентгенографического и патологоанатомического исследований у пациентов с атеросклерозом коронарных артерий в 73,5% случаев выявляют атеросклеротическое поражение непарных висцеральных ветвей брюшного отдела аорты.
По мнению А. И. Канаева и соавт., исследовавших 325 пациентов в возрасте 17-72 лет (средний возраст 35,5 ± 0,8 лет) с компрессией чревного ствола, нарушения кровотока в чревном стволе обусловлены гемодинамическими факторами, возникающими в результате изолированного стеноза чревного ствола либо в сочетании с нарушением кровотока в верхней брыжеечной артерии. Другие патогенетические факторы гемодинамических нарушений в непарных висцеральных ветвях брюшного отдела аорты включали механическое раздражение срединной дугообразной связкой диафрагмы и пульсовой волной чревного сплетения. У большинства пациентов с гемодинамическими нарушениями в чревном стволе выявлены заболевания желудка, двенадцатиперстной кишки, поджелудочной железы.
По мнению многих исследователей, помимо сдавления непарных висцеральных ветвей брюшного отдела аорты в развитии гемодинамических нарушений значительную роль отводят состоянию коллатерального кровотока
. Коллатеральный кровоток между чревным стволом и верхней брыжеечной артерией обеспечивает панкреатодуоденальная аркада. В случае стеноза чревного ствола, являющегося основным артериальным сосудом, кровоснабжающим регион, недостаточность кровообращения компенсируется посредством перераспределения крови в зонах: из зоны верхнебрыжеечной артерии в зону чревного ствола. Несостоятельность коллатерального кровотока при перераспределении крови приводит к ишемии в обеих зонах (steal syndrome).
В одном исследовании высказывается предположение об общности причинной связи гемодинамических нарушений в чревном стволе с избыточным развитием створок митрального клапана и клиническими признаками пролапса митрального клапана. L. Arcari, исследовав ультразвуковым методом 1560 пациентов, выявил в 3,7% случаев (57 человек — 23 мужчины и 34 женщины) нарушения кровотока в чревном стволе. Пролапс митрального клапана диагностирован у 47 (82,4%) пациентов с нарушениями кровотока в чревном стволе и 118 (7,9%; р < 0,001) без таковых признаков. У большинства пациентов с компрессией чревного ствола (средний возраст 35 ± 12 лет) не было выявлено явных причин для экстра- либо интравазального сдавления артерии. Автор многомерным статистическим анализом показал, что гемодинамические нарушения в чревном стволе являются независимым от пола и возраста фактором, связанным с пролапсом митрального клапана.
Пролапс митрального клапана
и другие варианты малых аномалий сердца нередко определяют у лиц с признаками наследственной дисплазии соединительной ткани, характеризующейся системными изменениями. Среди системных нарушений отмечают особенности развития, функциональные и органические заболевания желудка, двенадцатиперстной кишки, кишечника. Поскольку при наследственной дисплазии соединительной ткани помимо сердечной архитектоники изменяются строение и функциональное состояние сосудистого русла, нарушения кровотока в чревном стволе, возможно, обусловлены особенностями строения и метаболизма соединительной ткани.
T. Scholbach исследовал чревный ствол ультразвуковым методом у 3449 пациентов от 0 до 18 лет с жалобами на абдоминалгию. В 1,7% (59 пациентов в возрасте 22 месяцев — 19 лет, в том числе 81% женского пола) выявлены признаки синдрома компрессии чревного ствола. Результаты сонографии подтвердили у 21 пациента методом магнитно-резонансной томографии. Помимо боли в животе компрессия чревного ствола сопровождалась симптомами боли в грудной клетке (22%), тошнотой (29%), изжогой (17%), рвотой (15%), потерей массы тела (15%), постпрандиальным усилением признаков (15%), диареей (14%), дыхательным дискомфортом (14%), синкопе (12%), систолическим шумом над артерией (15%).
Таким образом, истинная распространенность нарушений кровотока
в непарных висцеральных ветвях брюшного отдела аорты не определена, литературные данные свидетельствуют о вариабельности результатов, обусловленных неоднородностью по возрасту, полу, клиническим проявлениям исследованных пациентов. Ультразвуковая диагностика, включающая режим дуплексного цветового картирования, является доступным методом, сопоставимым с ангиографическими исследованиями, рекомендуемым для скрининга пациентов с нарушениями кровообращения в висцеральных сосудах. При комплексном исследовании пациентов с нарушениями кровообращения в непарных висцеральных ветвях брюшного отдела аорты возникают трудности в выявлении единственной причины экстравазальной компрессии чревного ствола, преобладающей нередко при нарушениях кровообращения в непарных висцеральных ветвях брюшного отдела аорты, поскольку гемодинамические нарушения возникают под влиянием многих факторов.
Трисветова Е. Л., Вараницкая Н. М.
Белорусский государственный медицинский университет, 432-й Главный военный клинический медицинский центр Вооруженных Сил Республики Беларусь. Журнал «Медицинская панорама» № 9, октябрь 2009.
Показания и противопоказания к методу лечения
Показания:
Стеноз чревного ствола более 60% с синдромом хронической абдоминальной ишемии
Стеноз верхней брыжеечной артерии более 60% (симптомы сосудистой недостаточности кишечника не являются обязательным показанием, достаточно факта стеноза)
Этап эндоваскулярного лечения острой мезентериальной непроходимости (мезентериальный тромбоз)
Противопоказания:
- Аллергия на йод
- Аневризма торакоабдоминальной аорты (без операции по поводу аневризмы)
- Стадия некроза кишки при мезентериальном тромбозе
Возможные осложнения и прогноз
Основным негативным последствием стеноза чревного ствола называют нарушение функций пищеварительной системы. При отсутствии адекватного лечения на фоне недостаточного кровоснабжения органы ЖКТ (печень, поджелудочная железа, селезенка, желчный пузырь, желудок) не получают достаточного количества питательных веществ. Осложнениями данного патологического состояния называют:
- панкреатит;
- желчекаменную болезнь;
- холецистит;
- парез желудка, кишечника;
- атонию мочевого пузыря.
Прогноз болезни Данбара зависит от того, насколько рано выявлена патология. При своевременно выполненной операции восстановление функций органов пищеварения происходит довольно быстро. Больной на протяжении нескольких месяцев после вмешательства возвращается к нормальной жизни и не испытывает никаких дискомфортных ощущений.
Чтобы предупредить развитие стеноза чревного ствола необходимо внимательно относиться к своему здоровью и при выявлении каких-либо нарушений – сразу обращаться к врачу. Поводом для беспокойства должен стать стойкий болевой синдром в брюшной полости, который не купируется традиционными методами терапии. Врожденные аномалии развития предупредить невозможно.
Подготовка к лечению
Стандартное обследование перед операцией:
- Клинические анализы крови и мочи, биохимический анализ крови.
- Коагулограмма, агрегация тромбоцитов
- Гастроскопия (исследование желудка)
- Рентгенография легких
- ЭКГ
- ЭХО кардиография
- УЗИ органов брюшной полости, аорты и артерий конечностей
- Мультиспиральная компьютерная томография с контрастом аорты и ее ветвей
Перед операцией необходимо воздерживаться от приема пищи за 8 часов и жидкости за 2 часа. Других мероприятий по подготовке не требуется.
Результаты
Все больные после операции были выписаны в удовлетворительном состоянии. Интра- и послеоперационных осложнений не было. Случаев конверсии также не было. Основные показатели представлены в табл. 2.
Таблица 2. Послеоперационные данные больных с КСЧС
Средняя длительность операции лапароскопической декомпрессии составила 65 мин. Во всех наблюдениях послеоперационный период протекал без осложнений и в среднем составил 4 койко-дня. Всем пациентам в послеоперационном периоде назначали обезболивание, симптоматическую терапию и выполняли контрольное УЗИ брюшной полости.
Двум пациентам проведено контрольное обследование в позднем послеоперационном периоде: УЗИ в режиме импульсно-волновой допплерографии, МСКТ с внутривенным усилением (рис. 5) и ангиография (рис. 6). Клинически в обоих наблюдениях отмечалось уменьшение интенсивности, частоты и продолжительности болевого синдрома.
Рис. 5. Мультиспиральная компьютерная томограмма с внутривенным усилением и 3D-реконструкция после операции.
Рис. 6. Ангиограмма (целиакограмма) в боковой проекции до (а) и после (б) операции.
Как проходит метод лечения
Операция проводится под местной анестезией в области доступа. Возможно доступ будет на бедре или в области локтевого сгиба. Операционное поле обрабатывается антисептиком и закрывается стерильными простынями.
Хирург выполняет местную анестезию места прокола, после чего проводится пункция артерии специальной иглой и установка короткой трубочки — интрадюссера.
Через интрадюссер проводится вся дальнейшая работа с сосудами. Специальный проводник заводится в брюшную аорту, затем по нему проводится катетер, через который выполняется контрастное исследование чревного ствола и брыжеечной артерии. Этот этап называется селективной ангиографией. Она является окончательным методом диагностики. Если сужения артерий подтверждаются, то проводник заводится ниже места сужения. По проводнику проводится баллон со стентом. Раскрытием этого баллона устраняется сужение артерии, а стент укрепляет артериальную стенку.
После имплантации стента обязательно проводится контрольная ангиография, чтобы исключить возможные осложнения. Катетер и интродюссер извлекаются из места доступа, а кровотечение останавливается прижатием или с использованием специального сшивающего устройства «Ангиосил».
Возможные осложнения при лечении
Осложнения самой операции:
- Разрыв суженной артерии с кровотечением — требует экстренной открытой операции или установки специального покрытого стента (стент-графта). К счастью, встречается очень редко.
- Тромбоз реконструированной артерии — редкое осложнение, встречается при повышенной свертываемости крови. Если проводится предоперационная подготовка с использованием антитромбоцитарной подготовки, то риск минимальный. Если тромбоз наблюдается во время вмешательства, то выполняется тромбэктомия или тромболизис (введение препаратов рассасывающих тромб). Если признаки нарушения кишечного кровообращения наблюдаются после операции, то пациент повторно берется в операционную и проводится удаление тромбов с помощью ротарекса или специальных аспирационных катетеров.
Осложнения сосудистого доступа:
- Гематома в области пункции
- Тромбоз артерии в области пункции
- Повреждение нервов в области пункции
Эти осложнения встречаются крайне редко и легко устраняются при своевременном выявлении.
Программа наблюдения после метода лечения
Наблюдение за результатами ангиопластики и стентирования висцеральных артерий осуществляется с помощью УЗИ контроля через 3 месяца, а затем ежегодно.
Через год после вмешательства желательно выполнить мультиспиральную компьютерную томографию с контрастированием брюшной аорты и ее ветвей.
После лечения пациенту назначаются антитромботические препараты. Чаще всего это аспирин и клопидогрель (плавикс). Прием этих препаратов нужно осуществлять постоянно, обязательно ставя в известность врачей перед выполнением каких-либо других вмешательств.
Классификация форм заболевания:
Стеноз чревного ствола (снабжает кровью печень, селезенку, желудок, поджелудочную железу)
Это состояние, при котором просвет чревного ствола сужается, может быть приобретенным — развивается при поражении сосуда атеросклерозом, либо врожденным — при сдавлении извне дугообразной связкой диафрагмы (значительно реже — при воспалительных заболеваниях, аневризмах аорты, врожденных аномалиях развития, сдавлении новообразованиями брюшной полости). Первая причина часто сочетается с поражением других артерий (коронарных — внутрисердечные артерии, сонных, артерий нижних конечностей), вторая причина — врожденное состояние, проявления которого развиваются в молодом возрасте. Основными органами, испытывающими недостаток кровоснабжения, являются желудок, печень и поджелудочная железа, однако за счет «синдрома обкрадывания» страдает и кишечник. Значимым сужением просвета артерии в настоящее время считается более 50% от первоначального диаметра. Симптомы заболевания — боли в животе, вздутие, нарушения стула в виде чередующихся поносов и запоров, тошнота, потеря веса объединяются в единый синдром — синдром «хронической абдоминальной ишемии» (хроническая ишемическая болезнь органов пищеварения, абдоминальная ишемическая болезнь).
Установить причину сужения сосуда можно при помощи:
- дуплексного сканирования сосудов брюшной полости,
- выполнения ангиографии либо мультиспиральной компьютерной томографии — ангиографии (МСКТ-ангиография).
При установке показаний и выборе метода оперативного лечения учитывается возраст пациента, выраженность жалоб, эффективность консервативного лечения (без операции), степень компенсации функции задействованных органов. Показания к оперативному лечению, согласно современным стандартам, должны устанавливать совместно гастроэнтеролог и сосудистый хирург.
Существуют следующие виды операций:
- Эндоваскулярная балонная ангиопластика со стентированием чревного ствола.
Это вмешательство выполняется через прокол в бедренной, реже — в других артериях. При помощи специальных тонких инструментов суженный участок чревного ствола расширяется изнутри до восстановления нормального диаметра просвета и устанавливается стент — тонкий «каркас» из инертных сплавов, в дальнейшем препятствующий повторному сужению артерии. Применяется чаще всего при поражении чревного ствола атеросклерозом. - Лапароскопическая декомпрессия чревного ствола.
Операция выполняется малоинвазивно из отдельных проколов. Данный метод позволяет надсечь связку диафрагмы, «освободив» чревный ствол от ее давления. При этом артерия расправляется, со временем восстанавливая свой нормальный диаметр. Ранее подобные операции выполнялись на открытой брюшной полости, что иногда сопровождалось тяжелым послеоперационным периодом, характерным для открытых операций, поэтому их распространенность была ограниченной. Развитие лапароскопической хирургии позволило выполнять данные вмешательства с достижением хорошего послеоперационного и косметического результата. - Шунтирующие операции при сужении / закупорке чревного ствола или его протезирование.
Выполняются при далеко зашедших стадиях атеросклероза, когда установить стент либо извлечь атеросклеротическую бляшку из сосуда не представляется возможным. Суть операций заключается в формировании обходного кровотока помимо пораженного чревного ствола, либо его замена искусственным протезом. Данные вмешательства относятся к технически сложным, выполняются только на открытой брюшной полости и требуют высокой квалификации сосудистого хирурга.
Стеноз верхней брыжеечной артерии
Встречается значительно реже, чем стеноз чревного ствола. Наиболее частые причины заболевания— атеросклеротическое сужение просвета верхней брыжеечной артерии (на фоне системного атеросклероза) и врожденное нарушение структуры стенки артерии — фибромускулярной дисплазии. Верхняя брыжеечная артерия разветвляется на множество менее тонких сосудов, которые кровоснабжают тонкую кишку и часть толстой кишки. Заболевание зачастую протекает без каких-либо симптомов, и трудно поддается диагностике, пока не наступают серьезные осложнения — полная закупорка верхней брыжеечной артерии или ее ветвей. При данном состоянии пациенты попадают в хирургический стационар с признаками скоротечного омертвения лишенного кровоснабжения участка кишечника, отличить которое от других острых хирургических заболеваний живота иногда очень сложно. В данном случае требуется неотложная операция — резекция нежизнеспособного участка кишки.
Установить диагноз на ранних стадиях можно при помощи:
- ультразвуковой допплерографии брюшной аорты и ее ветвей (эффективность диагностики около 50%),
- магнитно-резонансной томографии (эффективность диагностики около 80%),
- ангиографии брюшной аорты и ее ветвей (позволяет установить наличие сужения сосуда в 90% случаев).
Лечение при раннем выявлении стеноза верхней брыжеечной артерии сходно с терапией системного атеросклероза, однако при значимых сужениях артерии возможно выполнение оперативного вмешательства — эндоваскулярной ангиопластики.
Стеноз почечной артерии
Сужение почечных артерий развивается вследствие атеросклеротического поражения, а также при более редком заболевании — фибромускулярной дисплазии. Нарушение поступления крови к одной или обеим почкам сопровождается общей негативной реакцией организма. Почка, испытывающая дефицит крови, получает ложную «информацию” об общем объеме крови, и начинает реагировать так, как если бы общее количество крови в организме снизилось. Усиливаются процессы синтеза гормонов, направленные на удержание воды в организме для поддержания постоянного объема жидкости в общем кровеносном русле. Данный механизм является патологическим, так как количество крови остается прежним, и, за счет продукции почечных гормонов, в кровеносное русло поступает дополнительный объем воды из клеток. Вследствие этого развивается стойкая почечная артериальная гипертензия — повышение артериального давления выше нормальных цифр, плохо поддающееся снижению лекарственными препаратами. Появляются отеки, нарушение работы сердца. Этот вид артериальной гипертензии обычно вовремя распознается лечащими врачами, и при ультразвуковом исследовании часто удается выявить поражение почечных артерий. Открытая операция для восстановления кровотока по почечной артерии — обходное шунтирование, протезирование (замена) пораженного участка в настоящее время выполняется все реже, на смену им приходят малоинвазивные эндоваскулярные методы — ангиопластика и стентирование.