Сердце человека – удивительный орган, благодаря которому возможно нормальное функционирование всех органов и систем. Сокращение сердечной мышцы обеспечивается, благодаря электрическим импульсам, которые проходят через специальные пути. При наличии дополнительных путей проведения этих импульсов происходят определенные изменения, которые можно отследить с помощью электрокардиограммы (ЭКГ). При изменениях желудочкового комплекса речь идет о феномене WPW (преждевременное возбуждение желудочков). При небольших нарушениях, характеризующихся лишь сменой скорости проведения импульсов между желудочками и предсердием, диагностируется синдром CLC.
Что представляет собой заболевание
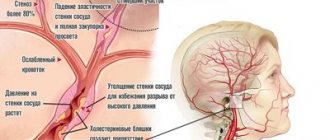
Синдром Клерка–Леви–Кристеско или CLC – патология строения сердца врожденного характера, одна из разновидностей синдрома преждевременного возбуждения желудочков. Обусловлена аномалия наличием пучка Джеймса. Благодаря этому пучку соединяется атриовентрикулярный узел с одним из предсердий. Эта особенность сопровождается передачей преждевременного импульса к желудочкам.
Диагностировать патологию удается с помощью ЭКГ. Часто синдром CLC встречается случайно у абсолютно здоровых людей, при этом какие-либо признаки у пациента отсутствуют. Известны случаи выявления данного заболевания у детей.
Даже при отсутствии симптомов не стоит полагать, что патология безвредна. Синдром преждевременного возбуждения желудочков способен вызывать аритмию. Состояние сопровождается учащением пульса (иногда свыше 200 ударов в минуту). Особенно это ощущается у людей пожилого возраста, молодые пациенты переносят аритмию легче.
Почему возникает синдром укороченного PQ?
Как уже было указано, анатомический субстрат данного синдрома у взрослых является врожденной особенностью, так как дополнительные пучки проведения формируются еще во внутриутробном периоде. Люди с такими пучками отличаются от обычных людей лишь тем, что у них дополнительная мельчайшая “ниточка” в сердце, которая принимает активное участие в проведении импульса. А вот как себя поведет сердце с данным пучком, будет обнаружено по мере роста и взросления человека. Например, у детей синдром CLC может начать проявляться как во младенчестве, так и в подростковом периоде, то есть во время быстрого роста организма. А может не проявляться совсем, так и оставаясь лишь электрокардиографическим феноменом на протяжении всей взрослой жизни до старости.
Причину, по которой синдром все-таки начинает проявляться пароксизмальной тахикардией, не может назвать никто. Однако известно, что у пациентов с органической патологией миокарда (миокардит, инфаркт, гипертрофическая кардиомиопатия, порок сердца и др) приступы тахикардии возникают намного чаще и клинически протекают с более выраженной клиникой и с тяжелым общим состоянием больного.
А вот провоцирующие факторы, способные вызвать пароксизм, можно перечислить:
- Физическая нагрузка, значительно или не очень превосходящая обычную физическую активность пациента,
- Психоэмоциональная нагрузка, стрессовая ситуация,
- Гипертонический криз,
- Употребление большого количества пищи за один прием, питье очень горячей или очень холодной жидкости,
- Посещение бани, сауны,
- Перепад внешних температур, например, выход на сильный мороз из очень жаркого помещения,
- Повышенное внутрибрюшное давление, например, в момент сильного кашля, чихания, акта дефекации, потуг во время родов, поднятия тяжестей и т. д.
Особенности патологии
Предвозбуждение сердечных желудочков может протекать бессимптомно, в этом случае речь идет о «феномене предвозбуждения». При появлении признаков патологии у пациента заболевание классифицируется как «синдром предвозбуждения».
Различают несколько видов заболевания:
- Брешенмаше (атриофасцикулярный) – здесь правое предсердие соединено со стволом пучка Гиса;
- Махейма (нодовентрикулярный) – при этом правая сторона межжелудочковой перегородки связана с атриовентрикулярным узлом;
- Кента (предсердно-желудочковый) – здесь предсердия и желудочки соединены в обход атриовентрикулярного узла;
- Джеймса (атрионодальный) – импульсы проходят между нижней частью атриовентрикулярного и синоатриальным узлом.
Важно! Иногда встречается наличие нескольких путей аномального проведения импульсов. Количество таких больных составляет не более 10% от всех случаев заболевания.
Синдром CLC четко отслеживается с помощью проведения электрокардиограммы
Лечение синдрома Лауна-Ганонга-Левайна
Основа лечения – медикаментозная терапия. Для борьбы с тахикардией врачи используют:
- бета-адреноблокаторы;
- блокаторы кальциевых каналов;
- сердечные гликозиды.
Пациент принимает лекарства постоянно. Приступ тахикардии купируется немедикаментозными методами: прием Вальсальвы или массаж каротидного синуса. Если эти процедуры не помогают, внутривенно вводят противоаритмические препараты. Лечение проводят под контролем артериального давления и электрокардиографии.
Изредка требуется хирургическое лечение. Основной метод: абляция атриовентрикулярного узла или пучка Гиса с имплантацией кардиостимулятора.
Показания к операции:
- медикаментозная терапия не устраняет приступы тахикардии;
- пароксизмы остаются частыми на фоне оптимального медикаментозного лечения;
- пациент не хочет постоянно принимать препараты;
- лекарства противопоказаны или пациент страдает от побочных эффектов.
Вмешательство выполняется эндоваскулярным методом: через сосуды на ноге. Это малоинвазивная процедура, после которой не нужно долго восстанавливаться. Пациент проводит в больнице лишь несколько дней.
Суть вмешательства: с помощью радиочастотного метода врач нагревает и разрушает ткани в области атриовентрикулярного узла. То есть, он «перерезает кабель», по которому импульсы проходят из предсердий в желудочки. Так решается проблема слишком быстрого проведения импульсов. Но возникает серьезный побочный эффект: теперь импульсы не проходят вообще. В итоге предсердия и желудочки сокращаются в разном ритме. Причем частота желудочковых сокращений снижена: она недостаточна для поддержания эффективной гемодинамики.
Эта проблема решается дополнительным этапом лечения: установкой кардиостимулятора. Это устройство, которое генерирует импульсы и доставляет их в миокард через имплантированные электроды. В стандартном варианте используются двухкамерная стимуляция. Один электрод устанавливают в правое предсердие, ещё один – в правый желудочек. Теперь между этими камерами сердца нет прямой связи, но искусственный водитель ритма подает импульсы таким образом, чтобы синхронизировать предсердные и желудочковые сокращения.
Процедура по установке кардиостимулятора минимально травматичная. Само устройство имплантируют под кожу грудной клетки через разрез 4-5 см. Электроды доставляют к сердцу через кровеносные сосуды. Аппарат может работать 7-10 лет, после чего батарея разряжается, и кардиостимулятор нужно заменить. Врач проверяет работоспособность электродов: если они функционируют, то их замена не требуется.
Что провоцирует CLC
Для того чтобы понять, как возникает синдром CLC, следует вспомнить анатомию. Для нормального наполнения желудочков сердца кровью и их сокращения после сокращения предсердий в строении органа присутствует специальный фильтр, расположенный между ними. Этот фильтр называется атриовентрикулярным узлом. При передаче импульса в этот узел возбуждение проходит медленно, после чего передается на желудочки. Благодаря такому процессу, кровь попадает в аорту и легочный ствол.
При некоторых врожденных патологиях у человека могут присутствовать обходные пути проведения сердечных импульсов. Часто таким путем выступает пучок Джеймса и некоторые другие каналы. При этом ЭКГ показывает незначительные отклонения от нормы или сильные нарушения, например, при серьезной деформации желудочков. Синдром преждевременного возбуждения желудочков в медицинской практике имеет название WPW.
Возможно ли развитие осложнений при укорочении PQ?
Феномен укороченного PQ ни к каким осложнениям привести не может. Из-за того, что проявлением синдрома PQ является приступ тахиаритмии, то и осложнения будут соответствующие. К ним относятся возникновение внезапной сердечной смерти, фатальных аритмий (фибрилляция желудочков), тромбоэмболия артерий головного мозга и легочной артерии, развитие инфаркта миокарда, аритмогенного шока и острой сердечной недостаточности. Разумеется, такие осложнения развиваются далеко не у каждого пациента, но помнить о них нужно любому. Профилактикой осложнений является своевременное обращение за медицинской помощью, а также своевременное проведение операции, если показания для таковой обнаружены врачом.
Как протекает заболевание
Патология может проявить себя в любом возрасте пациента. Длительное время болезнь способна протекать без явных признаков и симптомов. Феномен CLC сопровождается сокращением интервала P-Q во время проведения ЭКГ. При этом самочувствие пациента не нарушено, человек ведет полноценный образ жизни.
Признаками патологии часто становятся приступы тахикардии и некоторые другие проявления
При синдроме CLC у многих больных отмечаются внезапные приступы сильного сердцебиения – пароксизмальная тахикардия. Симптомы при этом наблюдаются следующие:
- появление приступа учащенного сердцебиения. Частота сердечных сокращений составляет до 220 ударов в минуту. Начало приступа сопровождается сильным толчком в области грудины или шеи;
- головокружение;
- шум в ушах;
- повышение потливости;
- вздутие живота;
- иногда возникает тошнота, сопровождающаяся рвотой;
- обильное выделение урины в начале или в конце приступа, иногда мочеиспускание непроизвольное.
Реже патология сопровождается мерцательной аритмией предсердий, учащенным сердцебиением неритмичного характера.
Синдром Вольфа-Паркинсона-Уайта: симптомы
Чаще всего симптоматика этого заболевания отсутствует, признаки выявляют уже при проведении электрокардиограммы. У более половины людей с наличием данной патологии после стрессов или физических нагрузок кардиологи Юсуповской больницы определяют жалобы на внезапные приступы сердцебиения, чередующиеся ощущением «замирания» в грудной клетке. Могут отмечаться боли в грудной клетке, чувство нехватки воздуха, головокружения, реже – потеря сознания. При нетяжелом проявлении симптомов возможно купирование их путем глубокого вдоха или задержкой дыхания. В редких случаях могут появиться осложнения: фибрилляция желудочков и остановка сердца.
Первая помощь во время приступа
Пациентам с синдромом CLC, часто испытывающим приступ повышенного сердцебиения, рекомендуется придерживаться следующих рекомендаций во время приступа:
- Выполнить массаж каротидного синуса. Воздействие на этот участок между разделением сонной артерии на внешнюю и наружную помогает нормализовать частоту сердечных сокращений.
- Мягко надавить на глазные яблоки.
- Для облегчения состояния можно опустить лицо в емкость с прохладной водой, задержав дыхание на 5 – 10 минут.
- Глубоко вдохнуть, натужиться, задержать дыхание на несколько секунд, медленно выдохнуть.
- Присесть несколько раз, напрягая все тело.
Важно! При часто повторяющихся приступах не стоит откладывать с визитом к врачу. Ранняя диагностика патологии поможет предотвратить осложнения, взять заболевание под медицинский контроль.
Диагностика
Главный метод диагностики синдрома CLC – электрокардиограмма. С помощью ЭКГ удается выявить следующие нарушения:
- сокращение интервалов P-Q;
- D-волна при наличии восходящей части R-зубца с одновременным снижением Q-зубца;
- появление комплекта QRS расширенного характера;
- отклонение СТ-сегмента и Т-зубца в обратную сторону от D-волны.
Большое внимание уделяется пространственной вектор-электрокардиограмме. С помощью метода удается с точностью определить месторасположение дополнительных проводимых каналов сердца.
Своевременная диагностика синдрома CLC позволяет взять патологию под медицинский контроль, предотвратить ее осложнения
Для более подробного исследования используют магнитокардиографию. Метод позволяет дать полную оценку деятельности сердечной мышцы. Происходит это благодаря оборудованию, регистрирующему магнитные составляющие в электродвижущей силе сердца.
Точную оценку деятельности сердечной мышцы позволяют дать такие методы инструментального исследования, как электрофизиологическое исследование сердца (ЭФИ), эндокардиальное и эпикардиальное картирование.
Особенности лечения патологии
Пациентам, у которых диагностируется бессимптомное течение патологии, особого лечения не требуется. Внимание уделяется больным, в роду у которых имелись случаи внезапной смерти. В группе риска также находятся люди, занимающиеся тяжелой физической работой, спортсмены, водолазы, летчики.
Если у больного отмечаются пароксизмы наджелудочковой тахикардии, терапия заключается в назначении медикаментозных препаратов, обеспечивающих купирование приступа. При этом обязательно учитывается характер нарушения сердечного ритма, наличие сопутствующих заболеваний сердечно-сосудистой системы.
Для избавления от ортодромной реципрокной наджелудочковой тахикардии применяются блокады, направленные на угнетение проводимости импульсов в атриовентрикулярном узле.
Медикаментозная терапия включает следующие препараты:
- Аденозин;
- Верапамил.
Часто для снижения проявления патологии назначаются b-адреноблокаторы, обладающие способностью расширения бронхов, артериаол и вен. Средства этой группы активируют выработку гликогенолиза печенью и скелетными мышцами, стимулируют секрецию инсулина.
Амиодарон – медикаментозный препарат, часто назначающийся при синдроме CLC
При отсутствии желаемого лечебного результата врачи используют Новокаинамид, помогающий блокировать импульсы, проходящие через дополнительный атриовентрикулярный канал. Лекарство отличается относительной безопасностью и хорошим эффектом при лечении многих сердечных патологий.
Кроме вышеописанных, используются следующие медикаментозные средства:
- Амиодарон;
- Соталол;
- Пропафенон;
- Флекаинид.
Важно! Использовать медикаментозные средства разрешается строго по назначению лечащего врача. Многие из них имеют серьезные противопоказания.
Среди немедикаментозных методов лечения следует выделить трансторакальную деполяризацию и предсердную электрокардиостимуляцию. Хирургическое лечение дополнительных проводящих путей используется в особых случаях, когда консервативная терапия не дает положительного эффекта. Операция проводится открытым методом в экстренных случаях при наличии серьезной угрозы для здоровья и жизни пациента. Метод заключается в разрушении дополнительных проводимых путей сердца.
Положительный прогноз для больных с нарушением проведения сердечных импульсов возможен при четком соблюдении рекомендаций врача
Кардиалгический синдром Х: вопросы дифференциальной диагностики и терапии
Проблема болевого синдрома в левой половине грудной клетки, или кардиалгического синдрома, постоянно приковывает к себе внимание врачей: совершенствуются подходы к оценке этих болей, пополняются дифференциальные ряды (см. таблицу). Но окончательно разрешить эту проблему так и не удалось. Особо актуальной эта тема может считаться из-за высокого риска связи кардиалгий с острыми заболеваниями и состояниями, которые могут привести к летальному исходу. Врачи общей практики зачастую вынуждены первыми решать вопросы диагностики, дифференциальной диагностики и тактики в отношении лиц с болью в прекардиальной области.
В последние годы в медицинской литературе все больше внимания уделяется относительно новому патологическому состоянию, которое, несомненно, относится к разряду кардиалгий, — синдрому Х. Для обозначения данного состояния используются русскоязычные и иноязычные синонимы: кардиалгический (кардиальный) синдром Х (syndrome X), стенокардия с поражением сосудов малого диаметра, болезнь малых сосудов (small vessel disease), синдром Джорлина-Лайкоффа (Gorlin-Licoff syndrome), микроваскулярная болезнь и др. Мы полагаем, что наиболее распространенным и соответствующим современному взгляду на данную проблему можно считать определение «кардиалгический синдром Х» [1]. Этим термином мы и будем пользоваться в дальнейшем, так как он указывает на основной клинический синдром болезни — боль в левой половине грудной клетки, а также отражает сложность понимания этиопатогенетических механизмов этой патологии.
Кардиалгический синдром Х (КСХ) — это патологическое состояние, характеризующееся наличием признаков ишемии миокарда (типичных приступов стенокардии и депрессии сегмента ST≥1,5 мм (0,15 мВ) продолжительностью более 1 мин, установленной при 48-часовом мониторировании ЭКГ) на фоне отсутствия атеросклероза коронарных артерий и спазма эпикардиальных венечных артерий при коронарографии.
Выделение КСХ произошло благодаря развитию и совершенствованию современных методов диагностики. Первое описание больного с длительно протекавшей стенокардией, у которого на аутопсии были обнаружены абсолютно нормальные коронарные артерии, принадлежит У. Ослеру и относится к 1910 году, позднее об этом феномене не упоминали. Только в 1967 году были представлены уникальные сообщения о двух больных с неизмененными при коронарографии венечными артериями и загрудинными болями, к 1973 году Кемпом были собраны данные о 200 таких пациентах [2]. Из этой группы была отобрана часть больных, у которых удалось доказать наличие признаков ишемии (продукция лактата во время болей, ишемические изменения сегмента ST при нагрузочных пробах). В связи с имеющимися объективными признаками сомнений в наличии этого патологического состояния в настоящее время нет, но и единое, взвешенное мнение о причинах его возникновения и патогенетических признаках, объединяющих пациентов, страдающих данным заболеванием, также отсутствует.
Этюды патогенеза. По современным представлениям, в основе развития КСХ лежит дефектная эндотелин-зависимая вазодилатация мелких миокардиальных артерий. Иначе говоря, во время физической нагрузки потребности миокарда в кислороде резко повышаются, что в норме приводит к расширению сосудистого русла сердечной мышцы, тогда как при КСХ этого не происходит. По каким-то неясным причинам мелкие артериальные сосуды утрачивают способность к дилатации, что на фоне все возрастающего уровня физической нагрузки провоцирует возникновение болей стенокардитического характера.
Возникновение дефектной вазодилатации может быть обусловлено перечисленными ниже причинами [1]:
- Снижение выработки мозгового натрийуретического пептида (brain-BNP) — биологически активного вещества, которое продуцируется миокардом и оказывает местное вазодилатирующее действие (несколько противоречит этому предположению тот факт, что ряд исследователей обнаруживают дефектную вазодилатацию не только в сосудах миокарда, но и в сосудах предплечья, то есть процесс носит распространенный характер).
- Снижение продукции адреномедуллина — вазоактивного пептида, вырабатываемого клетками мозгового слоя надпочечников и эндотелиоцитами, который снижает активность пролиферации гладких миоцитов и препятствует развитию гипертрофии сосудистой стенки. По данным же гистологических исследований, в сердечной мышце при КСХ обнаруживаются явления пролиферации гладкомышечных клеток медиального слоя мелких артерий.
- Чрезмерное образование эндотелина — непростаноидной субстанции, которая продуцируется эндотелиоцитами (под действием стрессов, гипоксии, ангиотензина-II, серотонина, повреждения интимы сосуда) и способствует пролиферации гладких миоцитов сосудов, что тоже может вызывать вышеописанные морфологические изменения. Кроме того, эндотелиин повышает концентрацию внутриклеточного кальция, а эффективность антагонистов кальция при КСХ можно считать доказанной.
- Тканевая инсулинорезистентность, приводящая к нарушению утилизации глюкозы миокардом и расстройствам деятельности эндотелия эпикардиальных сосудов [3, 4].
Еще одним очень важным патогенетическим моментом является снижение у большинства больных с КСХ порога восприятия боли; такие пациенты более чувствительны к ноцицептивным стимулам. Отмечается, что даже малая ишемия может приводить к яркой клинике стенокардии. Причиной возникновения болей считают нарушенный автономный контроль со стороны вегетативной нервной системы.
Ключевую роль в патогенезе заболевания может играть также и нарушение метаболизма аденозина. Когда это вещество накапливается в избытке, оно может вызывать ишемическое смещение ST и повышенную чувствительность к болевым стимулам. В пользу этого говорит положительный эффект на терапию аминофиллином.
Обобщая вышесказанное, можно отметить, что основными факторами, определяющими развитие загрудинных болей при данной патологии, являются дефектная эндотелинзависимая вазодилатация и снижение порога восприятия боли (рис. 1).
| Рисунок 1. Схема основных звеньев патогенеза кардиалгического синдрома X |
Клинические аспекты. Среди больных с КСХ преобладают лица среднего возраста, соотношение полов 1:1 с некоторым преобладанием женщин. В качестве основной жалобы фигурируют эпизоды болей за грудиной стенокардитического характера, возникающих во время физической нагрузки или провоцирующихся холодом, эмоциональным напряжением; с типичной иррадиацией в ряде случаев боли более продолжительные, чем при ИБС, и не всегда купируются приемом нитроглицерина (у большинства больных препарат ухудшает состояние).
При инструментальном обследовании у существенной части пациентов обнаруживаются приходящие или стойкие нарушения проводимости (по типу блокады левой ножки пучка Гиса). При ЭКГ покоя во время приступа загрудинных болей, пробах с физической нагрузкой и 48-часовом мониторировании по Холтеру обнаруживаются признаки ишемической депрессии сегмента ST, превышающие 1,5 мм по амплитуде и 1 мин по времени. Суточный профиль эпизодов ишемии показывает их высокую частоту в утренние и дневные часы; ночью и ранним утром ишемия встречается редко (как и у больных с ИБС). При нагрузочной сцинтиграфии миокарда с 201Tl имеются типичные ишемические очаговые нарушения накопления препарата.
Лабораторно во время приступа выявляется накопление миокардиального лактата. При проведении дипиридамоловой пробы у больных не отмечается увеличения коронарного кровотока на уровне мелких коронарных сосудов, клинически это проявляется усилением выраженности ишемии, появлением болей в грудной клетке. Положительной является эргометриновая проба, причем при оценке сердечного выброса отмечается его уменьшение на фоне введения препарата.
Сегодня в качестве диагностических критериев выделяются [1, 2, 5]:
- типичная боль в грудной клетке и значительная депрессия сегмента ST при физической нагрузке (в том числе на тредмиле и велоэргометре);
- преходящая ишемическая депрессия сегмента ST≥1,5 мм (0,15 мВ) продолжительностью более 1 мин при 48-часовом мониторировании ЭКГ;
- положительная дипиридамоловая проба;
- положительная эргометриновая (эрготавиновая) проба, снижение сердечного выброса на ее фоне;
- отсутствие атеросклероза коронарных артерий при коронароангиографии;
- повышенное содержание лактата в период ишемии при анализе крови из зоны коронарного синуса;
- ишемические нарушения при нагрузочной сцинтиграфии миокарда с 201Tl.
Дифференциальный диагноз. При первом обращении больного с кардиалгией всегда встает вопрос о дифференциальной диагностике этого состояния. На данном этапе важно правильно расспросить больного, выяснить особенности болевого синдрома и проанализировать прежде всего, насколько они соответствуют типичным проявлениям стенокардии.
При сборе анамнеза стоит обратить внимание на возраст и пол больного, наличие факторов риска и профессиональных вредностей. Существенную помощь может оказать имеющаяся медицинская документация, указывающая на сопутствующую патологию (порок сердца, длительно сохраняющуюся анемию, тиреотоксикоз, хронические заболевания легких и т. д.), которая способна симулировать клинику стенокардии. При объективном исследовании выявляются признаки, характерные для имитирующих стенокардию заболеваний: увеличение щитовидной железы, боль при пальпации области грудного отдела позвоночника, межреберных промежутков, плечевого сустава, изменение дыхательных шумов, тахикардия, аритмия, шумы в области сердца. Даже если на основании беседы с больным, изучения медицинской документации и объективного исследования вы убедились в том, что кардиалгия связана не с ИБС или КСХ, а с какой-то иной причиной, не стоит пренебрегать дополнительными обследованиями, которые могут опровергнуть ваши данные.
План дополнительного обследования пациента должен включать:
- общий анализ крови (исключение анемии, воспалительных изменений, которые могут быть связаны с латентно протекающей инфекцией, признаков активности ревматологического заболевания);
- липидный спектр (определение вероятности атеросклероза);
- уровень глюкозы натощак и/или при необходимости тест глюкозотолерантности (исключение сахарного диабета как фактора риска ИБС);
- острофазовые показатели (С-реактивный белок, сиаловые кислоты, серомукоид, фибриноген), ревматоидный фактор — для исключения ревматологической патологии;
- УМСС или реакцию Вассермана (для исключения сифилиса);
- стандартную ЭКГ и/или пробы с нагрузкой, холтеровское мониторирование;
- рентгенографию грудной клетки (размеры сердца, легочные поля), которая позволяет исключить наличие пневмонии, туберкулезного процесса в легких, плевральных наложений;
- при наличии признаков, указывающих на возможность выявления остеохондроза или другой патологии позвоночника, — рентгенографию грудного и шейного отделов позвоночника в прямой и боковой проекциях, функциональные пробы;
- ЭхоКГ — при наличии сердечных шумов, изменении размеров сердца при топографической перкуссии или по данным рентгенографии;
- ФГДС — при наличии жалоб со стороны пищеварительной системы и одновременно жгучих болей за грудиной (для исключения гастроэзофагеальной рефлюксной болезни);
- УЗИ органов брюшной полости — для исключения иррадиирующих болей, вызванных холециститом, панкреатитом и др.;
- коронароангиографию — проводится у пациентов, у которых окончательно нельзя исключить атеросклеротическое поражение коронарных артерий.
Перечисленные исследования в большинстве случаев позволяют точнее дифференцировать заболевания, входящие в «синдром болей в левой половине грудной клетки»; при этом исследования можно проводить по алгоритму оптимальной диагностической целесообразности. Иначе говоря, основываясь на данных субъективного и объективного методов обследования, следует составить план дальнейшего исследования (с учетом экономических затрат и уменьшения времени диагностики).
В качестве ориентира можно предложить алгоритм, представленный на рис. 2. Задачей диагностического поиска в этом случае является разделение кардиальных и экстракардиальных причин болей; отправным методом проведения диагностики избрана электрокардиография (рутинная, нагрузочные пробы или холтеровское мониторирование), которая доступна в большинстве лечебных учреждений и отличается простотой в использовании и дешевизной. Обнаружение любых(!) изменений на ЭКГ в более чем 90-95% случаев настораживает в плане кардиального генеза болевого синдрома (хотя стоит помнить и о возможности сочетания кардиальных и экстракардиальных причин), а их отсутствие убеждает в обратном. Далее необходимо разделить больных по возрасту и полу, после чего проанализировать наиболее вероятные кардиалгии в той или иной возрастно-половой группе и методы верификации диагноза. Эпидемиологический подход с учетом факторов возраста и пола существенно удешевляет и ускоряет процедуру дополнительного исследования.
Для уточнения экстракардиальной причины боли необходим поиск дополнительного синдрома, который осуществляется на основании жалоб больного, сбора анамнеза, а также минимального физикального исследования. После уточнения синдрома (патологии органов пищеварения, дыхания, костно-мышечной системы и т. д.) круг диагностического поиска еще более сузится.
Таким образом, при дифференциальной диагностике кардиалгий в качестве основных методов должны рассматриваться беседа с больным, физикальное исследование, электрокардиография (рутинная и мониторирование и/или нагрузочная), выделение ведущих синдромов с использованием принципа оптимальной диагностической целесообразности. Имеют значение эпидемиологические факторы (пол, возраст, курение).
Вопросы лечебной тактики у больных с кардиалгическим синдромом Х до конца не отработаны, но с учетом имеющихся в литературе данных стоит расставить некоторые принципиальные акценты. Необходимо в зависимости от ситуации проводить терапию в целях купирования болей в области сердца либо их предупреждения.
При приступе стенокардии на фоне КСХ больному назначается β-блокатор под язык (анаприлин в дозе 20-40 мг), антагонист Ca++ (нифедипин 5-10 мг) или вводится внутривенно 5-15 мл 2,4%-ного раствора аминофиллина (эуфиллина) в течение 15 мин [5]. От приема нитратов лучше воздержаться.
Для профилактики появления болей в области сердца обсуждается использование препаратов теофиллина длительного действия (теопека, теодура, теотарда и др.), особенно это показано больным с отсутствием тахикардии, сопутствующей обструктивной патологией дыхательных путей (бронхиальная астма, хронический обструктивный бронхит); при наличии тенденции к артериальной гипертонии препаратами выбора могут стать нифедипин длительного действия или амлодипин. Используются также психокорректоры (обычно антидепрессанты, в частности имипрамин) [6], антиагреганты.
Прогноз при синдроме Х в целом благоприятный и риск летальности, несмотря на яркую клиническую симптоматику, крайне низок. Однако при благоприятном общем прогнозе для больных с КСХ характерно низкое качество жизни, что обусловлено ограничением физической активности и выраженным болевым синдромом. Отмечена тенденция к переходу заболевания в дилатационную кардиомиопатию (особенно при наличии блокады левой ножки пучка Гиса по ЭКГ), в типичную ИБС.
Кардиалгический синдром Х — это заболевание, которое очень трудно выявить, оно может рассматриваться скорее как диагноз исключения, в связи с этим особенно важно уметь его дифференцировать.
Литература
- Калягин А. Н. Кардиалгический Х-синдром // Сибирский мед. журнал. 2001. Т. 25. № 2. С. 9-14.
- Костюк Ф. Ф. Х-синдром // Кардиология. 1992. Вып. 32. № 1. С. 80-82.
- Кудрявцев С. А. Особенности патогенеза, клиники и неинвазивной диагностики ишемической болезни сердца с ангиографически неизмененными коронарными артериями: Автореф. … канд. мед. наук, 1998.
- Майчук Е. Ю., Мартынов А. И., Виноградова Н. Н., Макарова И. А. Синдром Х // Клин. медицина. 1997. № 3. С. 4-7.
- Иоселиани Д. Г., Ключников И. В., Смирнов М. Ю. Синдром Х (вопросы определения, клиники, диагностики, прогноза, лечения) // Кардиология. 1993. Вып. 33. № 3. С. 80-85.
- Метелица В. И. Новое в лечении хронической ишемической болезни сердца. М.: Инсайт, 1999. 212 с.
А. Н. Калягин, ИГМУ, Иркутск