Кровь – это связующая нить между всем организмом человека. Она – как реки, питающие, дающие жизнь человеку. Практически каждое событие, происходящее в нашем организме, затрагивает кровеносную систему. Беременность перестраивает весь организм женщины, в том числе и кровеносную систему. Меняется и состав крови. В результате у будущей мамы может развиться тромбофилия. А женщине, страдающей тромбофилией, следует при наступлении беременности сразу же обсудить с врачом медикаментозную поддержку и схему анализов, которые позволят следить за состоянием крови и вовремя предупредить осложнение.
Чем опасна тромбофилия при беременности и что это за болезнь?
Планирование беременности при тромбофилии
Тромбофилия – это заболевание, при котором существенно повышается свертываемость крови, что влечет за собой риск развития тромбоза.
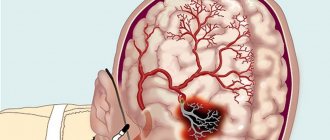
Сами по себе тромбы при нормальном стечении обстоятельств защищают организм человека, а не калечат его: если сосуд повреждается, образуется тромб, который закупоривает поврежденный сосуд. Но при тромбозе тромбы могут образовываться и в совершенно здоровых сосудах, перекрывая приток крови и питательных веществ к тканям.
Женщина может болеть тромбофилией и планировать стать матерью. Это вполне естественно. Но не так уж и редко болезнь развивается во время беременности.
В обоих случаях тромбофилия может стать опасной как для плода, так и для беременной женщины, поэтому необходимо контролировать состояние крови, чтобы вовремя отследить развитие болезни и начать лечение как можно раньше.
Симптоматика
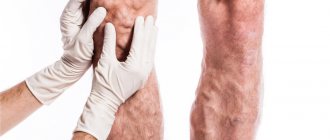
Болезнь часто протекает без каких-либо видимых признаков. Иногда в венах, находящихся на голени, можно диагностировать тромбозы. Данный недуг провоцирует появление покраснений, неприятных ощущений и отеков. Избавляются от проблемы при помощи специальных, разжижающих кровь, лекарственных препаратов. Определить заболевание при тромбофилии можно используя ультразвуковое обследование или рентген.
Тромбы могут стать причиной летального исхода, если оторвутся, то попадут в кровоток, ведущий к жизненно важным органам.
Появление тромба сопровождается следующими симптомами:
- дыхание затруднено;
- стопы и голени немеют;
- при вдохе появляются боли в груди;
- учащенное сердцебиение и инфаркты в раннем возрасте;
- кашель с кровью;
- частые выкидыши;
- самый явный признак тромбофилии – боль в области образования тромба, отек.
Наследственная тромбофилия и беременность
Заболевание, которое влияет на кровеносную систему, не может не влиять на организм в целом. Так, тромбофилия вносит свой вклад в способность женщины зачать ребенка. Из-за недостаточного кровоснабжения матки и органов малого таза эмбрион может не приживаться или вскоре отторгаться организмом.
Болезнь может быть наследственной. При беременности влиять на развитие генетической тромбофилии будут гены, отвечающие за свертываемость крови, и гены ферментов, которые контролируют обмен фолиевой кислоты.
В случае, если среди ближайших родственников есть страдающие этим заболеванием, при планировании беременности следует пройти молекулярно-генетическое исследование. И, если окажется, что болезнь передалась по наследству, желательно немедленно начать лечение, чтобы избежать проблем со здоровьем будущей матери и плода.
Опасность и факторы риска возникновения
На развитие заболевания влияет наследственный фактор (тромбофилия генетическая). Но существуют и некоторые приобретенные риски:
- заболевания крови. Эритремия, атеросклероз, варикозное расширение вен нижних конечностей, артериальная гипертензия;
- косвенно на развитие патологии могут повлиять и болезни, влияющие на двигательную активность (болезнь Шляттера), злокачественные образования, аутоиммунные заболевания (антифосфолипидный синдром, системная красная волчанка), поликистоз почек;
- инфекционные процессы;
- перенесенный инфаркт или инсульт;
- хирургические вмешательства;
- катетеризация вен;
- заболевания печени;
- ожирение;
- период беременности;
- нефротический синдром;
- некоторые лекарственные препараты (оральные контрацептивы, преднизолон).
Чем опасна тромбофилия при беременности
Почему именно для беременной женщины опасна тромбофилия? Потому что в ее организме зарождается новая жизнь с собственной кровеносной системой. У человека есть два круга кровообращения – большой и малый. У беременной женщины появляется еще один круг кровообращения, который называется плацентарным, по которому кровь вместе с питательными веществами поступает напрямую к плоду. Если кровь будет слишком вязкой, то скорость ее течения будет ниже, чем следует для нормального обеспечения будущего ребенка кислородом и всеми другими полезными веществами.
Кроме того, чтобы защитить женщину при родах от обширной кровопотери, организм повышает свертываемость крови. Но кровь при заболевании и так сворачивается очень быстро, поэтому риск образования тромбов повышается в несколько раз. Тромб может полностью перекрыть даже крупные сосуды, или же существенно уменьшить его просвет. Что тоже будет мешать крови свободно поступать к плоду.
В итоге при тромбофилии при беременности последствия для ребенка могут повлечь за собой угрозу замершей беременности, выкидыша или рождения ребенка с пороками развития. Кислородное голодание может стать причиной отставания в развитии новорожденного, слабого иммунитета. Но болезнь способна повредить и организму самой беременной женщины. Последствиями могут стать появление варикоза, очень сильный токсикоз, угрожающий жизни женщины, преждевременное отслоение плаценты с обильной кровопотерей. Если тромб закупорит сосуд мозга, то заболевание может привести к летальному исходу.
Гематогенные тромбофилии: акушерско-гинекологические аспекты
Авторы: Майоров М.В.
«Multi multa, nemo omnia novit»(«Многие знают много, но никто не знает всё», лат.)
Тромбофилией называется склонность к развитию тромбов. Различают гематогенную (изменения факторов свёртывающей, противосвёртывающей и фибринолитической систем), сосудистую (атеросклероз, васкулиты и т. д.) и гемодинамическую тромбофилию (различные нарушения системы кровообращения). Гематогенные тромбофилии (ГТ) широко распространены в клинической практике, осложняют течение многих заболеваний и могут приводить к ранней инвалидизации и даже гибели больных. Основными клиническими проявлениями ГТ являются рецидивирующие тромбозы вен и /или артерий, тромбоэмболии, ишемии и инфаркты органов, нарушения мозгового кровообращения, а также другие нарушения в магистральных сосудах и зонах микроциркуляции.
Исследования последних лет показали, что наличие тромбофилии сопряжено с повышенным риском осложнений беременности (привычное невынашивание, плацентарная недостаточность, задержка роста плода, преэклампсия), а также осложнениями при приёме комбинированных оральных контрацептивов (венозные тромбозы).
ГТ могут быть первичными, генетически обусловленными, а также вторичными, связанными с другими заболеваниями. Нарушения гемостаза, лежащие в основе многих тромбофилий, пока недостаточно известны широкому кругу коллег и часто своевременно не диагностируются.
В последние годы в связи с открытием ряда ранее неизвестных генетически обусловленных дефектов гемостаза, предрасполагающих к тромбозу (мутация фактора V Leiden, мутация протромбина и др.), стало возможным объяснение ранее необъяснимых случаев тромботических осложнений. Особенностью полиморфных вариантов данных генов является то, что они могут долгое время никак себя не проявлять. Патологические симптомы нередко возникают при дополнительных условиях (особенности питания, беременность, прием лекарств, образ жизни и т. д.). Выяснение этих дополнительных условий помогает эффективно предотвращать развитие заболеваний и их осложнений у носителей «дефектных» генов.
Различают две основные группы гематогенных тромбофилий: 1) связанные, преимущественно, с изменениями реологических свойств и клеточного состава крови; 2) обусловленные первичными нарушениями в системе гемостаза.
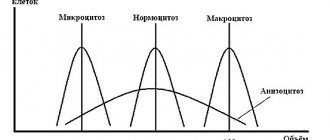
В первой группе выделяют формы, связанные с избытком клеток крови и её сгущением (полицитемия, эритроцитозы, тромбоцитемии и др.), с нарушением формы и «деформабельности» эритроцитов (например, множественные тромбозы и инфаркты при серповидноклеточной анемии), с повышением вязкости плазмы (миеломная болезнь, болезнь Вальденстрема, криоглобулинемия и др.).
Во второй группе выделяют формы: а) связанные с повышением агрегационной функции тромбоцитов (в том числе вследствие нарушения равновесия между стимуляторами и ингибиторами агрегации в плазме крови); б) связанные с гиперпродукцией и гиперактивностью фактора Виллебранда; в) связанные с дефицитом или аномалиями основных физиологических антикоагулянтов: антитромбина III, белков C и S; г) связанные с дефицитом или аномалиями факторов свёртывания крови и компонентов фибринолитической и калликреин — кининовой системы (дефицит фактора XII, плазменного пре — калликреина, высокомолекулярного кининогена, активатора плазминогена, ряд молекулярных аномалий фибриногена и др.).
Все эти нарушения могут быть наследственными, т. е. генетически обусловленными, и приобретёнными (симптоматическими). Профилактика и лечение наследственных тромбофилий может успешно осуществляться, в частности, имеющимися на вооружении клиницистов гепарином и оральными антикоагулянтами. В связи с этим основной проблемой этой части современной медицины являются выявление маркеров тромбофилий и отработка режимов противотромботической терапии (дозировки препаратов и длительности их назначения).
Можно предполагать, что предрасположенность к тромбозам детерминирована генетически. Основными мутациями, имеющими высокое прогностическое значение, являются следующие:
Мутация метилен-тетра-гидро-фолат-редуктазы.Наиболее изученной мутацией является вариант, в котором нуклеотид цитозин (C) в позиции 677, относящейся к 4-му экзону, заменен на тимидин (T), что приводит к замене аминокислотного остатка аланина на остаток валина в сайте связывания фолата. Такой полиморфизм MTHR обозначается, как мутация C677T. У лиц, гомозиготных по данной мутации, отмечается термолабильность MTHFR и снижение активности фермента примерно до 35% от среднего значения. Наличие этой мутации сопровождается повышением уровня гомоцистеина в крови. Повышение частоты аллеля 677T было отмечено не только при позднем токсикозе (гестозе), но и при других осложнениях беременности (отслойке плаценты, задержке роста плода, антенатальной смерти плода). Сочетание аллеля 677T с другими факторами риска приводит к повышению риска раннего выкидыша.
Лейденская мутация гена V фактора свертывания крови.Лейденская мутация гена V фактора свертывания крови характеризуется заменой нуклеотида гуанина на нуклеотид аденин в позиции 1691. Это приводит к замене аминокислоты аргинина на аминокислоту глутамин в позиции 506 в белковой цепи, являющейся продуктом этого гена. Мутация наследуется по аутосомно — доминантному типу. Наличие Лейденской мутации повышает вероятность развития целого ряда осложнений беременности: невынашивания на ранних сроках (риск повышается в 3 раза), отставания развития плода, позднего токсикоза (гестоза), фетоплацентарной недостаточности.
Одним из самых опасных осложнений применения гормональных контрацептивов являются тромбозы и тромбоэмболии. Оказалось, что многие женщины с такими осложнениями — гетерозиготные носители Лейденской мутации. На фоне приема гормональных контрацептивов риск тромбозов повышается в 6 — 9 раз. При наличии у пациентки Лейденской мутации риск развития тромбозов на фоне приема оральных контрацептивов повышается в 30 — 50 раз. Поэтому некоторые авторы предлагают обследовать на наличие Лейденской мутации всех женщин, принимающих гормональные контрацептивы или собирающихся их принимать. Как известно, тромбозы являются одним из грозных осложнений послеоперационного периода. В США, например, предлагают обследовать на наличие Лейденской мутации всех пациентов, готовящихся к большим операциям (по поводу миомы матки, кисты яичника, для кесарева сечения, и пр.).
С другой стороны, согласно литературным данным, в возрастной группе женщин, пользующихся гормональными контрацептивами, абсолютный риск тромбоэмболий настолько низок, что даже существенное повышение относительного риска может иметь весьма относительное значение (18). «Ab posse ad esse consequential non valet» («Из возможного ещё не следует действительное», лат.). Так, частота возникновения венозного тромбоза у молодых женщин составляет 2 на 10 тыс. человеко /лет, а тромбоэмболии легочной артерии со смертельным исходом — 6 на 100 тыс. человеко / лет. Если предположить, что все случаи со смертельным исходом обусловлены наличием Лейденской мутации фактора V, то для выявления 20 – 25 тыс. женщин с этой мутацией скринингу необходимо подвергнуть 500 тыс. женщин. Запретив носительницам мутантного гена использовать оральные контрацептивы, можно предупредить один случай смерти в год. Затраты на проведение подобного скрининга будут огромными. Кроме того, если женщины-носительницы мутантного гена, прекратив приём КОК, не будут использовать другой, не менее эффективный способ контрацепции, реально возникнет целый ряд неблагоприятных, потенциально опасных клинических последствий. Таким образом, «Certa amittimus, dum incerta petimus» («Гонясь за сомнительным, мы упускаем верное», лат.).
Мутация гена протромбина G20210A. Мутация гена протромбина G20210A характеризуется заменой нуклеотида гуанина на нуклеотид аденин в позиции 20210. При наличии данной мутации обнаруживаются повышенные количества химически нормального протромбина. Уровень протромбина может быть в полтора — два раза выше, чем в норме. Гетерозиготными носителями гена являются 2 — 3% представителей европейской расы. Мутация наследуется по аутосомно-доминантному типу. Это означает, что тромбофилия возникает даже у гетерозиготного носителя измененного гена. При возникновении тромбозов мутация G20210A часто встречается в сочетании с Лейденской мутацией.
Данная мутация является фактором риска всех осложнений, связанных с Лейденской мутацией (невынашивание беременности, фетоплацентарная недостаточность, внутриутробная гибель плода, гестозы, задержка развития плода, отслойка плаценты). Общепризнанно, что точное определение генетических маркеров может отражать подверженность предполагаемому фактору риска в течение всей жизни пациента лучше, чем соответствующие анализы плазмы, результаты которых могут изменяться со временем.
Антифосфолипидный синдром (синдром Hughes).Своеобразным вариантом ГТ является антифосфолипидный синдром (АФС) – симптомокомплекс, включающий венозные и/или артериальные тромбозы, различные формы акушерской патологии (в первую очередь, привычное невынашивание беременности), тромбоцитопению, а также другие разнообразные неврологические, кожные, сердечно – сосудистые и гематологические нарушения. В 1994 году на международном симпозиуме по антифосфолипидам было предложено называть АФС по имени английского ревматолога Hughes, впервые его описавшего и внесшего наибольший вклад в изучение этой проблемы.
Антифосфолипидные антитела (гетерогенная популяция антител, реагирующая с широким спектром фосфолипидов) могут непосредственно связываться с мембраной тромбоцитов, усиливая адгезию и агрегацию тромбоцитов; в конечном счёте, этот процесс может приводить к формированию тромба. Антифосфолипидные антитела способны вызывать тромботический эффект на сосудистом эндотелии, связываясь с фосфолипидами эндотелиальной клеточной стенки и отрицательно влияя на нормальную продукцию простациклина, являющегося вазодилататором и ингибитором агрегации тромбоцитов.
Течение гематогенных тромбофилий, тяжесть и распространённость тромботических осложнений непредсказуемы, взгляды на необходимость проведения диагностики и терапии различны, универсальные схемы лечения больных, к сожалению, отсутствуют. У одних больных АФС проявляется, преимущественно, венозными тромбозами, у других – инсультом, у третьих – акушерской патологией или тромбоцитопенией.
Так как при АФС потенциально могут поражаться сосуды любого калибра (от капилляра до аорты), спектр клинических проявлений чрезвычайно разнообразен. Наиболее характерным проявлением АФС является развитие акушерской патологии: — привычное невынашивание беременности (два и более самопроизвольных выкидыша), неразвивающиеся беременности в I и III триместрах; — антенатальная гибель плода; — преждевременные роды; — тяжёлые формы преэклампсии (гестоза); — задержка внутриутробного развития плода; — тяжёлые осложнения послеродового периода.
Спектр клинических проявлений требует проведения широкого диагностического поиска, внедрения новых высокочувствительных лабораторных методов обследования. Несмотря на достигнутый за почти 20 лет определённый прогресс в изучении механизмов развития, клинических особенностей и подходов к лечению, тромбофилические осложнения, в частности, при беременности, продолжают оставаться одной из наиболее актуальных мультидисциплинарных проблем современной медицины (5).
Тромбофилии могут быть управляемы применением небольших доз ацетилсалициловой кислоты (аспирина), гепарина, фолиевой кислоты, внутривенного введения иммуноглобулинов или концентратов цитокининов. Больным с АФС назначают антикоагулянты непрямого действия и антиагреганты (низкие дозы ацетилсалициловой кислоты), которые широко используются для профилактики тромбозов, не связанных с АФС.
Однако ведение больных с АФС имеет свои особенности, что связано с высокой частотой рецидивирования тромбозов. У беременных женщин без акушерской патологии в анамнезе с высоким уровнем АФЛ в сыворотке (но с отсутствием клинических признаков АФС) можно ограничиться назначением небольших доз ацетилсалициловой кислоты (75 мг/сутки). Эти пациентки требуют тщательного динамического наблюдения, т.к. риск тромботических осложнений у них довольно высок. Для тромбофилии с повторяющимися неблагоприятными исходами беременности, по имеющимся литературным данным, заслуживают внимания два варианта лечения: низкомолекулярным гепарином эноксапарином – у женщин с привычной поздней потерей плода, и лечение фолиевой кислотой (от 0,5 до 5 мг в сутки) – при тяжёлом гестозе. У больных как вторичным, так и первичным АФС, лечённых высокими дозами непрямых антикоагулянтов (варфарин), позволяющими поддерживать состояние гипокоагуляции, отмечалось достоверное снижение частоты рецидивирования тромботических осложнений. Однако использование высоких доз непрямых антикоагулянтов ассоциируется с увеличением риска кровотечений. Лечение гепарином в дозе 5000 ЕД 2 — 3 раза в день в сочетании с низкими дозами ацетилсалициловой кислоты у женщин с привычным невынашиванием беременности позволяет повысить частоту успешных родов примерно в 2 – 3 раза.
Также сообщается об эффективности плазмафереза, внутривенного введения иммуноглобулина, использования препаратов простациклина, фибринолитических средств, препаратов рыбьего жира у женщин с акушерской патологией. Большие надежды возлагают на низкомолекулярные гепарины, а также внедрение новых методов антикоагулянтной терапии, основанных на применении аргиналов, гируидинов, антикоагулянтных пептидов, антитромбоцитарных агентов (моноклональные антитела к тромбоцитам, RGD-пептиды) и других. «Nil actum reputans, si quid superessit agendum» («Не считай сделанным то, что ещё нужно сделать», лат.).
Таким образом, рациональная профилактика, ранняя диагностика, своевременное и адекватное лечение различных тромбофилий позволят снизить количество тромботических осложнений у пациенток акушерско — гинекологического профиля.
ЛИТЕРАТУРА
1. Бокарев И.Н., Бокарев М.И. Тромбофилии, венозные тромбозы и их лечение // Клин. мед., 2002. – № 5 , с. 4-8. 2. Громыко Г. Л. Роль антифосфолипидного синдрома в развитии акушерских осложнений // Проблемы репродукции, 1997, 3 4, с. 13 – 18. 3. Дёмина Т. Н. Профилактика осложнений беременности у женщин с привычным невынашиванием беременности при антифосфолипидном синдроме // Вестник эпидемиологии и гигиены, 1999, Т. 3, № 1, с. 176 — 181. 4. Дёмина Т. Н. Успехи и проблемы в диагностике и лечении антифосфолипидного синдрома в акушерской практике // Медико-социальные проблемы семьи, 1998, Т. 3, № 1, с. 62 -71. 5. Жук С. И., Чечуга С. Б., Лобастова Т. В. Современные аспекты патогенеза, диагностики и лечения антифосфолипидного синдрома и других тромбофилических состояний при беременности // www.medexpert.org.ua. 6. Майоров М. В. Антифосфолипидный синдром и акушерская патология: диагностика и лечение // Провизор, 2002, № 2, с. 33 – 35. 7. Макацария А.Д., Бицадзе В.О., Гениевская М.Г. и соавт. Антифосфолипидный синдром в акушерской практике, Москва: Руссо, 2001. – 344 c. 8. Насонов Е. Л., Баранов А. А., Шилкина Н. П., Алекберова З. С. Патология сосудов при антифосфолипидном синдроме, Москва – Ярославль, 1995, с. 162. 9. Насонов Е. Л., Алекберова З.С., Калашникова Л.А. и др. Антифосфолипидный синдром (синдром Hughes): 10 лет изучения в России // Клин. Мед., 1998, № 2, с. 4-11. 10. Папаян Л. П., Тарасова М. А., Кобилянская В. А., Григорьева В. А. Тромбофилия и комбинированные оральные контрацептивы // Проблемы репродукции, 1999, № 4. 11. Патрушев Л. И. Тромбофилические состояния и современные методы их диагностики // Рус. Мед. журнал, 1998; 6:3:63: 181 – 185. 12. Чайка В. К., Дёмина Т. Н., Яковлева Э. Б. и др. Антифосфолипидный синдром в акушерстве гинекологии и перинатологии. Методические рекомендации, Донецк, 2000. 13. Bertina R .M., Koeleman B. P., Koster T., Rosendaal F. R., Dirven R.. J, de Ronde H., van der Velden P.A., Reitsma P. H. Mutation in blood coagulation factor V associated with resistance to activated protein C.// Nature. — 1994. — Vol. 369. — P. 64- 67. 14. Brenner B. Thrombophilia and fetal loss.// Seminars in Thromb. Haemost. – 2003. – Vol. 29 (2) – P. 165-170. 15. Cumming A.M., Tait R. C., Fildes S., Yoong A., Keeney S., Hay C.R. Development of resistance to activated protein С during pregnancy.// Br. J. Haematol. – 1995. – Vol. 90 — P.725-727. 16. Dahlbock В., Carlsson M., Svensson P.J. Familial thrombophilia due to a previously unrecognized mechanism characterized by poor anticoagulant response to activated protein C: prediction of a cofactor to activated protein C.// Proc. Natl. Acad. Sci. USA — 1993. — Vol. 90. – P. 1004 -1008. 17. Nachman R. L. Silverstein R. Hypercoagulable states. Ann. Intern. Med. 1993; 119: 819 – 827. 18. Price D. T., Ridker P. M. Factor V Leiden mutation and the risk for thromboembolic disease: a clinical perspective. Ann. Inern. Med. 1997; 127:895 – 903.
Консультации Марка Вениаминовича Майорова в КлубКоме
опубликовано 03/12/2013 15:14 обновлено 09/12/2013 — Акушерство, гинекология, маммология
Диагностика тромбофилии у беременных
Диагностировать тромбофилию при беременности сложно, поэтому при малейших симптомах заболевания следует обратиться к специалисту. Признаков не так много, не всегда их трактуют в пользу заболевания.
Показательными являются сильный токсикоз, нарушения свертываемости крови (сеточка лопнувших сосудов или синяки под ногтями), повышенное артериальное давление, судороги.
Тромбы могут образовываться в любых сосудах и вызывать боль в различных частях тела, даже предынфарктное состояние. Диагноз «тромбофилия» могут заподозрить и по реакции плода: если к нему не поступает достаточное количество питательных веществ, он может проявлять излишнюю активность или, напротив, замереть.
Генетическая тромбофилия влияет на особенность родов?
Данная патология не является причиной для выбора в пользу, например, кесарева сечения. Способ родоразрешения выбирается, как и в прочих случаях.
Сдача анализов
Количество и время сдачи анализов определяет гинеколог. Результат сдачи крови из вены обычно готов на следующий день (имеется возможность срочного анализа).
Состояние системы свертывания крови оценивается по:
— гемостазиограмме;
— агрегации тромбоцитов;
— D-димеру.
Какой медицинский специалист назначает курс лечения?
При достаточной квалификации гинеколога никаких дополнительных консультаций для проведения лечения не требуется.
Гинеколог разбирается в гемостазе?
В медицинском центре работают врачи-гинекологи, уровень квалификации и опыт врачебной деятельности которых, несомненно, соответствуют необходимым требованиям.
Анализ на тромбофилию при беременности и ее планировании
Для того чтобы обнаружить или исключить болезнь, сдают два анализа крови – общий и коагулограмму, комплексный анализ показателей свертываемости крови.
Кровь для коагулограммы берут из вены, натощак (желательно не есть за 12 часов до взятия анализа). Перед анализом на свертываемость крови нельзя:
- курить;
- принимать алкоголь и психотропные вещества;
- есть жирную и острую пищу;
- предупредить лаборанта о приеме лекарств, если отказаться от препаратов не представляется возможным.
Особенно важно пройти анализы на тромбофилию при планировании беременности, если в семье есть случаи заболевания, чтобы диагностика наследственного заболевания помогла вовремя начать лечение.
Профилактика осложнений тромбофилии
Насколько бы профессиональный не был врач, нельзя перекладывать ответственность за свое здоровье только на достижения современной медицины, важно помнить, что каждый человек сам тоже должен заботиться о нем. Для того чтобы предотвратить появления осложнений при тромбофилии, нужно выполнять ряд простых правил:
- пересмотреть свой образ жизни. Сегодня риску болезни подвержены все, кто много сидит и мало двигается. Умеренная физическая активность, зарядка, лечебная физкультура только укрепят здоровье;
- правильный рацион питания, отказ от чрезмерного употребления жирного и копченого, а также промышленных полуфабрикатов;
- уменьшить количество потребляемого мяса;
- специальный питьевой режим — необходимо выпивать не менее полутора литра чистой воды в день;
- профилактические врачебные осмотры.
Данная статья размещена исключительно в познавательных целях и не является научным материалом или профессиональным медицинским советом.
Лечение тромбофилии при планировании беременности
Лекарства, диета и строгий режим – это три основных направления при лечении заболевания.
Лекарства при тромбофилии – это антикоагулянты, препараты для уменьшения свертываемости крови, они назначаются индивидуально и исключительно специалистами.
Дополнительно для лечения тромбофилии при планировании беременности рекомендуют принимать Омега-3. Прием Омега-3 уменьшает вязкость крови, снижает производство тромбоксана, сужающего сосуды, улучшает текучесть мембран эритроцитов. Все это оказывает антитромботическое действие при приеме на регулярной основе. Поэтому врачи рекомендуют непрерывный курс Омега-3 для профилактики тромбозов, особенно для женщин с высокими показателями свертываемости крови.
В составе комплекса Прегнотон Мама, рекомендованном для беременных женщин и подготовки к беременности, входят Омега-3 в эффективной дозировке. Принимать препарат можно в течение всего периода беременности.
Наши врачи
Малахов Юрий Станиславович
Врач — сердечно-сосудистый хирург, флеболог, Заслуженный врач РФ, доктор медицинских наук, врач высшей категории
Стаж 37 лет
Записаться на прием
Дроздов Сергей Александрович
Врач сердечно-сосудистый хирург, флеболог, доктор медицинских наук
Стаж 48 лет
Записаться на прием