Показания к протезированию
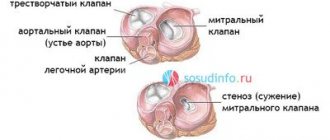
Для нормального кровотока необходима согласованная работа клапанного аппарата. Митральный, аортальный, трехстворчатый и клапан легочной артерии обеспечивают ток крови из камер сердца в аорту и легочный ствол, выполняя главную роль к гемодинамике. При разрушении их створок, сужении или неполном смыкании кровь поступает в сосуды в недостаточном количестве, что приводит к прогрессирующей сердечной недостаточности. Единственный способ улучшения состояния пациента – оперативное устранение дефекта и установка механического или биологического имплантата. Замена клапана на сердце и протезирование показаны при выявлении:
- врожденной или приобретенной сердечной патологии, порока сердца;
- постинфарктной патологии, аневризмы;
- пролапса, стеноза или недостаточности;
- атеросклеротического поражения;
- заболевания ревматической этиологии;
- атрезии клапана;
- инфекционного эндокардита и септического поражения;
- фиброзных рубцов или спаек на створках;
- кальциноза и уплотнения.
Клинические признаки, свидетельствующие о необходимости операции:
- снижение толерантности к физическим нагрузкам;
- возникновение одышки, невозможность спать в горизонтальном положении, появление влажных хрипов в нижних отделах легких (вследствие повышения давления в малом кругу кровообращения);
- визуализация на ультразвуковом исследовании тромбов в полостях сердца;
- расширение полостей сердца на эхокардиографии (левое предсердие более 40 мм);
- возникновение аритмий (экстрасистолия, блокады).
Сравнение биологических и механических протезов клапанов сердца
Протезирование клапанов сердца решает проблему восстановления правильной циркуляции крови в нем и предупреждает развитие сердечной недостаточности. Как правило, протезы клапанов имплантируются, если выполнить реконструктивную пластику собственного клапана пациента невозможно из-за выраженного повреждения его элементов или подклапанных структур.
Идеальный протез клапана должен:
- бесперебойно функционировать в течение всей жизни пациента;
- вызывать минимум осложнений;
- не снижать качество жизни, в том числе постоянным приемом требующей регулярного контроля антикоагулянтной терапии;
- не влиять негативно на остальные структуры сердца.
К сожалению, из десятков модификаций механических и биологических протезов, ни одна не отвечает в полной мере этим требованиям. Как механические, так и биологические протезы имеют преимущества и недостатки, которые врач должен учитывать, делая выбор для конкретного пациента. Основные различия механических и биологических протезов клапанов заключаются в следующем:
| Характеристики протеза и особенности клинической ситуации | Механические протезы | Биологические протезы |
| Срок службы | более 20 лет | до 15 лет, отдельные модификации у пациентов старше 60 лет – до 25 лет |
| Необходимость в повторной операции для замены протеза | отсутствует, если не возникли осложнения | присутствует через определенное время, в зависимости от скорости деградации |
| Выживаемость через 10-15 лет | выше | ниже в связи с высокой частотой ревизионных повторных операций, при которых смертность в 2 раза выше, чем при первичной |
| Риск тромбоэмболических осложнений | высокий | низкий |
| Необходимость в пожизненной антикоагулянтной терапии | да | как правило, нет. Часто антикоагулянты назначаются в первые 3 месяца после операции, а дольше – только при высоком риске тромбоза, например, из-за фибрилляции предсердий |
| Невозможность регулярного лабораторного контроля пожизненной антикоагулянтной терапии один раз в 5-14 дней для коррекции доз препаратов | имплантация противопоказана | имплантация показана |
| Риск кровотечений | высокий | низкий |
| Возраст пациента | до 60 лет | после 60 лет |
| Непереносимость или противопоказания к применению антикоагулянтов | не имплантируют | имплантируют |
| Влияние на форменные элементы крови и белки плазмы | негативное | отсутствует |
| Сопротивление потоку крови | высокое, повышающее нагрузку на сердце | низкое, не повышающее нагрузку на сердце |
| Склонность к инфицированию | более низкая | более высокая, за исключением отдельных модификаций |
| Планирование беременности после протезирования клапана | не имплантируют | имплантируют |
Исходя из этих позиций, складывается общемировая статистика протезирования клапанов сердца – имплантируется приблизительно 2/3 механических и 1/3 биологических протезов. Причем в странах, где большинству пациентов невозможно обеспечить качественный мониторинг антикоагулянтной терапии, а также в возрастных группах пациентов старше 60 лет – ситуация прямо противоположная.
Важно, что технологии протезирования клапанов сердца непрерывно прогрессируют. Так, профессор Даниэль Битран, возглавляющий Кардиохирургический центр больницы Шаарей Цедек в Иерусалиме, подчеркивает, что там применяются биологические протезы клапанов нового поколения, срок службы которых может достигать 25 лет, если они имплантированы пациентам старше 60 лет, когда скорость их деградации снижается. В этой клинике, а также в Немецком кардиоцентре в Берлине применяются бесшовные и бескаркасные биопротезы клапана аорты.
Бескаркасные клапаны отличаются великолепной приживаемостью, низким риском инфицирования и являются лучшим выбором при разрушении корня аорты, эндокардите, абсцессе этой области. Бесшовные биопротезы могут имплантироваться с помощью катетерной технологии (TAVI), эффективны при выраженном кальцинозе аорты, у пациентов с высоким хирургическим риском.
Некоторые принципы выбора протезов клапанов сердца и ведения пациентов с ранее установленными клапанами в особых клинических ситуациях:
| Клиническая ситуация | Механический протез | Биологический протез |
| Наступление беременности, которую пациентка желает сохранить, при уже установленном протезе | Непрерывный контролируемый прием прямых или непрямых антикоагулянтов с учетом профилактики пороков плода до 36-й недели, далее – перевод на нефракционированный гепарин | Как правило, молодым женщинам биологические протезы не имплантируют, но если он был все же установлен, врач имеет больше возможностей ограничения приема антикоагулянтов, нежелательных для плода |
| Протезирование у детей и подростков | Показан | Противопоказан |
| Протезирование у молодых людей 25-35 лет | Показан | Относительно противопоказан |
| Необходимость в постоянном гемодиализе | Индивидуальный подход с учетом повышенного риска инсультов и кровотечений | Индивидуальный подход с учетом высокой скорости деградации протеза, по сравнению с пациентами без гемодиализа |
| Протезирование трикуспидального клапана | Высокий риск тромбоза из-за низкого давления и медленного кровотока | Низкий риск тромбоза и медленная деградация по сравнению с биопротезами в аортальной и митральной позициях |
Даже по столь краткому анализу можно судить о том, насколько сложен оптимальный выбор механического или биологического протеза сердца, сколько принципиально важных вопросов приходится решать врачу, взвешивая предпочтительность имплантации той или иной модели применительно к конкретной клинической ситуации. Поэтому пациенты ведущих кардиохирургов мира в Кардиохирургическом центре больницы Шаарей Цедек в Иерусалиме и Немецком кардиоцентре в Берлине имеют преимущества еще на предоперационном этапе, так как им гарантирован индивидуальный подход и всесторонне взвешенное решение, в обязательном порядке согласованное с ними.
Методики выполнения и техники операции
Перед оперативным вмешательством проводят лабораторные и инструментальные исследования для определения противопоказаний и степени риска возникновения нежелательных последствий.
Назначают такие анализы:
- общий и биохимический крови;
- коагулограмму;
- печеночные пробы (АСТ, АЛТ, билирубин);
- крови на вирусные гепатиты и ВИЧ;
- сахар крови (для исключения сахарного диабета);
- рентгенографию органов грудной полости;
- УЗИ сердца.
Для протезирования используют два вида клапанов:
- Механические, изготовленные из специальных сплавов с добавлением графита или синтетического силикона. Механизм таких имплантатов: шариковый, лепестковый с двумя или тремя створками, вентельный по типу наклонного диска. Они износостойкие, однако, требуют приема определенных лекарств после операции.
- Биологические, изготовленные из аллотрансплантата пациента, свиного или лошадиного ксенотрансплантата. Наиболее часто используют ткани животного происхождения. Показаны при тяжелой сердечной патологии с непереносимостью антикоагулянтов, пожилым людям.
Операция на сердце по замене клапана бывает открытой с наложением скоб и швов или малоинвазивной. Во втором случае не проводят обширное вмешательство: доступ получают катетерами и стентом через пунктированную вену и небольшой разрез на бедре.
- При открытой операции протезируют все клапаны. Делают стернотомию – рассечение кожи и грудной кости до сердца. Через разрез предсердия или желудочка получают доступ к пораженному клапану. Имплантат устанавливают на место разрушенного, фиксируют швами. Рассеченный участок ушивают, накладывают скобы и проволочные швы сращения и заживления.
- К малоинвазивным методам относится трансапикальное протезирование. Выполняют небольшой разрез в межреберном промежутке справа и малый на сердце, через который вводят проводник с камерой, катетер и имплантат. Используют для замены митрального и трикуспидального клапана.
- Протезирование через бедренную вену наиболее щадящее, используют для аортального клапана. Не нужен аппарат искусственного кровообращения. После седации катетер со сложенным клапаном через небольшой разрез на бедре вводят в сосуд и продвигают до полостей сердца под контролем рентгена. Достигнув клапана, хирурги раздувают сосуд баллоном, и имплантированный элемент самостоятельно заполняет просвет.
Новый подход к оценке ремоделирования сердца при протезировании митрального клапана
УЗИ сканер HS50
Доступная эффективность.
Универсальный ультразвуковой сканер, компактный дизайн и инновационные возможности.
Диагностический вклад каждого из применяемых сегодня структурно-геометрических показателей ремоделирования сердца обладает достаточной информативностью, но отражает только один из множества аспектов этого сложного процесса. Роль показателя, способного комплексно и в полной мере отразить динамику ремоделирования сердца, на наш взгляд, может выполнять соотношение объемов полостей сердца, получившее название индекса ремоделирования объемов (ИРО) полостей сердца. ИРО отражает соотношение объема желудочка к объему предсердия. Его можно использовать отдельно для оценки ремоделирования правых и левых отделов сердца. Поскольку специально проведенное исследование показало, что ремоделирование и левых, и правых отделов сердца происходит по идентичному алгоритму, наиболее целесообразным признано оценивать степень ремоделирования сердца по изменению индекса ремоделирования объемов левых камер [1, 2].
Механические дисковые протезы нарушают физиологическую структуру кровотока: разделяют единый кровоток на два эксцентричных потока, неравных по объему и скорости (основной и малый), что и приводит к нарушению однородности течения, превышению скоростей течения выше физиологических значений и образованию зон замедленного течения крови. Как правило, хирурги ориентируют эти протезы большим отверстием в сторону задней стенки левого желудочка (ЛЖ). Отклонение направления потока может потребовать дополнительного времени для адаптации полости ЛЖ к измененному кровотоку и более протяженных сроков восстановления геометрии формы. Эксцентричность потока (смещение центра потока от центра проходного отверстия дискового протеза) является их ключевой гемодинамической характеристикой. Для двустворчатых протезов характерен центральный характер потока (совмещение центра потока с центром проходного отверстия протеза), что, очевидно, более благоприятно для восстановления геометрии полости ЛЖ. Симметричность расположения запирательных элементов облегчает диастолическое заполнение. Структура кровотока на этих протезах более однородная, отклонение оси движения кровотока значительно меньше, чем у дисковых моделей [1-10].
В целом дисковые протезы при митральном протезировании не уступают двустворчатым типам ПКС по эффективности и безопасности функционирования, показателям выживаемости пациентов и развития осложнений в течение 10 лет после операции [7]. Но возможности дисковых типов ПКС в создании необходимого физиологически подобного потока в полости ЛЖ после митрального протезирования более ограничены, какой бы ни была ориентация большого отверстия протеза в полости ЛЖ (рис. 1).
Рис. 1.
ЭхоКГ изображение дискового протеза в митральной позиции.
а)
Апикальный доступ.
б)
Апикальный доступ, с увеличением.
в)
По короткой оси.
г)
С цветным картированием транспротезного потока.
Двустворчатые протезы, обладая меньшей по сравнению с дисковыми ПКС высотой профиля, соответствуют хирургическим требованиям частичного или полного сохранения хордального аппарата ЛЖ при протезировании митрального клапана [1-2]. Характер потока за двустворчатым клапаном в большей степени отвечает организации близкого к физиологическому типу транспротезного потока, способствующего более эффективному восстановлению геометрии полости ЛЖ (рис. 2).
Рис. 2.
ЭхоКГ изображение двустворчатого протеза в митральной позиции.
а)
Апикальный доступ.
б)
Апикальный доступ, с увеличением.
в)
По короткой оси.
г)
С цветным картированием транспротезного потока.
В многочисленных исследованиях установлено, что протезирование митрального клапана механическими протезами обоих типов приводит к достоверному улучшению геометрических и структурно-морфологических параметров всех полостей сердца. И дисковые, и двустворчатые протезы способствуют таким изменениям геометрии полостей сердца, которые приводят к улучшению внутрисердечной гемодинамики и повышению качества жизни больного. В исследованиях доказано, что конструктивные особенности протезов достоверно влияют на процессы ремоделирования полостей сердца. Имплантация двустворчатых протезов создает более благоприятные условия для восстановления внутрисердечной гемоди намики и геометрии сердца [1, 2, 5].
Наиболее близким к нативному является кровоток у биологических протезов: гибкие створки биопротеза в диастолу обеспечивают свободу просвета проходного отверстия клапана и создают гораздо меньшее препятствие для транспротезного кровотока. Кровоток через биологический протез носит преимущественно ламинарный характер, ориентированный по длинной оси ЛЖ к его верхушке (рис. 3).
Рис. 3.
ЭхоКГ изображение биологического протеза (Sorin Perikarbon) в митральной позиции.
а)
Апикальный доступ.
б)
Апикальный доступ, с увеличением.
в)
По короткой оси.
г)
С цветным картированием транспротезного потока.
При открытии протеза плоскости ксеноперикардиальных створок, прикрепленные к стойкам, создают некое подобие короткого сосуда, протяженностью равной высоте стоек каркаса протеза (что составляет 18-22 мм), за пределами которого вокруг ламинарного диастолического транспротезного потока возникают небольшие парапоточные завихрения, практически не искажающие ламинарный характер трансклапанного потока, его гемодинамические характеристики и направление [1, 2, 5].
По сравнению с механическими протезами в отдаленные сроки после протезирования у пациентов с биологическими протезами структурно-геометрические показатели сердца оказываются ближе к норме, чем у пациентов с механическими протезами [5], причем положительное ремоделирование полостей сердца после имплантации биологических протезов начинается уже в ранние послеоперационные сроки.
Также установлено, что при протезировании митрального клапана восстановление геометрии предсердий значительно отстает от восстановления желудочков. Поэтому полного восстановления нормального соотношения полостей сердца не происходит, но наступает значительное улучшение, о чем свидетельствует динамика значений соотношения объемов полостей сердца. ИРО позволил оценить степень патологического ремоделирования сердечных камер при приобретенных пороках митрального клапана до операции и на всех этапах хирургического лечения. Статистический анализ, проведенный нами ранее [1], подтвердил хорошее качество и высокую прогностическую достоверность предлагаемой модели оценки степени патологического ремоделирования сердечных камер по индексу ИРО. Были предложены три варианта сценария восстановления геометрии сердечных камер в зависимости от исходного уровня ИРО, отражающего степень патологического ремоделирования с прогностической оценкой восстановления геометрии сердца [1]:
- I тип (легкая степень) — область благоприятного прогноза (ИРО ≥ 0,9);
- II тип (средняя степень) — область неполного восстановления (ИРО 0,6-0,8);
- III тип (тяжелая степень) — область неблагоприятного прогноза (ИРО ≤ 0,5).
Данная классификация апробирована на 368 пациентах, распределенных на 3 группы в зависимости от типа протеза, имплантированного в митральную позицию. При сравнительном анализе особенностей ремоделирования сердца в этих группах достоверно установлена корреляция между характером изменений послеоперационного ремоделирования сердца и типом митрального протеза (рис. 4).
Рис. 4.
Изменение типа (степени тяжести) ремоделирования у пациентов:
а)
1-й группы с двустворчатыми протезами (%).
б)
2-й группы с дисковыми протезами (%).
в)
3-й группы с биологическими протезами (%).
Анализ геометрии сердца в исследуемых группах по типу ремоделирования до операции показал, что в 1-й группе у пациентов с двустворчатыми клапанами доля прогностически благоприятного I типа составляет 38,9%, что почти на 3,0% меньше, чем во 2-й группе больных с дисковыми протезами, и на 13,9% больше, чем в 3-й группе пациентов с биологическими протезами. Доля пациентов с прогностически неблагоприятным III типом оказалась наибольшей в группе пациентов с биологическими протезами и составила 50,0%. Это оказалось на 22,2% выше, чем в группе с двустворчатыми протезами, и на 15,7% больше, чем в группе с дисковыми протезами.
Восстановление внутрисердечной гемодинамики и соответственно геометрии полостей сердца во всех исследуемых группах началось практически сразу после операции (см. рис. 4).
В ранние сроки после протезирования митрального клапана незначительно увеличилась доля пациентов с I типом ремоделирования: в 1-й группе пациентов с двустворчатыми протезами — на 3,9%, в 3-й группе пациентов с биологическими протезами — на 16,6%. Во 2-й группе пациентов c дисковыми протезами доля лиц с I типом снизилась на 22,7%. Во всех группах достоверно уменьшилась доля лиц с прогностически неблагоприятным III типом ремоделирования: в 1-й — на 8,7%, во 2-й — на 9,3%, а в 3-й группе была отмечена наиболее выраженная положительная динамика (в ранние сроки после операции доля пациентов с III неблагоприятным типом ремоделирования снизилась на 41,7%).
В отдаленные сроки после операции в 1-й группе доля пациентов с I типом возросла еще на 23,9%, во 2-й группе — на 33,1% и в 3-й группе — на 47,3%. В результате доля пациентов с I типом в 1-й группе составила 66,7%, во 2-й группе — 52,2% и в 3-й — 88,9%. Доля пациентов с неблагоприятным III типом уменьшилась по сравнению с ранними послеоперационными сроками в 1-й группе еще на 12,4%, во 2-й — на 16,3% и в 3-й группе больных с III типом не осталось. В группах с механическими протезами доли пациентов с III типом оказались практически равными: 6,7% и 8,7% в 1-й и 2-й группах.
Доля пациентов со II, умеренно благоприятным типом ремоделирования в 1-й группе до операции составляла 33,3%, во 2-й — 23,8% и в 3-й — 50,0%. В ранние сроки после операции доля пациентов со II типом достоверно увеличилась во всех группах: в 1-й — на 4,8%, во 2-й — на 32,1% и 3-й — на 25,0%. В отдаленные сроки после операции она снизилась во всех группах: в 1-й — на 11,4%, во 2-й — на 16,5%, в 3-й — на 38,9%. В результате по сравнению с исходными данными доля пациентов со II типом ремоделирования в 1-й группе уменьшилась на 3,3%, в 3-й — на 13,9%, а во 2-й группе она увеличилась на 15,6%, по всей вероятности, за счет улучшения геометрии сердца у пациентов с III типом ремоделирования (см. рис. 4).
Структура транспротезных кровотоков, конструктивные и гемодинамические особенности различных типов протезов оказывают непосредственное влияние на интенсивность послеоперационного восстановления геометрии сердца. Поэтому уменьшение доли пациентов с I типом и увеличение со II типом в раннем послеоперационном периоде можно объяснить тем, что гемодинамика дисковых протезов в меньшей степени соответствует требованиям быстрого восстановления внутрисердечной гемодинамики и геометрии полостей сердца, чем у двустворчатых протезов. Поэтому в ранние послеоперационные сроки в группе лиц с дисковыми протезами, по-видимому, происходит адаптация к измененному транспротезному кровотоку, в результате чего и отмечается некоторый регресс геометрических параметров полостей сердца. Тем не менее применение дискового типа протезов для митральной позиции протезирования вполне оправдано, так как в течение 5 лет сердце постепенно адаптируется к специфике функционирования дискового протеза и геометрия сердечных камер постепенно восстанавливается, в результате чего доля пациентов с III, прогностически неблагоприятным типом ремоделирования у них практически сближается долей пациентов с двустворчатыми протезами. Структура кровотока через биологический протез максимально приближена к гемодинамическим характеристикам нативного клапана, создает наиболее благоприятные условия для восстановления геометрии сердечных камер. Именно в 3-й группе больных с биологическими протезами отмечена наиболее заметная положительная динамика в ремоделировании сердца по индексу ИРО. Помимо гемодинамических характеристик транспротезного кровотока, столь выраженной положительной динамике способствовало то, что в этой группе оказалось мало пациентов с ревматическим поражением митрального клапана, но все пациенты с отрывом хорд от створок митрального клапана оказались в этой группе.
В группе с биологическими протезами до операции доли пациентов с I и II типами оказались равными (по 25%), число пациентов с III типом составило 50%. Таким образом, пациентов с III, самым неблагоприятным типом ремоделирования в 3-й группе оказалось на 26,3% больше, чем в группе с двустворчатыми протезами, и на 15,7% больше, чем в группе с дисковыми протезами. Такое значительное количество пациентов с прогностически неблагоприятным типом ремоделирования находит объяснение: именно в группе с биологическими протезами оказалось самое большое количество пациентов с IV ФК (62,8%). Выраженность положительной динамики в ремоделировании сердечных камер отмечалась практически сразу после операции. Наконец, в исследовании отмечена выраженная положительная динамика у пациентов с III типом ремоделирования, доля которых уже в ранние сроки после операции уменьшилась на 41,7%, а в отдаленные сроки больных с этим типом ремоделирования в группе с биологическими протезами не осталось. Это вполне согласуется с закономерностями ремоделирования всех структурногеометрических параметров сердца в этой группе. Динамика значений указывает на то, что гемодинамические характеристики транспротезного кровотока через биологический протез наиболее приближены к нативным и создают условия, наиболее близкие к естественным, что создает условия, наиболее благоприятные для восстановления внутрисердечной гемодинамики и геометрии камер сердца (см. рис. 4, в).
Заключение
Настоящее исследование на клиническом материале подтвердило, что все виды протезов, имплантированных в митральную позицию, способствуют эффективному восстановлению внутрисердечной гемодинамики. На характер и интенсивность восстановления геометрии сердца достоверно оказывают влияние особенности транспротезного кровотока, обусловленные конструктивными характеристиками протеза. Представленные результаты исследования убедительно доказывают, что протезирование митрального клапана механическими протезами в отдаленные сроки после операции приводит в конечном итоге к идентичным результатам, но характер и сроки восстановления полостей сердца значительно различаются. Так, у пациентов с дисковыми протезами в ранние сроки после операции произошел достоверный регресс в геометрии сердца, который можно расценить как реакцию на специфику эксцентричного транспротезного кровотока с нарушенной однородностью и высокой скоростью течения, с образованием зон замедленного течения и т.д. Тем не менее дисковый протез достоверно улучшает внутрисердечную гемодинамику, что постепенно приводит к улучшению геометрии сердечных камер. Структуру транспротезного кровотока двустворчатого протеза, разделенного двумя симметричными створками, отличает более физиологичный характер. Поэтому уже в ранние сроки после операции отмечается положительная динамика в ремоделировании сердечных камер, которая в итоге приводит к значительному улучшению геометрии сердца. В результате пациентов с I, самым благоприятным типом ремоделирования в группе с двустворчатыми протезами стало на 14,5% больше, чем в группе с дисковыми протезами, а с III, самым неблагоприятным типом — на 2% меньше. Зато в группе с биологическими протезами в отдаленные сроки после операции пациентов с III типом не осталось совсем. Полностью открытое свободное проходное отверстие биологического протеза не создает препятствия для транспротезного кровотока, сохраняя его структуру аналогичной структуре кровотока на нативном митральном клапане человека, что способствует быстрому восстановлению геометрии сердца и переходу в более благоприятный тип ремоделирования уже в ранние сроки после операции. В отдаленные сроки самый благоприятный I тип ремоделирования в этой группе составил 88,9%, а II, умеренно благоприятный тип — 11,1%. Отсутствие в группе с биологическими протезами в отдаленные сроки после операции прогностически неблагоприятного III типа достоверно свидетельствует о том, насколько важным фактором в восстановлении геометрии сердца является характер транспротезного кровотока. Чем ближе к физиологическим параметрам характер транспротезного кровотока, тем быстрее и полноценнее восстанавливается геометрия сердца. Поэтому одним из продуктивных направлений усовершенствования конструктивной формы механического протеза является поиск решения, обеспечивающего максимальную свободу просвета проходного отверстия.
Выводы
- Восстановление геометрии сердца в отдаленные сроки после операции можно определять по динамике изменений индекса ИРО, который отражает переход состояния геометрии сердца из одного типа ремоделирования в другой.
- После протезирования митрального клапана геометрия сердца улучшается, но степень и характер восстановления достоверно зависят не только от характера и тяжести исходной патологии, но и от особенностей транспротезного кровотока, оказывающего влияние на процессы ремоделирования полостей сердца.
- Двустворчатые протезы являются более эффективными из всех современных механических протезов в митральной позиции для восстановления геометрии сердечных камер. Дисковые протезы в большей степени, чем двустворчатые, искажают нормальную физиологическую структуру кровотока, что приводит к нарушению однородности течения, превышению скоростей течения выше физиологических значений, образованию зон замедленного течения крови. Это может потребовать дополнительного времени для адаптации сердечных камер к измененному кровотоку и способствует умеренному регрессу ИРО сердечных камер в ранние сроки после операции, увеличивая общую продолжительность времени восстановления геометрической формы сердца.
- Наиболее выраженная положительная динамика в восстановлении геометрии полостей сердца отмечена при имплантации биологических протезов в митральную позицию. Полностью открытое свободное проходное отверстие биологического протеза не создает препятствия для транспротезного кровотока, сохраняя его структуру аналогичной структуре кровотока на нативном митральном клапане человека, что способствует быстрому восстановлению геометрии сердца и переходу в более благоприятный тип ремоделирования уже в ранние сроки после операции.
Литература
- Бокерия Л.А., Косарева Т.И., Макаренко В.Н. Типы патологического ремоделирования сердца у пациентов с приобретенными пороками митрального клапана // Клиническая физиология кровообращения. 2011 (в печати).
- Бокерия Л.А., Косарева Т.И., Макаренко В.Н. и др. Оценка соотношения объемов полостей сердца как индекса ремоделирования при приобретенных пороках митрального клапана // Клиническая физиология кровообращения. 2010. N1. С. 22-30.
- Бокерия Л.А., Косарева Т.И., Макаренко В.Н. и др. Ремоделирование полостей сердца в зависимости от типа механического протеза после митрального протезирования // Бюллетень НЦ ССХ им. АН. Бакулева «Сердечно-сосудистые заболевания». 2010. N6. С. 54-62.
- Ивлева О.В. Оценка процессов ремоделирования левого желудочка у пациентов с синусовым ритмом и фибрилляцией предсердий до и после протезирования митрального клапана. Дисс. …канд. мед. наук. М., 2008. 202 с.
- Косарева Т.И., Макаренко В.Н., Муратов Р.М., Фадеев А.А. Эхокардиографическая оценка ремоделирования полостей сердца при протезировании митрального клапана механическими и биологическими протезами // Клиническая физиология кровообращения. 2010. N2. С. 28-35.
- Abhayaratna W.P., Barnes M.E., Langins A.P. Reversal of left atrial remodeling in patients with «isolated» left ventricular diastolic dysfunction // J Am Coll Cardiol. 2007. N49 (Suppl A). P. 91A (abstr).
- Fiore A.C., Swartz M.T., Sharp T.G. Double-Valve Replacement with Medtronic-Hall or St. Jude Valve // Ann. Thorac. Surg. 1995. V. 59. P. 1113-1119.
- Greffe G., Henaine R., Metton O. et al. Choice of echocardiography method for postoperative evaluation of mitral valve replacement with a mechanical prosthesis // Arch. Cardiovasc. Dis.; 2008; 101(4): 204-212.
- Machler H., Gert R., Mathias P. et al. Influence of a tilting prosthetic mitral valve orientation on the left ventricular flow — an experimental in vivo magnetic resonance imaging study // Eur J Cardiothorac Surg. 2007. V. 32. P. 102-107.
- Machler H., Perthel M., Reiter G. et al. Influence of bileaflet prosthetic mitral orientation on left venticular flow — an experimental in vivo magnetic resonanse imaging study // Eur J Cardiothorac Surg. 2004. V. 26. P. 747-753.
УЗИ сканер HS50
Доступная эффективность.
Универсальный ультразвуковой сканер, компактный дизайн и инновационные возможности.
Противопоказания к имплантации
Протезирование не рекомендуют при:
- остром нарушении кровообращения;
- декомпенсированной сердечной недостаточности с ФВ<25- 20%;
- обострении астмы;
- диабете и почечной недостаточности;
- интоксикации на фоне вирусных или инфекционных заболеваний;
- печеночной недостаточности в стадии декомпенсации.
Выбор метода протезирования зависит от случая пациента, его основного диагноза, предполагающегося масштаба оперативного вмешательства и вердикта врача-кардиохирурга. При противопоказаниях к срочной операции требуется поддерживающая терапия для подготовки больного.
Реабилитация и возможные осложнения
По окончании успешно проведенного протезирования двое суток пациент находится в интенсивной терапии. Это необходимо для восстановления сил после наркоза, анестезии и седации. Срок пребывания в реанимации составляет двое-трое суток, далее в стационаре три-четыре недели. За это время происходит заживление раны на грудине, адаптация организма к гемодинамике после протезирования. На протяжении всего периода врач регулярно измеряет артериальное давление, оценивает на УЗИ состояние сердца, шва.
После малоинвазивной замены восстановление занимает не более семи-десяти дней. Учитывая малые размеры раны, заживление происходит быстрее, с менее выраженным болевым синдромом.
Реабилитация в послеоперационный период включает:
- Ограничение физической нагрузки в первую неделю.
- Постепенное увеличение двигательного режима в течение первых двух недель.
- Назначение лекарственной терапии для предупреждения тромбоза, закупорки клапана тромбом.
- Индивидуальный подбор режима нагрузок после восстановления гемодинамики.
- Специальную диету и контроль над состоянием.
Наиболее часто после протезирования беспокоят:
- общая слабость;
- иногда возникающее головокружение;
- головная боль;
- ноющая боль в области шва;
- периодические боли в сердце;
- отеки ног;
- нарушение сна.
Как правило, такие осложнения не постоянны и проходят в течение четырех-пяти недель после операции.
При ухудшении состояния обращаются к кардиологу или хирургу. Раннее обследование предупреждает оперативные последствия замены сердечного клапана и улучшает жизнь пациента.
Добрый день, дорогие друзья! Если вы перенесли операцию на клапанах сердца, то эта тема – для вас. Известно, что радикальным способом лечения больных с приобретенными пороками сердца является хирургическая коррекция клапанных поражений. Приобретённые пороки часто возникают вследствие ревматизма, инфекционного процесса на клапанах сердца или возрастной кальцификации клапанов (чаще аортального или митрального). Двустворчатый аортальный клапан (встречается у 1-2% населения, в норме он трёхстворчатый) быстрее изнашивается и нередко кальцифицируется в 50 – 60 лет. Клинически порок сердца проявляется одышкой, утомляемостью, сердцебиением при нагрузках. При появлении жалоб необходимо обратиться к врачу для прохождения обследования. Важно понимать, что оперативное вмешательство улучшает качество жизни. Операция по протезированию клапана сердца проводится в условиях искусственного кровообращения. Целью операции на клапане является нормализация кровотока в сердце. Пораженный клапан меняется на искусственный. В человеческом организме сроки работы искусственного клапана зависят от многих факторов, в том числе от образа жизни больного. Для поддержания здоровья пациентам, перенесшим операцию по коррекции клапанного порока сердца, необходимо регулярно проходить обследование в рамках диспансерного наблюдения и вести здоровый образ жизни. При удовлетворительном состоянии и отсутствии каких-либо осложнений посещать кардиолога нужно один-два раза в год. При изменении самочувствия пациента, график его динамического наблюдения меняется, осмотры проводятся от его состояния. После операции на клапанах сердца необходимо принимать назначенные врачом лекарственные препараты в чётком соответствии с полученными рекомендациями, важно соблюдение определенной диеты. Прекращать приём препаратов или самостоятельно изменять их дозу категорически запрещается. Если Вам имплантирован механический клапан, то будут назначены лекарственные препараты – антикоагулянты. Они разжижают кровь, чтобы предотвратить образование сгустков. Действие антикоагулянтов должно тщательно контролироваться с помощью анализа крови, называемого коагулограммой. Важно предупреждать развитие инфекции у больного с искусственным клапаном сердца. Немедленно обратитесь к врачу при следующих симптомах: – Внезапная или постепенно нарастающая одышка. – Временная слепота на один глаз или серая завеса перед глазами. – Слабость или онемение в области лица, ноги, руки, одной стороны тела, даже если они имели временный характер. – Невнятная речь, даже в течение короткого промежутка времени. – Необычно быстрое набирание веса, удерживание жидкости, отеки ног в области лодыжек (для контроля необходимо каждый день взвешиваться). – Слабость, особенно если она сопровождается лихорадкой, не проходящей в течение нескольких дней (врачи рекомендуют измерять температуру два раза в день в течение 2-3 недель). – Озноб или лихорадка с температурой выше 40°С. – Необычные кровотечения или кровоподтеки. – Стул темного или даже черного цвета, моча темного цвета, также обращайте внимание на наличие примеси крови в испражнениях. – Чувство жжения или изменения в частоте мочеиспускания. – Потеря сознания даже на короткий промежуток времени. – Внезапное изменение или отсутствие нормального звука или ощущения в вашем сердечном клапане в момент открывания и закрывания, а также в сердечном ритме и частоте. – Покраснение, отек, выделения или чувство дискомфорта в области шва. Образ жизни с искусственным клапаном сердца требует отказа от вредных привычек. Прежде всего, следует отказаться от курения, и лучше это сделать еще до операции. Контролируйте уровень артериального давления. Следует ограничить количество употребляемой соли, уменьшить количество животных жиров, жареных блюд, копченостей в пользу овощей, нежирных видов мяса и рыбы, все это поможет Вам надолго сохранить здоровье и избежать новых проблем.
Выводы
Прогноз протезирования благоприятный. Оперативное устранение пороков сердца, стеноза и недостаточности клапанов сердца снижает риск инвалидности, смерти от сердечной недостаточности и ощутимо улучшает самочувствие. После операции риск летального исхода связан с тромбозом крупных сосудов или участка имплантированного клапана. Крайне важно соблюдать рекомендации и назначения врача. Реабилитация в условиях санатория или кардиологического лечебного учреждения помогает поддерживать хорошее самочувствие долгие годы после оперативного вмешательства.