Когда возникает систолический шум в сердце
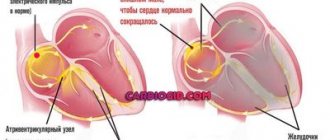
Патогенез явления простой. Систолический шум на верхушке сердца возникает вследствие нарушения линейного течения крови во время сокращения желудочков, в результате чего появляются завихрения, которые и создают дополнительные звуки. Это наблюдают при сужениях, аномальных образованиях, регургитации (патологическом возврате), ускорении кровотока (вследствие изменения состава, как при анемии).
Если нормальные тоны звучат как четкие удары, то патологические шумы напоминают жужжание, шипение, шорох. Они сопровождаются дополнительными феноменами – «кошачьим мурлыканьем» (диастолическое дрожание), проведением в аксиллярную область (район лопатки), учащенным сердцебиением.
В зависимости от этиологии подобного аускультативного феномена выделяют функциональные (еще они называются невинными) и органические шумы. К первым относятся все с преходящим характером. И при определенных условиях восстанавливается нормальное состояние. Второй тип возникает во время структурных изменений сердечных тканей. В этом случае процесс считается необоротным, а лечение затрудняется.
Функциональные (невинные) шумы появляются в таких случаях:
- физическое перенапряжение;
- нервное возбуждение и неврозы;
- лихорадка, инфекционные заболевания;
- гипертиреоз;
- анемический синдром;
- астеническая конституция;
- беременность;
- относительная недостаточность клапанов.
Органические шумы характерны для таких патологий:
- коарктация (сужение) аорты или легочных артерий;
- расширение аорты или других сосудов;
- недостаточность аортальных клапанов;
- добавочные аномальные хорды;
- митральная или трикуспидальная недостаточность;
- стеноз клапанов;
- комбинированные пороки.
У подростка 17-18 лет с астеническим телосложением в некоторых случаях на осмотре обнаруживают физиологический систолический шум, однако он считается вариантом нормы.
Шум в сердце ребенка
Шум в сердце ребенка является одной из самых частых причин обращения к детскому кардиологу и всегда вызывает тревогу родителей.
Статья опубликована в новом номере журнала Центра высоких медицинских технологий.
Читать весь выпуск
Что такое шум в сердце? Это звук, выслушиваемый в паузах между тонами сердца. Важны характер, тембр и продолжительность шума. Шумы сравнивают с тонами сердца, учитывают время возникновения относительно первого или второго тона, относительно фазы сокращения (систолический, либо диастолический), а также учитывают место наилучшего выслушивания (над аортой, легочной артерией, на верхушке). Соотношение точки прослушивания шума с анатомическим строением сердца позволяет врачу сделать предположение о причине возникновения шума. В зависимости от этого различают функциональные и органические шумы.
Функциональный шум — это особенность звуковых проявлений сердечной деятельности у здоровых детей (не связанных с нарушениями структуры сердца) и является физиологической особенностью детской сердечно- сосудистой системы. Функциональные шумы отражают процессы перестройки кровообращения, которые происходят в сердечно- сосудистой системе вследствие адаптации к вне утробной жизни. Они могут обнаруживаться с рождения и до подросткового возраста. Шум может быть постоянным и непостоянным, меняться от положения тела. Часто встречается при анемии, рахите, гипотрофии, заболеваниях, протекающих с повышением температуры тела (ОРВИ, ангина, пневмонии) и после нормализации состояния такой шум исчезает. Он также встречается у детей с узкой или плоской грудной клеткой, при дисплазии соединительной ткани (пролапсы митрального клапана). Самой частой причиной функционального шума являются хорды — это тяжи (нити) в полости левого желудочка сердца, которые, создавая шум, не мешают его работе. Функциональные шумы не сопровождаются нарушением кровообращения, у детей нет жалоб и не ограничена физическая активность.
Органические или патологические шумы могут быть врожденными (связанными с врожденными пороками сердца (ВПС) и приобретенными (чаще в результате инфекционного поражения клапанов сердца). При этом в той или иной степени нарушается кровообращение: у ребенка появляются жалобы на одышку, потливость, цианоз (посинение), отмечается снижение массы тела, пониженный аппетит, быстрая утомляемость и низкая физическая активность.
Шумы, вызванные ВПС, обычно обнаруживаются при рождении или на первых месяцах жизни ребенка, очень редко начинают выслушиваться через несколько лет. Такие шумы означают, что сердце неправильно сформировалось, имеется нарушение анатомической структуры: дефект (отверстие) перегородки, сужение (стеноз) магистрального сосуда, либо клапана сердца. Еще одна причина — недостаточность клапанов сердца, створки которых не смыкаются полностью, и возникает обратный ток крови (регургитация). Большинство пороков сердца может быть устранено с помощью оперативного лечения.
Шумы, вызванные приобретенным поражением сердца, связаны с воспалительным процессом, большинство случаев — в результате ревматизма, бактериального эндокардита. При этом у ребенка на первом месте будут симптомы инфекции: повышение температуры, изменение анализа крови, и ему будет показано медикаментозное лечение.
Выявить шум в сердце можно с помощью аускультации (прослушивания) сердечных тонов с помощью фонендоскопа. После этого педиатр рекомендует консультацию детского кардиолога, который проведет осмотр и направит на электрокардиографию (ЭКГ), чтобы выявить нагрузки на отделы сердца, а также эхокардиографию (ЭХО-КГ или УЗИ сердца), которая позволит точно выявить анатомическую причину шума. Затем детский кардиолог интерпретирует полученные данные. Для уточнения диагноза пациент может быть направлен на компьютерную томографию или магнитно-резонансную томографию, а если потребуется — и на ангиографию сердца.
Итак:
* Если у Вашего ребенка обнаружен шум, нужно выяснить причину его возникновения. Существует высокая вероятность, что он может носить функциональный («невинный») характер.
*Основной метод диагностики причины шума в сердце — эхокардиография или УЗИ сердца. Желательно провести исследование в родильном доме, в 1 месяц, далее по показаниям: перед началом посещения детского сада, школы и спортивной секции.
*При наличии врожденной патологии сердца необходимо наблюдение детского кардиолога, а если потребуется оперативное лечение — консультация кардиохирурга.
О чем говорит шум у ребенка
Выявление систолических шумов в сердце у ребенка еще не говорит об опасных заболеваниях. Часто у младенцев обнаруживают подобное состояние, однако причина – несовершенное развитие сердечно-сосудистой системы, непропорциональность определенных структур. Обычно это проходит с возрастом.
Еще один источник – индивидуальные врожденные особенности строения сердца (дополнительных хорд (тяжей, соединяющих сосочковые мышцы и клапаны)). Это считается вариантом нормы и не требует никакого лечения.
Часто такое явление развивается вследствие физических или нервных нагрузок, лихорадки или инфекционных болезней. Когда эти состояния проходят, систолические шумы исчезают.
Существует немало опасных болезней, при которых также выявляют этот диагностический признак. К ним относятся:
- дефект межжелудочковой перегородки – при этом происходит сброс крови из одного желудочка в другой;
- аномалии легочных вен и аорты – включают расширение или сужение (коарктацию) сосудов;
- врожденные пороки клапанов (недостаточность или стеноз) – при этом кровь возвращается в сердечные полости, или же с трудом проходит через суженный просвет;
- сочетанные патологии (тетрада, пентада Фалло) – совмещают сразу несколько аномалий развития.
В этом случае опасность намного большая, чаще подобные состояния требуют оперативного вмешательства. Тем не менее при раннем выявлении патологии и правильном лечении прогноз обычно благоприятен.
Ишемическая болезнь сердца и анемия
Чаще всего это увеличение работы ЛЖ (тахикардия, повышение систолического АД) или недостаточность коронарного кровотока (тромбообразование в венечных артериях, спазм). Реже как факторы, способствующие развитию или прогрессированию ИБС, рассматриваются снижение перфузионного давления (ДАД) или нарушение кислород-транспортной функции крови и т. д.
Для наглядности приводим выписки из историй болезни пациентов, у которых эти факторы играли роль «запускающего механизма». Мнение о том, что штаны принято носить только мужчинам, а женщины должны быть утонченные и элегантные, отдавая предпочтение юбкам и платьям, в нынешнее время абсолютно не актуально.
Клинический случай 1
Больной Ш., 84 года, был госпитализирован в мае 2013 г. с жалобами на давящие боли за грудиной при небольшой физической нагрузке и в покое.
Более 30 лет регистрируются высокие цифры АД (до 200/120 мм рт. ст.), сахарный диабет 2-го типа.
4 мес. назад перенес острый инфаркт миокарда без зубца Q боковой стенки левого желудочка. При коронарографии: передняя межжелудочковая ветвь (ПМЖВ) левой коронарной артерии (ЛКА) стенозирована в проксимальной трети на 50%, в дистальной трети — последовательные стенозы 30–50%; огибающая артерия (ОА) стенозирована в средней трети на 70%, правая коронарная артерия (ПКА) субокклюзирована в передней трети, окклюзирована в средней трети, дистальная часть слабо контрастируется по меж- и интраартериальным анастомозам. Выполнено стентирование средней трети ОА. Реканализацию ПКА выполнить не удалось.
Обращено внимание на наличие гипохромной анемии легкой степени (гемоглобин -106 г/л). Проведенное обследование возможного источника кровотечения не выявило. Выписан в удовлетворительном состоянии с рекомендацией приема ацетилсалициловой кислоты и клопидогрела, сахароснижающей терапии, препаратов железа.
Дома рекомендованные препараты принимал нерегулярно, врача не посещал.
Около 2 мес. назад отметил нарастание слабости. Стали беспокоить редкие приступы загрудинных болей. На ЭКГ от 10.05.13 г.: на фоне синусового ритма с ЧСС 75 уд./мин — выраженная депрессия сегмента ST в отведениях V2-6 (рис. 1). От предложенной госпитализации отказался.
Последние 2 нед. участились приступы загрудинных болей давящего характера, они стали возникать при минимальной физической нагрузке и в покое, сублингвальный прием нитроглицерина оказывал кратковременное действие, появилось чувство нехватки воздуха. Обратился в поликлинику, откуда был доставлен в ЦКБ с диагнозом «ИБС, прогрессирующая стенокардия».
При поступлении: кожные покровы бледные. Отеков нет. ЧД — 18 в 1 мин. Дыхание жесткое. Пульс — 72, АД — 140/70 мм рт. ст. на обеих руках. Систолический шум в точке Боткина и на верхушке, проводящийся в левую подмышечную область.
ЭКГ при поступлении (рис. 2): синусовый ритм с ЧСС 59 уд./мин, замедление атриовентрикулярной проводимости (PQ — 0,24 с). Замедление проводимости по левому предсердию и желудочку. Гипертрофия левого желудочка. Нарушение реполяризации в V2-5.
ЭхоКГ: гипертрофия миокарда ЛЖ (ММЛЖ — 240 г). Утолщение межжелудочковой перегородки (МЖП), более выраженное в базальной части (1,6–1,8 см), без признаков обструкции выходного отдела ЛЖ. Толщина ЗСЛЖ — 1,5 см. Сократительная способность миокарда ЛЖ удовлетворительная (ФВ по Тейхольцу — 63%), КСР — 3,6 см, КДР — 5,5 см, ЛП — 5,1 см. Зон нарушенной кинетики не выявлено. Изменение диастолической функции ЛЖ по первому типу.
В экстренном порядке выполнена коронароангиография (КАГ) (рис. 3): ствол ЛКА не изменен. ПМЖВ стенозирована на границе передней и средней третей на 50%, на протяжении дистальной трети — последовательные стенозы 30–60%. 1ДВ — анатомически некрупная, стенозирована в устье на 80%, окклюзирована в средней трети, дистальная часть слабо контрастируется по интерартериальным коллатералям. ВТК стенозирована в устье до 50%. ОВ анатомически крупная, проходима на всем протяжении, ранее имплантированные стенты — без стенотических изменений. ПКА субокклюзирована в передней трети, окклюзирована в средней трети, дистальная часть слабо контрастируется по меж- и интраартериальным анастомозам. Сбалансированный тип коронарного кровоснабжения.
Учитывая отсутствие динамики стенозов-КА по сравнению с КАГ от января 2013 г., чрескожное коронарное вмешательство не проводилось.
В анализе крови: гемоглобин — 61 г/л, эритроциты — 2,30×10*12, ЦП — 0,8, гематокрит — 18,5, лейкоциты — 7,7×10*9.
Кардиоспецифические ферменты (КФК МВ, тропонин Т) находились в пределах референсных значений.
В анализе мочи: удельный вес — 1020, белок — 0,15, лейкоциты — 0–5 в поле зрения, эритроциты — 100–150 в поле зрения.
Дополнительный целенаправленный расспрос позволил выяснить, что на протяжении последних 4 мес. неоднократно были эпизоды выделения темно-красной мочи, иногда длившиеся по несколько дней (макрогематурия?).
Убедительных данных, говорящих об остром очаговом поражении миокарда, на момент госпитализации не получено. Учитывая наличие анемии тяжелой степени, произведена трансфузия отмытых эритроцитов (1150 мл за 2 сут) с положительным эффектом: уровень гемоглобина повысился до 100 г/л, число эритроцитов — до 3,59×10*12, гематокрит — до 29,4.
На ЭКГ через 1 сут после последней гемотранфузии отмечается нормализация конечной части желудочковых комплексов в грудных отведениях (в V4 — зубец Т слабоотрицательный).
Самочувствие пациента значительно улучшилось: в течение последующих 3 сут при расширении двигательного режима до уровня физических нагрузок, соответствующих 3 функциональному классу, боли в грудной клетке не возникали, выраженность одышки существенно уменьшилась, объем нагрузок ограничивался главным образом мышечной утомляемостью. Эпизоды макрогематурии не повторялись. В удовлетворительном состоянии больной переведен для дообследования в урологическое отделение.
Клинический случай 2
Больной К., 50 лет, госпитализирован в стационар в декабре 2014 г. с клиникой прогрессирования стенокардии напряжения, одышки, возникающих при минимальной физической нагрузке, в покое, с нарастанием общей слабости в течение последнего месяца.
В анамнезе: АГ с максимально известными значениями АД 200/100 мм рт. ст. давностью более 15 лет; регулярно принимает антигипертензивные препараты, однако контроль АД нерегулярный. В 2002 г. перенес ОИМ, в этом же году выполнено аортокоронарное шунтирование (АКШ) ПМЖА, ПКА, ОА. В 2009 г. развилась клиника прогрессирующей стенокардии, в связи с чем выполнено стентирование шунта к ОВ ЛКА. В мае 2014 г. — повторный ОИМ задней стенки левого желудочка, проводился системный тромболизис, чрескожное коронарное вмешательство с реканализацией и стентированием АКШ к ОА. После выписки и до настоящей госпитализации — состояние стабильное.
Сопутствующие заболевания: сахарный диабет 2-го типа, мочекаменная болезнь, хронический геморрой, железодефицитная анемия легкой степени регистрируется с 2009 г. (препараты железа не принимал).
При поступлении: кожные покровы бледные, сухие. ЧД — 18 уд./мин. Дыхание жесткое, небольшое количество свистящих хрипов на выдохе. Тоны сердца глухие. ЧСС -76 уд./мин. АД — 150/90 мм рт. ст. на обеих руках.
ЭКГ зарегистрирована на фоне болевого приступа (рис. 4): ритм синусовый, ЧСС — 88 уд./мин, смещение сегмента ST вверх от изолинии в отведениях III, aVF, V1. В отведениях I и aVL смещение сегмента ST книзу от изолинии. Зубец Q длительностью 0,04 с во II, III, aVF отведениях.
ЭхоКГ: гипертрофия миокарда ЛЖ (ММЛЖ — 213 г, МЖП — 1,5 см, ЗСЛЖ — 1,2 см). Дилатация левого предсердия (5,3×6,1 см). Нарушение диастолической функции левого желудочка по первому типу. Гипокинез диафрагмального, заднебазального и заднебоковых сегментов. ФВ — 54% по Тейхольцу.
В общем анализе крови: гемоглобин — 70 г/л, эритроциты — 4,29×10*12, гематокрит -23,5, ЦП — 0,48, гипохромия, анизоцитоз, пойкилоцитоз (овалоциты, мишеневидные эритроциты), лейкоциты — 5,9×10*9. Сывороточное железо — 1,9.
Кардиоспецифические ферменты (КФК МВ, тропонин Т) находились в пределах референсных значений.
Таким образом, убедительных данных, свидетельствующих об остром очаговом поражении миокарда, на момент госпитализации не получено. Высказано предположение, что причиной прогрессирования стенокардии являлась тяжелая железодефицитная анемия, вероятнее всего, постгеморрагическая. Проведена трансфузия эритроцитной взвеси 630 мл за первые сутки, начато парентеральное введение препаратов железа.
Трансфузионную терапию перенес хорошо. Ангинозные боли не рецидивировали. На ЭКГ, зарегистрированной после гемотрансфузии (рис. 5): ЧСС — 62 уд./мин. Сегмент ST вернулся к изолинии.
В анализе крови спустя 1 сут: уровень гемоглобина возрос до 105 г/л, число эритроцитов — до 5,71×10*12, гематокрит — 38,3, ЦП — 0,55, гипохромия, анизоцитоз сохраняются. Лейкоциты — 8×10*9.
В течение 3 сут пациент находился в ОРИТ, антиангинальной терапии не требовалось, т. к. приступы стенокардии не рецидивировали.
Проводился поиск возможного источника кровопотери, онкопоиск: при колоноскопии выявлен хронический комбинированный геморрой 3 ст. Другой патологии, которая могла бы объяснить наличие анемии, не найдено.
Проводилось постепенное расширение двигательного режима. Физические нагрузки, соответствующие уровню 3 функционального класса, приступов стенокардии и ЭКГ-признаков ишемии миокарда не вызывают.
Через 12 дней в стабильном состоянии пациент выписан для дальнейшего лечения в амбулаторных условиях. Хирургом рекомендовано выполнение в плановом порядке дезартеризации геморроидальных узлов под ультразвуковым контролем.
Клинический случай 3
Больной З., 82 года, госпитализирован в стационар с жалобами на дискомфорт за грудиной, нехватку воздуха, возникающие без четкой связи с физической нагрузкой, длительностью до 4–5 мин, накануне был затяжной приступ длительностью более 1 ч, выраженную слабость, потливость. Настоящее ухудшение состояния отмечает в течение последних 3 дней на фоне появившейся гипотонии.
В течение 2 нед. до госпитализации принимал по поводу дорсалгии нестероидные противовоспалительные препараты (НПВП) (кеторолак). 4 дня назад отметил появление учащенного жидкого стула темной окраски, необычно низкое АД — 80/40 мм рт. ст.
В 1995 г. перенес ОИМ нижней стенки ЛЖ. В этом же году выполнено маммарно-коронарное шунтирование ПМЖА, АКШ ЗБВ ОА и ПКА. В 2003 г. — линейное аортобедренное шунтирование синтетическим протезом слева. Ранний послеоперационный период осложнился развитием повторного ОИМ нижней стенки ЛЖ.
С 2009 г. — пароксизмы мерцательной тахиаритмии.
Постоянно принимает бисопролол — 2,5 мг/сут, периндоприл — 5 мг/сут, аторвастатин — 20 мг/сут, варфарин — 5 мг/сут. Контроль МНО не проводился более года.
При поступлении: кожные покровы и видимые слизистые бледные. Число дыханий — 20 в 1 мин. Дыхание ослабленное, жесткое. Тоны сердца глухие, ритмичные. ЧСС — 76 уд./мин. АД — 110/70 мм рт. ст.
Лабораторные данные: гемоглобин — 91 г/л, эритроциты — 3,93×10*12, гематокрит — 33,0, ЦП — 0,84, лейкоциты — 10,2–10,6×10*9, тромбоциты — 223×10*9, анизоцитоз, анизохромия.
Кардиоспецифические ферменты: КФК — 268 при поступлении, через 10 ч — 319, КФК МВ — 30 при поступлении, через 10 ч — 42, тропонин Т при поступлении — 177, через 10 ч — 538.
Сывороточное железо — 13 мкмоль, белки транспорта железа в границах нормы. Коагулограмма: АЧТВ — нет коагуляции, МНО — нет коагуляции, фибриноген — 3,3 г/л, Д-димер — 1147.
ЭКГ (рис. 6) при поступлении: синусовый ритм, АВ-блокада I ст., рубцовые изменения нижней стенки ЛЖ, смещение сегмента ST во II, III и avF отведениях, высокий R — в V1-2. Архив ЭКГ не предоставлен.
ЭхоКГ: склероз и кальциноз стенок аорты, кольца и створок АК. ММЛЖ — 204 г, толщина МЖП — 1,0 см, ЗСЛЖ — 1,0 см. Дилатация левых отделов сердца (ЛП — 4,5×5,5 см, левый желудочек: КСО — 92, КДО — 171). Относительная недостаточность МК II степени. Гипокинез среднего заднего и заднебокового сегментов ЛЖ. Снижение глобальной сократительной способности миокарда ЛЖ (ФВ по Тейхольцу — 47%). Диастолическая дисфункция левого желудочка первого типа.
С учетом жалоб, анамнеза, лабораторно-инструментальных данных у больного диагностирован повторный ОИМ диафрагмальной и заднебазальной локализации.
Не исключалось состоявшееся желудочно-кишечное кровотечение на фоне приема НПВП и орального антикоагулянта, в связи с чем экстренно выполнена ЭГДС: эндоскопические признаки хронического эзофагита, язва нижней трети пищевода Forrest II C. Острая язва желудка Forrest II B (без признаков продолжающегося кровотечения). Язва привратника Forrest I B (с признаками продолжающегося кровотечения). После эндоскопического инъекционного гемостаза кровотечение остановлено.
Причиной ОИМ, вероятно, явилась гипотония и анемия на фоне желудочно-кишечного кровотечения. Начата консервативная гемостатическая, противоязвенная терапия. От проведения КАГ с возможным чрескожным коронарным вмешательством решено воздержаться до стабилизации состояния.
На фоне лечения цифры АД стабилизировались на уровне 120/85 мм рт. ст., уровень гемоглобина повысился до 110 г/л, возросло число эритроцитов — до 5,71×10*12, гематокрит — 38,3, ЦП — 0,55, лейкоциты — 8×10*9, гипохромия, анизоцитоз сохраняются.
Уровень активности КФК снизился до 113 ед, МВ КФК — до 12,7, тропонина Т — до 225.
ЭГДС через 2 сут: язва нижней трети пищевода Forrest III, острая язва желудка Forrest III, язва привратника Forrest II С (отсутствие признаков кровотечения, появление в области дна фибрина).
На 3-й день пребывания в стационаре возобновились кратковременные приступы сжимающих болей за грудиной (2 приступа: во время приема пищи и при попытке сесть в кровати).
По экстренным показаниям выполнена коронароангиография (рис. 7): ствол ЛКА стенозирован на протяжении передней и средней трети до 70%, субокклюзирован в дистальной трети с переходом на устья ОВ и ПМЖВ; ПМЖВ субокклюзирована в устье, стенозирована в передней трети на 80%, окклюзирована в средней трети, дистальная часть контрастируется по функционирующему маммарно-коронарному шунту. ОВ субокклюзирована в устье, стенозирована в передней трети на 80%; ПКА субокклюзирована на протяжении передней и средней трети, окклюзирована на границе средней и дистальной третей, дистальная часть контрастируется по межартериальным анастомозам.
Правый тип коронарного кровоснабжения.
Маммарно-коронарный шунт из правой маммарной артерии в дистальной трети ПМЖВ проходим. Шунты к ОА и ПКА не визуализируются.
Попытка реканализации стенозированных артерий — без успеха в связи с выраженным кальцинозом.
В течение последующих суток — состояние с отрицательной динамикой: в виде учащения кратковременных приступов стенокардии, сопровождающихся выраженными ЭКГ-признаками ишемии миокарда (рис. 8). Отмечено снижение гемоглобина со 110 до 87 г/л, гематокрита — до 26,0.
Кардиоспецифические ферменты в пределах нормальных значений. ЭхоКГ: размер левых отделов сердца прежний, новых участков нарушения движений стенок ЛЖ не выявлено.
Гастроскопия: активное кровотечение из острого дефекта слизистой кардиоэзофагеального перехода (Forrest I). Эндоскопическая остановка кровотечения.
После переливания 600 мл эритроцитной взвеси состояние с положительной динамикой: ангинозные боли и ЭКГ-признаки ишемии миокарда не рецидивируют (рис. 9), восстановление уровня гемоглобина (110 г/л), эритроцитов (3,85×10*12), гематокрита -33,7.
При контрольной ЭГДС через 10 дней положительная динамика — уменьшение в размерах язвенных дефектов без признаков кровотечения.
На фоне терапии ингибиторами протонной помпы, β-блокаторами, клопидогрелом 75 мг/сут показатели красной крови стабильны, двигательный режим расширен и по уровню нагрузок соответствует 3 ФК.
ХМЭКГ: ритм синусовый, ЧСС (за сут/днем/ночью): 78/77/78 уд/мин, максимальная ЧСС — 99 уд/мин, минимальная — 64 уд/мин. Отмечается появление депрессии сегмента ST при увеличении ЧСС свыше 90 уд/мин.
Приведенные случаи демонстрируют возможность проявления коронарной недостаточности на фоне снижения кислород-транспортной способности крови как у пациентов с тяжелым, так и умеренным поражением коронарного русла. Устранение анемии во всех трех случаях способствовало повышению коронарного резерва и стабилизации состояния.
Диагностика и дальнейшие действия
Если у вас или вашего ребенка обнаружили систолический шум, это означает, что необходимо пройти дополнительные обследования, дабы выявить конкретную причину подобного явления.
При том используют такие диагностические процедуры:
- электрокардиографию (ЭКГ);
- холтеровское суточное ЭКГ-мониторирование;
- рентген органов грудной клетки;
- эхокардиографию (ультразвуковое исследование сердца);
- функциональные нагрузочные пробы (велоэргометрию, степ-тест);
- магнитно-резонансную или компьютерную томографию.
Делают соответствующие лабораторные тесты, которые включают общий и биохимический анализ крови и мочи, ревматические пробы, коагулограмму и другие специфические исследования.
Помимо этого, пациенту понадобится консультация ревматолога, аллерголога, эндокринолога. Если никаких органических изменений не обнаружено, то человека просто ставят на контроль. Это значит, что ему нужно периодически приходить в больницу для профилактического осмотра. Назначают и общеукрепляющие средства (ЛФК или физиотерапию). При выявлении серьезных патологий больному прописывают лечение.
Выводы
Систолические шумы появляются вследствие нарушения нормального кровотока в полостях сердца, изменения состава крови или присутствия преград и аномальных структур. Выслушиваются такие звуки в момент сокращения миокарда желудочков.
Функциональные (невинные) шумы возникают при патологических состояниях, не связанных с нарушением внутренней архитектоники сердца, и со временем обычно исчезают. Органические же развиваются во время структурных изменений и сигнализируют о серьезных заболеваниях. Для установления точной причины назначают дополнительные обследования.